[b]【前处理】自动转盘式连续液液提取仪提取[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]分析某桃汁的香气成分https://bbs.instrument.com.cn/topic/6958792[/b]
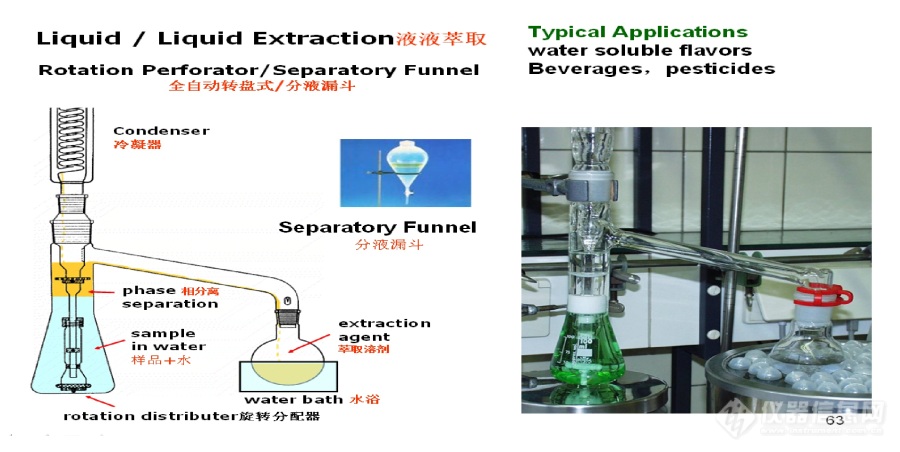
【前处理】自动转盘式连续液液提取仪提取[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]分析某桃汁的香气成分前言液-液萃取(liquid/liquid extraction,LLE)是一种最常用,最普通的提取挥发性香气组分的方法。其优点为容易操作,设备不贵,重线性好,热效应少,浓缩倍数高。适合于水质样品或水溶性溶剂样品,例如各种饮料、果汁中香气香味成分的提取。一般最简单的设备就是采用分液漏斗。操作常采用少量多次的萃取方法。需要加入样品和有机溶剂,人工不断的震摇,放气,分层,转移出有机相,然后反复几次后合并有机相,干燥浓缩供后[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质谱分析用。使用分液漏斗的优点是价格便宜,缺点是需要人工操作震荡、放气、分离有机相。想要摆脱人工操作,采用自动的液液萃取,可以使用自动转盘式连续液液提取仪。但缺点是设备费用要高些,萃取时间较分液漏斗长,但萃取效率高,节省人力。下面简单介绍一下自动转盘式连续液液提取仪的原理。从下面自动转盘式连续液液提取仪示意图看出,左边烧瓶中加入样品和水。右边烧瓶中加入提取溶剂。溶剂加热后进入冷凝管,冷凝后流入样品瓶。溶剂萃取样品中组分后,通过相分离又回到溶剂瓶。反复数次,最后把样品中的组分转移到溶剂中。[img=,690,346]https://ng1.17img.cn/bbsfiles/images/2018/09/201809091630227452_8396_1615838_3.jpg!w690x346.jpg[/img][align=center]图 1 自动转盘式连续液液提取仪示意图和实物图[/align]************************************************************本文采用自动转盘式连续液液提取仪提取桃汁的香气成分,用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质谱法分析鉴定。用Amdis质谱数据解卷积处理质谱数据,并结合保留指数校正使质谱检索结果更为准确。使用动态范围宽的FID来定量。[b]1试验部分[/b]1.1 仪器与装置安捷伦6890N/5973I[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱联用仪,带FID检测器,一根毛细管柱通过分流进入MS和FID。自动转盘式连续液液提取仪,德国Ludwig。1.2样品样品:10%桃味果汁饮料,样品购于某超市。乙醚,正戊烷均为色谱纯。乙醚使用前重新蒸馏。氯化钠为分析纯。香气化合物标准品均来自Sigma-Aldrich等主要试剂公司,少数为原料精制标样。C6-C30正构烷混合标准物来自AccuStandard。超纯水。1.3 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/MS条件1.3.1 色谱条件:色谱柱:安捷伦HP-Innowax(60m×0. 25 mm ( i.d.)×0.25μm)毛细管柱升温程序: 60℃,以3 ℃/min升至250℃,保持28 min;载气:He, 纯度99.999%以上,流速1.8 mL/min 进样口温度250℃,分流进样,分流比10:1 进样量:1μl。检测器:FID, 氢气:30ml/min, 空气:350ml/min, 尾吹:N2,30ml/min, 温度:270℃。1.3.2质谱条件: 电子轰击(EI)离子源;电子能量70eV;传输线温度250℃;离子源温度230℃;四级杆温度150℃。SCAN扫描范围:29-400。EMV:1550V。[b]1.4样品处理及分析方法[/b]采用自动转盘式连续液液提取(ALLE),准确取250g的10%桃味果汁饮料样品和0.6mg/kg的内标物加入自动转盘式连续液液提取仪样品烧瓶中,加入150g高纯氯化钠水至烧瓶径部10cm左右,在溶剂烧瓶中加入40ml乙醚/正戊烷(1:1混合)提取溶剂,并放几粒沸石。开启电磁搅拌适当速度,水浴加热至提取溶剂沸腾并开始回流。提取时间为2小时。萃取液用无水Na2SO4干燥后用K-D浓缩器浓缩到1ml。进样1微升进行[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]-MS/FID分析。在分析样品前,和样品分析完全相同的条件下,用0.05%的C6-C30的正构烷标样注射到[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]MS,获得正构烷的保留时间,用于计算保留指数。分析样品后,用软件计算样品各个组分的保留指数,并和标样的保留指数对比来,结合质谱来定性。事先也用同样方法测定标样的保留指数备用。[b]2 结果与讨论[/b]2.1. 实验结果10%桃味果汁饮料的总[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]图(TIC)如下:[img=,690,514]https://ng1.17img.cn/bbsfiles/images/2018/09/201809091630595344_5670_1615838_3.jpg!w690x514.jpg[/img][align=center]图2. 10%桃味果汁饮料的总[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]图(TIC)[/align]****************************************************2.2. 数据处理:先用Amdis质谱数据解卷积处理质谱数据,减少本底干扰,对共流出峰拆分,提取出大峰下面的峰或隐藏在里面的色谱峰。同时用Amdis的MSL质谱数据库和工作站的PBM(L)质谱数据库检索,并结合保留指数来鉴定峰。所有保留指数均由标准样品测定。极少数没有保留指数的化合物,参照其它资料和以往的经验,在保证良好匹配度的情况下确认。由于FID的动态线性范围很宽,定量结果稳定,复杂的多挥发性组分一般用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]FID来定量,而不用质谱总离子(TIC)来定量。用FID检测器的结果加校正因子计算10%桃味果汁饮料挥发性组分的含量。计算公式:Ci =( Ai/As)*Cs*Fi/sCi为香气组分浓度(mg/kg)Ai为香气组分峰面积As为内标物的峰面积CS为加入到样品的浓度(mg/kg)Fi/s为组分i相对内标物的相对校正因子。2.3. 10%桃味果汁饮料挥发性成分[align=center]表 10%桃味果汁饮料挥发性成分表[/align][table=21][tr][td] [/td][td] [/td][td] [/td][/tr][/table] [table=355][tr][td]No.[/td][td]组分名称[/td][td]浓度[/td][/tr][tr][td]1[/td][td]Ethyl Acetate[/td][td]0.080 [/td][/tr][tr][td]2[/td][td]ETHYL BUTYRATE[/td][td]0.116[/td][/tr][tr][td]3[/td][td]ETHYL METHYLBUTYRATE-2[/td][td]0.005[/td][/tr][tr][td]4[/td][td]LIMETOL[/td][td]0.009[/td][/tr][tr][td]5[/td][td]PENTEN-2-OL, 3E-[/td][td]0.038[/td][/tr][tr][td]6[/td][td]ISOAMYL ALCOHOL[/td][td]0.007[/td][/tr][tr][td]7[/td][td]LIMONENE[/td][td]0.088[/td][/tr][tr][td]8[/td][td]BUTYL BUTYRATE[/td][td]0.015[/td][/tr][tr][td]9[/td][td]OCIMENE Z-BETA[/td][td]0.003[/td][/tr][tr][td]10[/td][td]BUTANONE, 3-HYDROXY-3-METHYL-2-[/td][td]0.017[/td][/tr][tr][td]11[/td][td]OCIMENE E-BETA[/td][td]0.003[/td][/tr][tr][td]12[/td][td]CYMENE, P-[/td][td]0.007[/td][/tr][tr][td]13[/td][td]HEXENOL, 3Z-[/td][td]0.013[/td][/tr][tr][td]14[/td][td]ALDEHYDE C 8[/td][td]0.006[/td][/tr][tr][td]15[/td][td]PROPANOL, 2-OXO-[/td][td]0.009[/td][/tr][tr][td]16[/td][td]HEXENYL ACETATE, 3E-[/td][td]0.010[/td][/tr][tr][td]17[/td][td]HEXENYL ACETATE, 3Z-[/td][td]0.583[/td][/tr][tr][td]18[/td][td]ALCOHOL C 6[/td][td]0.026[/td][/tr][tr][td]19[/td][td]METHYLISOPROPYLTHIAZOLE, 4,2-[/td][td]0.285[/td][/tr][tr][td]20[/td][td]ROSEOXIDE, CIS-[/td][td]0.003[/td][/tr][tr][td]21[/td][td]HEXENOL, 3E-[/td][td]0.038[/td][/tr][tr][td]22[/td][td]HEXENOL, 3Z-[/td][td]1.900[/td][/tr][tr][td]23[/td][td]HEXENYL ISOBUTYRATE, 3E/Z-[/td][td]0.090[/td][/tr][tr][td]24[/td][td]ALDEHYDE C 9[/td][td]0.010[/td][/tr][tr][td]25[/td][td]HEXENOL, 4Z-[/td][td]0.012[/td][/tr][tr][td]26[/td][td]HEXYL BUTYRATE[/td][td]0.212[/td][/tr][tr][td]27[/td][td]LIMONENEPOXIDE, 1,2-Z-[/td][td]0.014[/td][/tr][tr][td]28[/td][td]FURFURAL[/td][td]1.126[/td][/tr][tr][td]29[/td][td]MENTHONE[/td][td]0.008[/td][/tr][tr][td]30[/td][td]CYCLOHEXANOL, 3,3,5-TRIMETHYL- P.1[/td][td]0.006[/td][/tr][tr][td]31[/td][td]BENZALDEHYDE[/td][td]0.305[/td][/tr][tr][td]32[/td][td]DIHYDRO LINALOOL[/td][td]0.040[/td][/tr][tr][td]33[/td][td]LINALOOL[/td][td]0.936[/td][/tr][tr][td]34[/td][td]TETRAHYDRO THIOPHENONE, 3-[/td][td]0.004[/td][/tr][tr][td]35[/td][td]2-HYDROXYPROPYL ACETATE[/td][td]0.030[/td][/tr][tr][td]36[/td][td]DIETHYL MALONATE[/td][td]1.096[/td][/tr][tr][td]37[/td][td]PROPYLENE GLYCOL, 1,2-[/td][td]1.796[/td][/tr][tr][td]38[/td][td]3-Decanol[/td][td]0.016[/td][/tr][tr][td]39[/td][td]ISOPHORONE[/td][td]0.012[/td][/tr][tr][td]40[/td][td]TERPINENOL, 4-[/td][td]0.006[/td][/tr][tr][td]41[/td][td]1-HYDROXY-2-PROPYL ACETATE[/td][td]0.030[/td][/tr][tr][td]42[/td][td]HEXYL CAPRONATE[/td][td]0.190[/td][/tr][tr][td]43[/td][td]BUTYRIC ACID[/td][td]0.164[/td][/tr][tr][td]44[/td][td]TERPINEOL, BETA-TRANS-[/td][td]0.006[/td][/tr][tr][td]45[/td][td]MENTHOL[/td][td]0.017[/td][/tr][tr][td]46[/td][td]DOWANOL DPnB P.1[/td][td]0.009[/td][/tr][tr][td]47[/td][td]METHYLBUTYRIC ACID, 2-[/td][td]0.602[/td][/tr][tr][td]48[/td][td]DOWANOL DPnB P.2[/td][td]0.014[/td][/tr][tr][td]49[/td][td]TERPINEOL, ALPHA-[/td][td]0.377[/td][/tr][tr][td]50[/td][td]2-HYDROXYPROPYL BUTYRATE[/td][td]0.021[/td][/tr][tr][td]51[/td][td]2-HYDROXYPROPYL BUTYRATE, 3-METHYL-[/td][td]0.008[/td][/tr][tr][td]52[/td][td]1-HYDROXY-2-PROPYL BUTYRATE[/td][td]0.010[/td][/tr][tr][td]53[/td][td]PROPYLENE GLYCOL TRIMER 6[/td][td]0.008[/td][/tr][tr][td]54[/td][td]CITRONELLOL[/td][td]0.007[/td][/tr][tr][td]55[/td][td]NEROL[/td][td]0.033[/td][/tr][tr][td]56[/td][td]PHENYLETHYL ALCOHOL, 1-[/td][td]0.012[/td][/tr][tr][td]57[/td][td]DAMASCONE, BETA-[/td][td]0.006[/td][/tr][tr][td]58[/td][td]DAMASCENONE, BETA-[/td][td]0.011[/td][/tr][tr][td]59[/td][td]GERANIOL[/td][td]0.120[/td][/tr][tr][td]60[/td][td]CAPRONIC ACID[/td][td]0.016[/td][/tr][tr][td]61[/td][td]OCTALACTONE, GAMMA-[/td][td]0.336[/td][/tr][tr][td]62[/td][td]IONONE, BETA-[/td][td]0.044[/td][/tr][tr][td]63[/td][td]OCTALACTONE, DELTA-[/td][td]0.022[/td][/tr][tr][td]64[/td][td]LINALOOL, 7-HYDROXY-6,7-DIHYDRO-[/td][td]0.176[/td][/tr][tr][td]65[/td][td]PYRONE, 3-HYDROXY-2-[/td][td]1.289[/td][/tr][tr][td]66[/td][td]ETHYLMALTOL[/td][td]0.376[/td][/tr][tr][td]67[/td][td]FURANEOL[/td][td]0.021[/td][/tr][tr][td]68[/td][td]CAPRYLIC ACID[/td][td]0.044[/td][/tr][tr][td]69[/td][td]TRIACETIN[/td][td]0.843[/td][/tr][tr][td]70[/td][td]MENTHOL, 8-HYDROXY, NEO-[/td][td]0.019[/td][/tr][tr][td]71[/td][td]LACTOJASMONE[/td][td]0.013[/td][/tr][tr][td]72[/td][td]DECALACTONE, GAMMA-[/td][td]1.900[/td][/tr][tr][td]73[/td][td]DECALACTONE, DELTA-[/td][td]0.129[/td][/tr][tr][td]74[/td][td]MASSOIALACTONE[/td][td]0.173[/td][/tr][tr][td]75[/td][td]JASMINLACTONE[/td][td]0.025[/td][/tr][tr][td]76[/td][td]GAMMA UNDECALACTONE[/td][td]0.298[/td][/tr][tr][td]77[/td][td]PYRONE, 3,5-DIHYDROXY-2-METHYL-4-[/td][td]0.009[/td][/tr][tr][td]78[/td][td]CAPRIC ACID[/td][td]0.037[/td][/tr][tr][td]79[/td][td]GERANIOL, 7-HYDROXY-6,7-DIHYDRO-[/td][td]0.011[/td][/tr][tr][td]80[/td][td]UNDECALACTONE, DELTA-[/td][td]0.111[/td][/tr][tr][td]81[/td][td]DODECALACTONE, DELTA-[/td][td]0.299[/td][/tr][tr][td]82[/td][td]HYDROXYMETHYLFURFURALE, 5-[/td][td]0.022[/td][/tr][tr][td]83[/td][td]VANILLIN[/td][td]0.100[/td][/tr][tr][td]84[/td][td]BENZYL BENZOATE[/td][td]0.284[/td][/tr][tr][td]85[/td][td]PALMITIC ACID[/td][td]0.003[/td][/tr][tr][td]Sum[/td][td]17.14[/td][/tr][/table] 从上述结果来看,从10%桃味果汁饮料里面一共鉴定测定了85个挥发性组分,总量约17.14mg/kg。样品含丰富的酯,醛,醇,酮,酸,内酯等化合物。酯类化合物提供各种香气:异佛尔酮,麦芽酚,紫罗兰酮,大马酮等提供桃子甜香味道;内酯有桃子特有味道;还有一些来自精油的成分。丙二醇为添加香精的溶剂。No.65,77,85等来自饮料样品基质的糖分。2.4. 使用自动转盘式连续液液提取仪可以减轻人的劳动,不用使用分液漏斗的人工不断的震摇,放气,分层,转移出有机相,合并有机相的操作。节省萃取溶剂,例如一般分液漏斗萃取需要40mlX4的萃取溶剂,而自动转盘式连续液液提取仪仅需要40ml萃取溶剂就可以。但缺点是设备费用要高些,萃取时间较分液漏斗长,但萃取效率高,节省人力。2.5. 对于某些含胶,蛋白的样品,和分液漏斗一样,自动转盘式连续液液提取仪也可能会产生乳化的问题,但控制好电磁搅拌速度就可以避免。2.6. 由于液液萃取需要有机溶剂来提取,需要浓缩。这样对于沸点极低的易挥发组分可能会有所损失。例如二甲基硫醚漏检,需要顶空或固相微萃取等其它前处理方法来弥补。2.7. 由于液液萃取是从水质样品或水溶性溶剂中提取,对于强极性化合物可能会有损失。例如麦芽酚(Maltol)等组分的回收率有影响。
氙灯耐候试验箱分为水冷氙灯和风冷氙灯,水冷氙灯样品架为转盘式,可以以每分钟1~5转的速度进行公转并且每一个小样品支架也会以每分钟1~5转的速度进行自转。那么,在试验过程中引起氙灯耐候试验箱转盘不转动的原因有哪些呢?下面雅士林技术员为您一一解答。 故障原因一:氙灯耐候试验箱转台开关未开启。 解决方法:1、检查转台开关打开状态;2、调节转盘转速。 故障原因二:测量转台电机是否有电压输入,电机是否有卡列现象,电机线圈是否有短路现象,电机电容是否有损坏。注:测量线路,一定要专业人来测量。 以上情况是针对购买了雅士林氙灯试验箱的用户。
据我所知:分二种 一:转盘式,二.转臂式.请各位高手华山论剑
硫酸稀释时,发出大量热,这个温度最大是多少?
安捷伦gcms自动进样器前进样塔转盘错识 代码222 大神们有没偶过
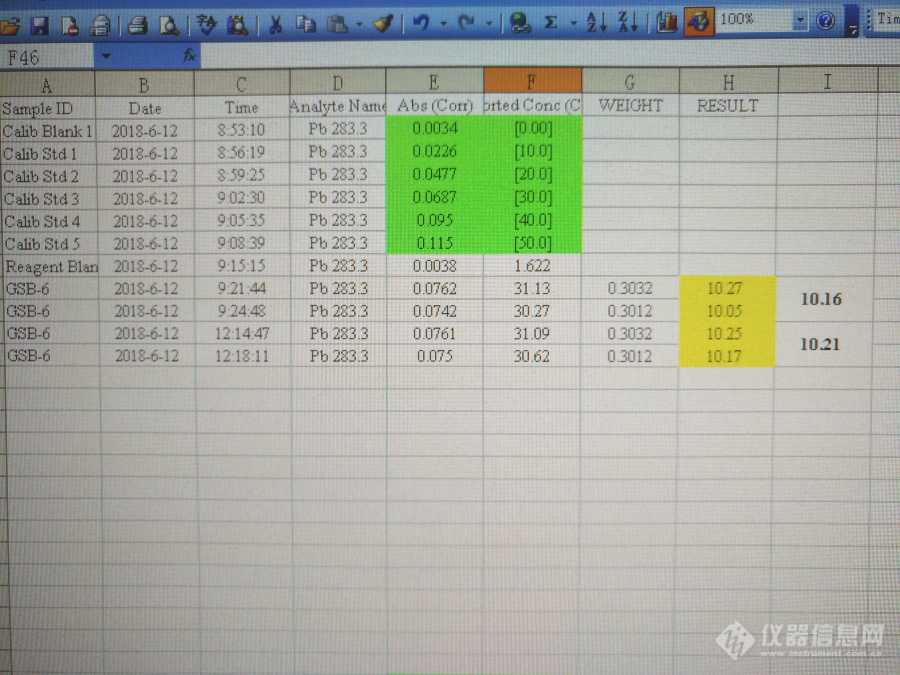
[align=center]前言[/align]自从用上了带有自动进样器的机子,感觉自己终于脱离了苦海。想当初,手持[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]往那小小的石墨管进样孔里面打样品溶液,啥也看不见,就象闭着眼睛一样,一下一下约摸着把那几微升样品溶液打进去!单说每天进几百枪的辛苦,能向谁述说?何况进样时擦碰刮蹭,导致测出来的数据昏天黑地,简直就是一场噩梦。现在有了它,一切便有了一个改观。而且,用上了自动进样器以后,我的测试数据也一天天地好了起来,而且连配制标液做标曲也可由它代劳了,于是对自动进样器这一神器感觉有点膜拜了。后来在论坛上看到安老师淡然谈到时说手动进样比自动进样更准确,我当时很不服气。然而,常言道:上的山多终遇虎。在一个偶然的情况下,我发现仪器自稀释与人工手动稀释有所差异,这才不再迷信盲从,于是有了下面的实验。1 方法与过程1.1 见图1.人工手动配制铅标准溶液系列:10ug/L、20ug/L、30ug/L、40ug/L、50ug/L,上机做校准曲线。标准物质GSB-6(菠菜)微波消解、赶酸定容后,再人工稀释4倍,上机测定。图1中红色方框内GSB-6的测定均值为10.16mg/kg,稍低(GSB-6的标值范围为11.1mg/kg±0.9mg/kg)。[align=center][img=,690,462]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021502561314_1930_2076515_3.jpg!w690x462.jpg[/img][/align][align=center]图1[/align][align=left]1.2 见图2 仪器自稀释配制铅标准溶液系列:12.5、25.0、37.5、50.0ug/L,做校准曲线。标准物质GSB-6(菠菜)与上述图1中所用为同一样品,即经微波消解后,再赶酸、定容,然后人工稀释4倍后,上机测定。图2中红色方框内GSB-6的测定均值为9.80mg/kg,明显低于图1中GSB-6的测定值。GSB-6(菠菜)的标值范围:11.1mg/kg±0.9mg/kg。[/align][align=center][img=,690,462]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021503378227_7192_2076515_3.jpg!w690x462.jpg[/img][/align][align=center]图2[/align][align=left] [/align][align=left]1.3 见图3 仪器自稀释配制铅标准溶液系列,12.5、25.0、37.5、50.0ug/L,做校准曲线。标准物质GSB-6(菠菜)经微波消解、赶酸定容后,再经仪器自稀释4倍后测定。图3中红色方框内GSB-6的测定值为12.31mg/kg,明显超过了标值上限。GSB-6(菠菜)的标值范围:11.1mg/kg±0.9mg/kg。[/align][align=center][img=,690,462]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021504049511_5133_2076515_3.jpg!w690x462.jpg[/img][/align][align=center]图3[/align][align=left]2 分析与讨论[/align][align=left]2.1 通过对比1.1与1.2可以看出,由仪器自稀释配制标液做标曲测出同一个样品GSB-6的铅含量低于人工配制标液做标曲的测定值。这表明这两种配制标液的方式不尽相同,仪器自稀释与人工手动稀释之间存在较大差异。[/align][align=left]图1中蓝色方框内为1.2中红色方框内GSB-6的测试数据代入1.1中校准方程进行计算,结果为10.21mg/kg,进入GSB-6的标值范围。[/align][align=left]图2中蓝色方框内为1.1中红色方框内GSB-6 的测试数据代入1.2中校准方程进行计算,结果为9.75mg/kg,明显低于GSB-6的标值下限。[/align][align=left]2.2 通过对比1.2与1.3可以看出,人工手动稀释GSB-6后的测定值显著低于仪器自稀释GSB-6后的测定值。由此可知仪器自稀释的取液量比人工手动偏大,将导致校准曲线的信号值偏高,而使测定值偏低,这一点从1.1与1.2的对比中得到印证。[/align][align=left]3 结论[/align][align=left]结论似乎就是一句话:仪器的自稀释不可靠啊!但是这样讲,未免太过武断。没有经过大量重复性的验证试验,没有看到大量重现性的验证结果,就这样简单地否定广大仪器公司殚精竭虑为我们制造出来的自动进样器不仅厂家不答应,广大自动进样器的忠实拥趸们也是不会答应的。实际上,就连本人也不愿意看到这样的结果。但是,这些数据毕竟是真实存在的现实。在这里,我只想提醒我们的同行,对此要留一个心眼。如果有不服的版友采用实验数据驳倒了我的结论,哪怕是把我体无完肤了,我心亦热。因为我真的很喜欢自动进样器![/align][align=left]谨以此文向安老师致意![/align][align=left] [/align]
同位素稀释法中有正稀释和反稀释,其原理是什么?还有是双同位素稀释?望各位赐教.
稀释制冷机(dilution refrigerator)1951年H.London提出可以用超流4He稀释3He的方法制冷的理论。到1965年P.Das等人根据这一理论制成了3He-4He稀释制冷机,目前已达到2mK的低温。它可以长时间地维持毫K范围的温度,有较大的冷却能力,已成为获得毫K温度的最重要的手段和设备。3He,4He的混合液在0.86K以上时,液3He可以以任何比例溶解在液4He中,但是当混合溶液的温度降到0.86K以下时,混合液则分离成两相,其中含3He多的相称为浓缩相,而含3He少的相称为稀释相。在低于0.86K的任一温度都对应于一定的3He含量的稀释相和浓缩相,并达到相平衡。当从稀释相中取走3He原子时,为了保持两相的平衡,则由浓缩相中的3He通过相界面进入稀释相以补充被移去的3He原子。可以计算得3He在稀释相中的焓和熵比在浓缩相中要大得多。所以这种稀释过程需要吸热,利用这个吸热现象制成了稀释制冷机。从稀释制冷机的结构图来看,包含相界面的室称做混合室,3He原子从浓缩相经过相界面进入稀释相要吸热而制冷,使温度降低。包含稀释相的自由表面的室称为蒸馏室,温度维持在0.6~0.7K。此时3He的饱和蒸气压远高于4He的饱和蒸气压,可以用抽气机抽走,这时浓缩相中的3He原子就不断地通过相界面进入稀释相,抽走的3He经过冷凝再补充到浓缩相中形成循环,使制冷机不断地运行。
讨论一下下
RT:7890B,,自动进样器转盘错误,代码222。没有规律的出错,一个序列160样品出错6次,在分析结果时才发现!
如题,如果水样不稀释,那么采用滤膜法检测耐热大肠菌群,可测定多少范围以内的结果,换句话说结果达到多少数量就需要对水样进行稀释了呢?
我们单位那台AAS没有自动稀释器,配标液很累,一次好多元素,每个配很多,而且测试时经常样品会OVER,感觉很不方便.请问大家,可以另外装个自动稀释的进样系统嘛,用自动稀释的测试准确度和自己配标液测试比,哪个更准
各位专家和版友,我用的是海光AFS-230E的自动进样器,在样品测得的结果超过标准曲线两倍的时候会出现是否要自动稀释的提示,然后选择自动稀释,输入稀释的倍数,自动进样器会根据输入的倍数的大小调节蠕动泵的快慢进行稀释,但是我发现稀释后的结果和我自己去手动稀释测出的结果相差挺大的,大的时候有2倍,都是自动稀释的大于手动稀释的,不知道原因在哪里?希望各位帮助小弟寻找一下原因,谢谢了!
稀释气设计的目的为了在线对样品溶液进行稀释,没有一种溶剂比纯净的氩气更干净,用氩气在雾化室后面引入系统,去稀释雾化的气溶胶,实现对样品的稀释是一个特别好的创新。使用这种技术,开发方法也更为简便,可以通过减小雾化气流速,增大稀释气的办法去改变进入仪器的样品浓度,还能避免稀释过程的污染。另外,用ICP火焰的燃料氩气去稀释,相对于溶剂稀释,待测元素强度降低得更少一些,对于Be这种难电离元素更是这样,在一定稀释倍数内强度甚至不降反升。 但是,因为引入了这一路气会带来一些其他影响。且有好有坏。两点好处:首先是空白的本底会变得更低一些,这就意味着信噪比因为稀释气的引入而有所增大,这一点是特别好的结果。其次,稀释气的稀释作用,会降低气溶胶的酸度,进而起到了保护锥的作用。 一点坏处:对于I,Au,Hg,B等容易残留的元素,因为稀释气的引入,会使气溶胶更干,减小了冲洗进样系统的作用,加重了残留效应。要根据实际情况去设置一个合理的稀释气流速,这个流速一定是根据实际情况去优化的,比较通用的流速肯定是比较低的(小于0.4ml/min)。比如做碘的时候,稀释气最好就设置为0;在Hg,Au等冲洗效果特别不好的时候,可以考虑把雾化气流速设置得高一些并且关掉稀释气。 稀释气还有提升气溶胶的作用,所以优化AMS气体时和优化雾化气流速类似,而并不是单纯的稀释作用。

氮吹仪采用氮气对加热的液体样本进行浓缩纯化,是化学,生物化学,有机化学等研究中对样本进行批处理常用的仪器。我对氮吹仪的了解基于我在脂肪酸提取过程中积累的经验。我的实验要求并不高,仅仅是将样品浓缩,所以没有采用进口的氮吹仪(其实我觉得对于一般的实验来说,像这种小仪器,国产和进口除了在价格上有着巨大的差距外,使用起来在性能上没有本质差异),但也使用过下面两种类型的国产氮吹仪。http://ng1.17img.cn/bbsfiles/images/2012/11/201211140850_404010_1306303_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/11/201211140850_404011_1306303_3.jpg对于这两种氮吹仪,不管厂家怎么描述的天花乱坠,使用过的人会有不同的感觉,尽管我后来一直使用转盘式的那款,但是个人仍旧更喜欢右侧的平板式的。下面简单的对两款氮吹仪进行比较:(1)我使用过的这两款都是水浴式的,在这一方面,转盘式的因为下面的水浴锅很大,需要的水很多,而平板式的需要的水却很少,操作更方便。(2)两款氮吹仪的体积差异显著,转盘式的看似很小,实际很大,我记得刚买回来的时候着实吓了我一跳,这对于狭小的实验室特别是通风厨来说实在不算有点。(3)两种类型的氮吹仪都可以单独调整气流,不过转盘式的调整起来比较麻烦,应为需要转动转盘才可以够到每一根针,这个也比平板式的要麻烦一些。(4)转盘式的因为转盘下面安装的弹簧经常泡在水里,并且每次实验都需要转动数次,所以弹簧比较容易损坏,我使用的那一台就在买后不久折了弹簧,耐用性没有平板式的好。(5)在堵针,坏针方面两者倒是差不多,我用过的两台好像在一大段时间后都有一两根不好用的针。(6)外观上,转盘式的看起来很高档,像是大家规秀,而平板式的更为简约,像小家碧玉。上述比较仅是我个人根据自己的使用心得进行的比较,只代表个人意见,供大家参考,并无针对性,刻意褒贬之意。
非甲烷总烃氮气作为稀释气,如果氮气不合格,是否可以把氮气按比例用高纯氧气稀释,之后作为稀释气使用
请问专家:我在进酰氯样品时总发现进样器内有气泡产生,用的是热导检测,产生了一个多余的峰,我估计是酰氯与不锈钢起反应。样品用溶剂稀释后也眼这种现象。现在用的是国产进样器,不知是否有更好的进样方法或进样器?若有耐腐蚀进样器请提供购买途径。
自动进样器自动稀释功能准么?有时候稀释后的数据和未自动稀释的差距很大不知道那个准些?如果不稀释的话,那被测点就超过范围了,超过范围的曲线一般是弯曲了,所以不稀释的化是不准确的吧?那仪器自己稀释后的数据可信么?请赐教!
http://www.instrument.com.cn/show/Breviary.asp?FileName=C243075%2Ejpg&iwidth=200&iHeight=200 深圳市清时捷科技有限公司 的 D-50精密稀释配液器(D-50)已参加“国产好仪器”活动并通过初审。自上市以来,这款产品已经被多家单位采用,如果您使用过此仪器设备或者对其有所了解,欢迎一起聊聊它各方面的情况。您还可以通过投票抽奖、参与调研等方式参与活动,并获得手机电子充值卡。【点击参与活动】 仪器简介: 产品简介:稀释配液器是一种对样品进行定量或连续稀释的仪器,适用于实验室精密稀释、标准曲线制作及标样稀释,以及医疗、生化制剂精确配液,批量定容分液等。其稀释过程完全模拟手工过程,定容准确度远远高于最精密的A级品容量瓶和人工操作,且随时可以校准,避免了手工操作时因为移液管质量参差不齐的问题而导致的稀释误差。产品特点:1.相对误差小于0.1%,定容准确度远远高于最精密的A级品容量瓶和人工操作。2.配备温度补偿探头,实现自动校准温度系数,弥补环境温度对稀释定容体积的影响,确保了不同温度下的高精度准确稀释、定容。3.专为解放日常实验过程中需要手工进行的稀释定容操作,解决制作标准曲线时跳点、线性不理想、标准系列计算复杂、稀释定容难的问题而研发。应用范围:可广泛应用于水质分析、化工、化纤、生物、化学、临床、食品分析、免疫检测等实验室精密稀释、标准曲线制作及标样稀释,以及医疗、生化制剂精确配液,批量定容分液等。【了解更多此仪器设备的信息】
越来越多的仪器上安装自动稀释系统了。可是对于一些低沸点、易挥发的有机溶剂,自动稀释系统怎样保证稀释的精准度呢?
我发现很多气体分析需要直接进样的,买的标气都需要稀释的,那你们的实验室是怎么稀释标准气体的?如果GC分析的时候用得是曲线酪校准定量的,你们又是怎么做这种T度的稀释的呢?
我是水系的GFC,主要做环境水样的分子量分布。流动相是水,样品也是水。用的是示差检测器。我想问的是:常常会有比较脏的样品(比如说过完滤膜的城市污水),因为怕污染柱子,常稀释样品10倍,100倍的,发现稀释前后得到的分子量分布是很不相同的。我很疑惑,是这样的吗?如果稀释完进样不能反应原样品的分子量分布,难道我能把那么脏的水直接进柱子?
我做过几次“水中卤代烃”的能力验证,每次都是发“甲醇中卤代烃”浓样。作业指导书上建议的稀释方法是:用10uL的微量注射器取浓样5uL,注入10mL水,稀释倍数是2000倍,报结果按稀释后的浓度。能力验证样品可以这样稀释,我们平时稀释标准溶液,需要大比例稀释的时候,能不能采取这种办法呢?毕竟操作比逐级稀释要省事。
本人现在遇到一个问题:在配标准溶液时,是逐级稀释好还是一步稀释(都从母液中吸取,然后定容)好?要提供数学计算依据。这个与误差传递有关,但我不会计算,哪位高人帮帮小弟。谢谢!急等![color=red][size=4]calfstone老师就对这个问题发表自己的看法,详情请点击:[/size][/color][URL=http://www.instrument.com.cn/bbs/shtml/20080520/1269771/]标准溶液稀释中的不确定度分析-兼对逐级稀释还是一步稀释哪个好的回答[/URL]
请教各位大虾:我用的是瓦里安AA240FS+GTA120,用的PDF120的自动进样器,由于样品浓度超过标准曲线的最高点,自动进样器在线自动稀释,第一次显示DF=2,但稀释后的样品上机仍超过标准曲线;则继续稀释上机,又显示DF=5,还是超标则再次稀释上机;显示DF=10,还是超标,且样品进样体积<1ul,无法再稀释,最终结果显示overed。我的问题是:DF 是什么意思,系统帮助表明为稀释系数,但我还是弄不懂:DF=10D到底是稀释了多少被呢?我的样品进样体积是10ul。
这样能挣上金币吗?逐级稀释和一步稀释的比较在日常分析中常常需要对溶液进行稀释。我们知道由于稀释的过程中会产生一些随机误差,而且误差随着稀释倍数的增加误差也随之增加,所以有些标准里会有逐级稀释到多少多少浓度,或者是每次稀释倍数不能超过20倍的明确要求。可是在实际操作中,当需要较大的稀释倍数的情况下,逐级稀释显然是费时费事的。那么可不可以进行一步稀释呢?我的同事找我提出了这个问题,当然是想省事了。尤其因为大多水样的矿化度很高,大量稀释的需要是在所难免的。我个人认为在保证质量可靠的情况下是可以一步稀释的。我建议同事做一下比较。同事于是对同一个未知样品分别进行两级稀释和一步稀释作为两个样品,然后对两个稀释样品进行了钙离子和硫酸根离子含量测定。一步稀释方法:用1.00mL移液器吸取1.00mL原液样品定容到100mL。此溶液为A液。两级稀释方法:先用5.00mL移液器吸取100mL原液样品定容到100mL。再用10mL大肚移液管从一级稀释液中吸取10.00mL溶液定容到50mL。此溶液为B液。测定方法:电感耦合等离子发射光谱法测钙离子,离子色谱法测硫酸根。测定结果:A液B液均值相对偏差钙离子mg/L10.3810.4710.420.38%曲线方程y=117800x-1750 r=1.000000硫酸根mg/L10.1510.1210.140.20%曲线方程y= r=结论是显而易见的。我认为在实际操作中可以一步直接稀释100倍。有这个数据作依据,我说你这么做就是了。可这个同事却去找领导,希望领导肯定并支持这样做法。很可惜领导没有同意。所以这个同事不得不仍然重复着大量的稀释和大量的清洗工作。不能理解同事这样做法。除非这组数据是编出来的,要么就是对自己的操作水平没自信,不然为何自讨苦吃?[f
由于样品溶度很高,但要精密测定,需要稀释很多倍数,为了实验简便操作,请问各位大虾,有没有稀释高溶度用的精密仪器??如果没有的话,请问可否用100微升的进样器代替,误差会比用移液管的误差大么??
楼主最近做了一个食品样,汞含量比较高,超出标曲最高点。于是准备稀释。第一次用水直接稀释20倍,得到浓度为1.0ppb左右,加标回收率算出来63%;第二次用5%硝酸稀释10倍,得到浓度为1.5ppb左右,加标回收率112%;第三次仪器自动稀释(载流5%hcl稀释)20倍,得到浓度为1.5左右,加标回收率145%。
实验室打算用稀释接种法测定BOD,请问下用什么设备曝气稀释水,求介绍