推荐厂家
暂无
暂无
 留言咨询
留言咨询
 留言咨询
留言咨询
 400-860-5168转2060
400-860-5168转2060
 留言咨询
留言咨询

 400-629-8889
400-629-8889
 留言咨询
留言咨询

 400-875-7187
400-875-7187
 留言咨询
留言咨询

 400-611-9236
400-611-9236
 留言咨询
留言咨询
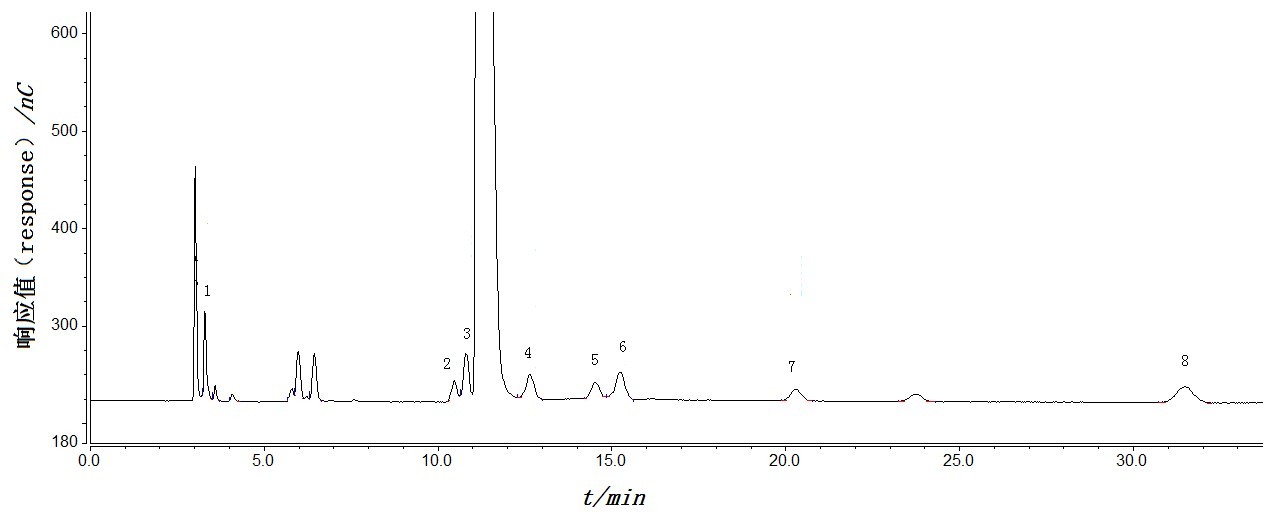




今天我们聊一款小众的色谱柱-氨基色谱柱,如果大家在实际使用过程中有遇到,可以参考。在高效液相色谱(HPLC)中,氨基色谱柱(NH2柱)是一种常用于正相和亲水性相互作用液相色谱(HILIC)的色谱柱。它通常用于分离糖类、脂溶性维生素、核苷酸和水溶性维生素等物质。 01.氨基色谱柱的组成 1)色谱柱管:色谱柱管通常是由不锈钢制成管状结构,用于容纳填料。 2)填料:通常由硅胶或聚合物基质组成。在氨基色谱柱中,填料是在硅胶或聚合物基质上键合了氨基(-NH2)官能团的球形颗粒。这些颗粒具有均匀的孔径分布,允许不同大小的分子进入孔隙内部。氨基官能团提供了亲水性相互作用和弱阴离子交换的特性,适合于分离极性化合物。 02.氨基色谱柱的分离机制 1)HILIC模式:在这种模式下,氨基色谱柱用作亲水性相互作用色谱柱,适用于糖类、糖醇等化合物的分析。流动相通常是水和有机溶剂(如乙腈)的混合物,通过调整流动相中水和有机溶剂的比例,可以控制分析物的保留行为。在HILIC模式下,氨基色谱柱的氨基提供了与极性化合物相互作用的位点,通过氢键和偶极-偶极相互作用实现保留 。 2)弱阴离子交换模式:在酸性流动相条件下,填料表面带正电荷,适用于水溶性维生素或核苷酸类的分析。这种模式下,氨基色谱柱的氨基官能团可以作为弱阴离子交换位点,通过离子交换作用保留带负电荷的分析物 。 3)正相模式:氨基色谱柱也可以在正相色谱中使用,分析酸性物质、烃类化合物、维生素A和D等。在正相色谱中,通常使用非极性流动相,氨基柱的氨基官能团可以与分析物形成氢键或其他极性相互作用 。(较少) 03.氨基色谱柱使用的注意事项 1)使用前: a. 检查色谱柱包装和标签:确保色谱柱没有物理损伤,确认色谱柱的规格和填料类型符合实验需求。 b. 阅读说明书:[font=&]仔细阅读色谱柱的使用说明书,了解色谱柱的pH稳定性范围、最大操作压力等参数。 c. 系统冲洗:使用适当的溶剂冲洗色谱系统,确保系统中没有气泡和污染物。 d. 色谱柱平衡:柱子需要用流动相平衡,直到基线稳定。HILIC模式下,通常需要平衡4~5小时。(有些甚至过夜平衡)注:如果上一个试验是无机盐的流动相试验,需要对仪器进行充分的冲洗,怕产生盐析;同理,如果是做了氨基柱的试验换成无机盐试验,也是要充分冲洗。 2)使用中: a. 流动相组成:确保流动相组成适合分析物和色谱柱,严格控制pH值在色谱柱的允许范围内(通常是pH 2-8)。注:如果是是无机盐与有机相的混合流动相,要注意加入的先后顺序,可能会有结晶析出 b. 样品溶解性:样品应在流动相中完全溶解,避免在柱上沉淀。 c. 流速控制:设置合适的流速,以获得最佳分离效果。 d. 样品负载:避免超载,以保持色谱峰形和分辨率。 e. 温度控制:根据需要调整柱温,以优化分离效果。 3)使用后: a. 柱子清洗:分析完成后,使用适当的溶剂冲洗色谱柱,以去除可能的污染物。 注:如果是含有无机盐-有机相的流动相 这个冲洗要先含有较多水的有机相进行冲洗(如95%水-乙腈),除盐→然后再转到高有机相冲洗(如95%乙腈水),除杂→再过渡置换成保存溶液 一般不要使用100%水冲洗色谱柱,氨基会水解。 b. 柱子保存:短期内如果不用,可以用与流动相相同组成的溶剂保存。长期不用,建议用色谱柱出厂时的保存液(如100%异丙醇)保存。 c.记录使用情况:记录色谱柱的使用情况,包括分析的样品、使用条件和色谱柱表现,以便于追踪柱效和寿命。 04.氨基色谱柱使用的局限性 1)pH值限制:氨基色谱柱的氨基官能团对pH值较为敏感,通常推荐的pH值使用范围是2-8。超出这个范围可能会加速氨基官能团的水解,从而缩短色谱柱的使用寿命。 2)溶剂兼容性:在反相条件下使用时,需要注意流动相中水的比例和pH值,因为高比例的水和极端的pH值可能导致官能团水解。 3)样品极性:氨基色谱柱对极性化合物的分离效果较好,但对非极性化合物的分离能力相对较弱。 4)样品负载:样品浓度和负载量不宜过高,以避免超载现象,导致色谱峰形变宽和分辨率下降。 5)温度敏感性:虽然适当的温度升高可以提高某些极性化合物的溶解度和分离效率,但过高的温度可能会加速色谱柱的老化。 6)缓冲盐类:如果流动相中含有缓冲盐,需要特别注意在分析前后使用不含盐的流动相进行适当的过渡,以避免盐类在柱内的析出。 7)保存溶剂:新购买的氨基柱的保存溶剂可能与使用的流动相不互溶(可能出厂保存在正相溶剂中,一般要用异丙醇置换),需要使用适当的溶剂进行过渡。 https://ng1.17img.cn/bbsfiles/images/2024/10/202410081129146844_2050_3203140_3.png!w490x14.jpg 总结一下:氨基色谱柱(NH2柱)在高效液相色谱(HPLC)中的角色有点像个分类专家,它通过分子的极性来区分它们。这种色谱柱是由不锈钢管和特殊填料构成的,填料上的氨基官能团能够与极性分子亲和,帮助我们把不同的分子分开。使用时,得注意几点:首先,pH值要控制在2到8之间,这样氨基官能团才能稳定工作。其次,样品要在流动相中溶解得好,免得在柱子里堵路。流速和温度也要适当调整,以保证分离效果。用完以后,别忘了用合适的溶剂冲洗,短期保存可以用流动相,长期的话最好用出厂时的保存液。氨基色谱柱虽然对极性分子分离有一手,但对非极性分子就不太灵了,而且它的分辨率和灵敏度可能不如其他类型的色谱柱。所以,如果你的样品极性很强,氨基色谱柱是个好选择,但要是分子大小差不多,或者你需要高分辨率和灵敏度,那就可能得考虑其他色谱柱了。总的来说,氨基色谱柱是个实用的工具,特别适合分析那些对环境条件敏感的极性分子。
承接上回,我们说了一下氨基色谱柱的原理、构造、分离机制、使用过程中的注意事项及它的局限性,今天主要说说它的维护保养和相关的注意事项,色谱柱固有一死,但好的操作还是能延缓它的生命周期的。 01.氨基色谱柱的维护由于氨基柱是一款既可以正相使用,也可以反相使用,但是我们要注意到的是:正相溶剂和反相溶剂往往是不互溶的,正常情况新氨基柱出厂时保存在正相环境中(如Luna的氨基柱保存在正己烷-乙腈(99:1)中)。 1)正相体系的维护 a. 推荐先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再根据流动相选用极性相近的氯仿或二氯甲烷以相同的流速冲10倍柱体积,最后换成你实验的流动相。 b. 正相使用时,不宜分析含醛基、羰基的化合物,不可用于还原糖的分析;流动相要彻底脱气,并不得含有羰基化合物和过氧化物(质量不好的乙醚、四氢呋喃含有少量)。 c. 任何时候更换流动相时都要确保新流动相与柱子原保存液可互溶。d. 使用前要确认仪器是否耐受正相溶剂,如果泵相关的密封圈组件不耐受,会造成损害。 2)反相体系的维护以上述色谱柱保存在正相溶剂正己烷-乙腈(99:1)为例,一般用以下方法进行置换操作: a. 在进行过渡置换前,需要把仪器的整个系统都用异丙醇冲洗(你需要测柱效涉及的管路),包括检测器,保证仪器是无水的一个状态。 b. 由于新的氨基柱保存在正己烷-乙腈(99:1)中,与反相流动相是不互溶的,因此如果使用反相的方法,[color=#595959]必须用至少10倍柱体积的异丙醇冲洗过渡(至少2h,0.5mL/min),以除去正相保存溶液。过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。 c. 再用至少10倍柱体积95%水-5%乙腈(或甲醇)冲洗(不含缓冲盐的流动相可省去)过渡,最后用流动相平衡。(可能每家色谱柱会有不同,但是就是不建议用100%的水去过渡色谱柱) d. 用完后洗柱时,必须先用95%水冲洗至少10倍柱体积,除去所用缓冲盐(不含缓冲盐的流动相可省去)。然后保存于乙腈/水(80:20)溶液(一个月内)中。长期不用的话,建议用异丙醇保存(一个月以上)。(不同厂家的色谱柱可按照说明书执行)其他:当使用氨基柱进行酸性物质的分析时,酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。---------建议用10-15倍的柱体积的为pH=11 NH3的乙腈-水(50:50)溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。 注:反相条件下使用时,要特别注意控制pH值范围(根据你色谱柱耐受使用pH),pH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。 02.氨基色谱柱的注意事项[font=PingFang SC, system-ui, -apple-system, BlinkMacSystemFont, Helvetica Neue, Hiragino Sans GB, Microsoft YaHei UI, Microsoft YaHei, Arial, sans-serif]关于它的注意事项,前面也上一篇也基本涵盖了使用中的注意事项和它自身的一些局限性的事项,这里就不再重复阐述,详见高效液相色谱基础篇|关于氨基色谱柱使用的小知识。这里只是再次提醒大家在使用过程中强调注意的几点: 1.如果用正相体系,确保仪器可耐受; 2.如果用反相体系,仪器要充分的平衡; 3.如果柱子保存是正相溶剂,仪器也要充分的过渡,以免溶液分层造成检测器波动; 4. 如果是反相体系,流动相平衡时间要长(至少6个小时跑不了,我一般都过夜平衡) 5. 及时记录色谱柱状态,做好维护管理;如果氨基水解了,一般较难再生,建议更换。 https://ng1.17img.cn/bbsfiles/images/2024/10/202410081133544526_2231_3203140_3.png!w490x14.jpg 总结一下:氨基色谱柱的维护保养其实挺讲究的。首先,你得搞清楚你的柱子是正相用还是反相用,因为这俩用的溶剂不互溶。如果是正相,就用正己烷-乙腈之类的冲一冲,换成氯仿或者二氯甲烷再冲冲,最后换成你的流动相。正相的时候别用那些含醛基、羰基的化合物,也别分析还原糖。反相的话就稍微复杂了点,先得用异丙醇把仪器整个系统冲洗一遍,确保无水状态。然后,因为新柱子有些是正相溶剂里保存的,所以得用异丙醇过渡,至少冲个两小时,避免正相溶剂在仪器中与其他溶液分层。接着用不含缓冲盐的水-乙腈(或甲醇)冲洗,最后用流动相平衡。用完记得先用95%的水冲洗,再保存在乙腈/水溶液中,长期不用的话就用异丙醇。还要注意的是,如果你分析的是酸性物质,氨基柱可能会质子化,影响保留性质或者柱效。这时可以用pH=11的NH3的乙腈-水溶液冲洗,分析时流动相里稍微加点氨。最后,使用前要注意仪器是否耐受正相溶剂,反相体系要充分平衡,柱子保存的如果是正相溶剂,仪器也要充分过渡。反相体系的流动相平衡时间要长,至少得过夜。同时也要及时记录柱子的状态,做好维护。如果氨基水解了,那柱子就差不多该换了。
11、怎么通过选择合适的柱子来提高分离度?答:提高分离度可从三个主要影响因素来考虑,柱效、选择性和保留因子。可通过减小填料粒径和增加柱长提高柱效;选择性和固定相选择以及pH条件有关,通过选择合适的色谱柱和合适的pH,可以提高选择性;有时候适当延长出峰时间增加保留因子,也可提高分离度。12、流动相走空了,液相色谱柱还能用吗?如果可以应该如何再生?答:能用的!可能柱子里会有气泡进去,但之后多用流动相冲冲,看到基线稳定,就没问题了。用色谱柱的保存液低流速长时间冲洗,然后再检测一下柱效,看柱子是否恢复,液相最好设置一下最低压限,这样就不怕流动相走光而会损伤色谱柱。11、如何改善峰形?(前伸峰、拖尾峰)答:前伸峰是由于色谱柱过载。当一种或多种化合物的进样量超过色谱柱固定相容量时,可能发生这种情况。液相膜越薄,色谱柱中保留的每种化合物就越少。这涉及到进样体积和进样中每个峰的化合物浓度。通过减少进样量、分流样品或进样浓度较低的样品,可减小进样体积。12、氨基柱时,有时候峰型突然变宽,有拖尾,用一段时间就又好了,什么原因,如何再生?如果可以冲的话,一般冲多久?答:氨基柱的硅胶孔内的氨基浓度非常高(大约有1mol/L),在有水存在的时候,在孔内形成一个pH10左右甚至超过10的很强的碱性小环境,并会导致硅胶基体慢慢溶解。不过硅胶基体的溶解会生成酸性的硅醇基,又会降低孔内的pH值,延缓硅胶基体的溶解进程。一段时间后,两个相反的过程会达成一个动态平衡,从而稳定下来。对你问题提到的这个现象,我想到的是这个原因。氨基柱,要看氨基柱的应用模式,是正相还是HILIC?这两种模式的情况是大不相同的。正相使用,一般很怕有水。但HILIC模式应用,一般流动相是乙腈/水,是不怕水的。不过键合氨丙基基团非常容易水解,所以一般氨基柱不适宜保存有水的溶剂中。作为正相应用时,流动相中要求一点都不能含水,但清洗柱子上的污染物质,是可以含水的,因为水有强极性,在正相色谱上洗脱能力极强,当然不必用100%纯水。氨基柱具体冲洗方法,正相条件按照正相硅胶柱的清洗方法,HILIC模式按C18柱的清洗方法。氨基柱,要看氨基柱的应用模式,是正相还是HILIC?这两种模式的情况是大不相同的。正相使用,一般很怕有水。但HILIC模式应用,一般流动相是乙腈/水,是不怕水的。不过键合氨丙基基团非常容易水解,所以一般氨基柱不适宜保存有水的溶剂中。作为正相应用时,流动相中要求一点都不能含水,但清洗柱子上的污染物质,是可以含水的,因为水有强极性,在正相色谱上洗脱能力极强,当然不必用100%纯水。氨基柱具体冲洗方法,正相条件按照正相硅胶柱的清洗方法,HILIC模式按C18柱的清洗方法。13、C18如果之前曾有些天一直保存在酸性环境中,会对柱子有什么损坏吗?pH在2左右。答:pH2左右容易使键合在硅胶基质上的固定相水解流失,包括C18和封尾试剂的水解,封尾试剂相对更容易水解。不知道你保存的酸性环境是不是含有缓冲盐,如果不含缓冲盐,只是短期几天保存在酸性流动相中,也不必过份担心,最多相当于这几天一直在使用这根色谱柱,因此减少几天的使用寿命吧;有缓冲盐就麻烦一点,保存期间水分挥发可能会导致缓冲盐结晶在柱内析出,对柱子损伤很大。14、色谱柱的安装有什么技巧?还有所谓的死体积怎么测定呢?答:色谱柱安装技巧不多,只要接头和柱头匹配,确实拧紧不漏就可以了,但也要注意不要拧得太紧以至于损伤螺纹。所谓死体积就是完全不保留的物质出峰时从进样到流过色谱柱的总体积,一般用极性非常强的尿嘧啶的出峰来测定。死体积包括柱体积(色谱柱内溶剂能占据的空腔体积)和柱外体积两部分。你从厂商这里买到色谱柱,柱体积已经是固定了,你能尽量避免减少的是柱外体积。进样器内死体积、毛细管长度、毛细管和色谱柱连接紧凑与否,保护柱或在线滤器产生的死体积大小,都对这个有影响。样品在柱内,除扩散外,还有和填料作用引起的组分分离;但样品在柱外,那就只有扩散这个使柱效下降的因素了。所以,要取得好的分离效率,柱外体积应该是越小越好。峰有时候前延,有时候拖尾,一般不是色谱柱的问题,应该是样品和色谱柱填料的作用问题,可以说如果色谱柱类型选择没问题,关键就是色谱条件的选择。包括进样量、样品溶剂、流动相组成(包括添加剂)、流动相pH以及柱温,都对峰形有影响。另外测定分子量较大的多肽,用样品老化平衡色谱柱很重要,分子量越大的物质,需要平衡时间越长。如果柱子没平衡好,峰形也可能会不正常。所以最好把你具体的测定条件也列一下,也便于有针对性的分析原因。15、柱塞板可不可拆下用超声波清洗,会有什么不良后果?答:不建议将柱筛板拆下清洗,因为拆下承压的柱筛板会导致柱床发生变化,影响色谱性能。应该对污染的色谱柱先进行清洗维护,维护没有效果,再把拆洗柱筛板作为最后的手段。16、CN基柱应该怎样维护才好呢?比如做完实验用什么流动相冲柱子、短期用什么溶剂保存、长期用什么溶剂保存等等。答:CN可作正相柱,也可作反相柱用,除了保存溶剂有特殊要求外,其它维护办法和一般正相和反相柱没有多大区别。17、色谱分析运行时,标样和样品的峰均随时间加宽答:如果保留时间没有很大区别,只是加宽的峰拖尾,可能表明有活化点。如果加宽的峰是对称的,可能是由于正常的色谱柱“损耗和流失”。如果峰前伸,说明色谱柱过载。18、排除色谱柱流失问题的最佳方法是什么?答:诊断色谱柱是否存在流失问题的最佳方法是第一次在方法条件下安装色谱柱时,做一次空白色谱图,然后将最近的运行和空白运行色谱图对比。如果在空白运行中产生了很多峰,则色谱柱性能改变,这可能是由于载气中含有氧气,也可能是由于样品残留。如果有GC-MS,则低极性色谱柱的典型流失离子(例如DB/HP-1或5)质/荷比m/z将为207、73、281、355等,大多数为环硅氧烷。19、请问我做一种药的分析,查美国药典规定使用100mm×40mm8μm色谱柱,流速3mLmin。可现在市场上已不容易找到这种规格的产品,于是我按USP中色谱柱比较的数据库的指引,选了一款选择性一致的等价色谱柱,其规格是100mm×46mm3μm的色谱柱,当选用3mLmin的流速时发现柱压超高,请问我如何对方法进行调整以满足USP的要求?答:流速调整原则是流动相通过柱子的线速度一致,等价柱的截面积大了,流速也应增加才能保持相同的线速度。新流速计算结果是:(4.6/4.0)2x3.0=4.0ml/min。但3ml/min流速都已导致柱压太高,4.0ml/min明显不行。好在USP还有个允许±50%的流速调整指导原则,这样将流速调至2.0ml/min既符合USP规定,又能使柱压降到可接受的范围,但这种改变不能引起其它不好后果。这个例子中,等度分析中,流速改变会引起塔板数和峰宽的改变,但不会影响峰的选择性。3um粒径色谱柱柱效比8um的高很多,可考虑缩短柱长以补偿或部分补偿流速降低造成的测定时间增加。所以,更佳选择是50mm×4.6mm,3μm的柱子,2.0ml/min的流速运行,可以在符合USP规定的情况下,又得到更快速的测定分离。20、最近我非常的沮丧,按照药典上的色谱条件和方法做某药物的分析,却始终得不到满意的结果。有人建议我对色谱条件,如进样量、流动相pH和温度等,进行微调以得到良好的峰形和分离效果,可按公司规定我不能这样做,怎么办?答:如果你心里老有这个思维定势“按规定,我不能......”,然后什么也不敢做,那真是不好办!只有去做了,去试着改变条件看看得到什么结果,你才能发现问题所在。如果改变条件后,仍得不到好结果,就要去找色谱条件以外的原因,如色谱柱、色谱仪器以及样品和制样过程中的是否存在问题?不管通过微调你是否取得了好结果,你也有了向领导汇报问题和解决方案的依据。而且,绝对不能调整药典规定色谱条件的说法通常是不对的。美国药典USP说的是如果改变药典方法需要重新做方法验证,但方法调整或者称微调以符合系统适应性的要求是允许的,是不需要重新做方法验证的。USP列了调整的几条指导原则,如±50%的流速调整,±10℃的温度调节等等(详见"Chapter 621,Chromatography," United States Pharmacopeia No. 31-NF 26, (2008).)。当然既然是指导原则,这些规定都不是绝对的,如温度