植物细胞原生质体制制备与融合2006-11-20 17:14植物细胞原生质体制制备与融合1、原生质体常现的杂交育种由于物种间难以逾越的天然屏障而举步维艰。科学家们受细胞全能性理论及组织培养成功的启示,逐渐将眼光转向细胞融合,试图用这种崭 图3-2新的手段冲破自然界的禁钢。1937年michel率先实施植物细胞融合的试验。如何去除坚韧的细胞'接成了牛物学工作者必须解决的首要难题。196O年该领域终于出现了重大突破。由英国诺丁汉大学Cocking教授领导的小组率先利用真菌纤维素酶,成功地制备出了大量具有高度活性可再生的番茄幼根细胞原生质体,开辟了原生质体融合研究的新阶段。植物细胞原生质体是指那些已去除全部细胞壁的细胞。2、原生质体制备(1)取材与除菌 为了让制得的原生质体一般都生活力较强,再生与分生比例较高。常用的外植体包括:种子根。子叶、下胚轴、胚细胞、花粉母细胞、悬浮培养细胞和嫩叶。对外植体的除菌要因材而异。悬浮培养细胞一般无需除菌。对较脏的外植体往往要先用肥皂水清洗再以清水洗2~3次,然后浸人 70%酒精消毒后,再放进 3%次氯酸钠处理。最后用无菌水漂洗数次,并用无菌滤纸吸干。(2)酶解 现以叶片为例说明如何制备植物原生质体。①配制酶解反应液:反应液应是一种PH值在5·5~5·8的缓冲液,内合纤维素酶0.3%~3.0%以及渗透压稳定剂、细胞膜保护剂和表面活性剂等,②酶解:除菌后的叶片 撕去下表皮 切块放人反应液 不时轻摇 (条件25℃~30℃,2~4h)反应液转绿。反应液转绿是酶解成功的一项重要指标,说明已有不少原生质体游离在反应液中。经镜检确认后应及时终止反应,避免脆弱的原生质体受到更多的损害。(3) 分离 在反应液中除了大量的原生质体外,尚有一些残留的组织块和破碎的细胞。为了取得高纯度的原生质体就必需进行原生质体的分离。可选取200~400目的不锈钢网或尼龙布j叭i过滤除渣,也可采用低速离心法或比重漂浮法直接获取原生质体。(4) 洗涤刚分离得到的原生质体往往还含有酶及其他不利于原生质体培养。再生的试剂,应以新的渗透压稳定剂或原生质体培养液离心洗涤2~4次。 (5) 鉴定 只有经过鉴定确认已获得原生质体后才能进行下阶段的细胞融合工作。由于已去除全部或大部分细胞壁,此时植物细胞呈圆形。如果把它放人低渗溶液中,则很容易胀破。也。'厂月荧光增白剂染色后置紫外显微镜下观察,残留的细胞壁呈现明显荧光。通过以上观测,基本上可判别是否原生质体及其百分中 此外,尚可借助台盼蓝活细胞染色、胞质环流观察以及测定人、作用、呼吸作用等参数定量检测原生质体的活力。4、 原生质体的融合(1)化学法诱导融合 化学法诱导融合无需贵重仪器,试剂易于得到,因此一直是细胞融合的主要方法。尤其是聚乙二醇(PEG)纳合成钙高pH诱导融合法已成为化学法诱导细胞融合的主流。以下简介此方法(在无菌条件下进行):按比例混合双亲原生质体-----滴加 PEG溶液,摇匀,静置----滴加高钙高pH值溶液,摇匀,静置-----滴加原生质体培养液洗涤数次-----离心获得原生质体细胞团一筛选、再生杂合细胞。(2)物理法诱导融合 1979年Senda等发明了微电极法诱导细胞融合。1981年Zi。。mann等提出了改进的平行电极法,现简介如下:将双亲本原生质体以适当的溶液悬浮混合后,插入微电极,接通一定的交变电场。原生质体极化后顺着电场排列成紧密接触的珍珠串状。此时瞬间施以适当强度的电脉冲,则使原生质体质膜被击穿而发生融合。电激融合不使用有毒害作用的试剂,作用条件比较温和,而且基本上是同步发生融合。只要条件摸索适当,亦可获得较高的融合率。上述操作实际上是供体与受体原生质体对等融合的方法。由于双方各具几万对基因,要筛选得到符合需要且能稳定传代的杂合细胞是相当困难的。最近,有人提出以X射线、伽玛射线。纺锤体毒素或染色体浓缩剂等对供体原生质体进行前处理。轻剂量处理可造成染色体不同程度的丢失、失活、断裂和损伤,融合后实现仅有少数染色体甚至是DNA片段的转移;致死量处理后合u可能产生没再仅体万染色体w划她旋余种。利用这种价值不对称融合方法,大大提高了融合体的生存率和可利用率。经过上述融合处理后再生的细胞株将可能出现以下几种类型.2) 亲本双方的细胞核和细胞质能融洽地合为一体,发育成为完全的杂合植株。这种例子不多。3) 融合细胞由一方细胞核与另一方细胞质构成,可能发育为核质异源的植株。亲缘关系越远的物种,某个亲本的染色体被丢失的现象就越严重。 4) 融合细胞由双方胞质及一方核或再附加少量他方染色体或DNA片段构成。④原生质体融合后两个细胞核尚未融合时就过早地被新出现的细胞壁分开。以后它们各自分生长成嵌合植株。5、 杂合体的鉴别与筛选双亲本原生质体经融合处理后产生的杂合细胞,一般要经含有渗透压稳定剂的原生质体培养基培养(液体或固体),再生出细胞壁后转移到合适的培养基中。待长出愈伤组织后按常规方法诱导其长芽、生根、成苗。在此过程中可对是否杂合细胞或植株进行鉴别与筛选。 (1) 杂合细胞的显微镜鉴别 根据以下特征可以在显微镜下直接识别杂合细胞:若一方细胞大,另一方细胞小,则大。小细胞融合的就是杂合细胞;若~方细胞基本无色,另一方为绿色,则自绿色结合的细胞是杂合细胞;如果双方原生质体在特殊显微镜下或双方经不同染料着色后可见不同的特征,则可作为识别杂合的标志;发现h述杂合细胞后可借助显微操作仪在显微镜下直接取出,移置再牛培养基培养。(2)以互补法筛选杂合细胞 显微鉴别法虽然比较可信,但实验者有时会受到仪器的限制,工作进度慢且未知其能否存活与个长 遗传互补法则可弥补以上不足。 遗传互补法的前提是获得各种遗传突变细胞株系。白化互补:不同基山叨的白化突变株出aBxAh,可互补为绿色细胞株AaBb。生长互补:甲细胞株缺外源激素A不能生长,乙细胞株需要提供外源激素B才能生长,则甲株与乙株融合,杂合细胞在不含激素A、B的选择培养基上可能生长。抗性互补筛选:假如某个细胞株具某种抗性(抗青霉素)另一个细胞株具另一种抗性(如抗卡那霉素),则它们的杂合株将可在含上述两种抗生素的培养基上再生与分裂。这种筛选方式即所谓的抗性互补筛选。代谢互补筛选:根据碘代乙酚胺能抑制细胞代谢的特点,用它处理受体原生质体,只有融合后的供体细胞质才能使细胞活性得到恢复,等等。 (3)采用细胞与分子生物学的方法鉴别杂合体 经细胞融合后长出的愈伤组织或植株,可进行染色体核型分析、染色体显带分析、同功酶分析以及更为精细的核酸分子杂交、限制性内切酶片段长度多态性(RFLP,见8.2.2.2)和随机扩增多态性DNA(RAPD)分析,以确定其是否结合了双亲本的遗传素质。(4)根据融合处理后再生长出的植株的形态特征进行鉴别质。
植物细胞原生质体制制备与融合1、原生质体常现的杂交育种由于物种间难以逾越的天然屏障而举步维艰。科学家们受细胞全能性理论及组织培养成功的启示,逐渐将眼光转向细胞融合,试图用这种崭 图3-2新的手段冲破自然界的禁钢。1937年michel率先实施植物细胞融合的试验。如何去除坚韧的细胞'接成了牛物学工作者必须解决的首要难题。196O年该领域终于出现了重大突破。由英国诺丁汉大学Cocking教授领导的小组率先利用真菌纤维素酶,成功地制备出了大量具有高度活性可再生的番茄幼根细胞原生质体,开辟了原生质体融合研究的新阶段。植物细胞原生质体是指那些已去除全部细胞壁的细胞。2、原生质体制备(1)取材与除菌 为了让制得的原生质体一般都生活力较强,再生与分生比例较高。常用的外植体包括:种子根。子叶、下胚轴、胚细胞、花粉母细胞、悬浮培养细胞和嫩叶。对外植体的除菌要因材而异。悬浮培养细胞一般无需除菌。对较脏的外植体往往要先用肥皂水清洗再以清水洗2~3次,然后浸人 70%酒精消毒后,再放进 3%次氯酸钠处理。最后用无菌水漂洗数次,并用无菌滤纸吸干。(2)酶解 现以叶片为例说明如何制备植物原生质体。①配制酶解反应液:反应液应是一种PH值在5·5~5·8的缓冲液,内合纤维素酶0.3%~3.0%以及渗透压稳定剂、细胞膜保护剂和表面活性剂等,②酶解:除菌后的叶片 撕去下表皮 切块放人反应液 不时轻摇 (条件25℃~30℃,2~4h)反应液转绿。反应液转绿是酶解成功的一项重要指标,说明已有不少原生质体游离在反应液中。经镜检确认后应及时终止反应,避免脆弱的原生质体受到更多的损害。(3) 分离 在反应液中除了大量的原生质体外,尚有一些残留的组织块和破碎的细胞。为了取得高纯度的原生质体就必需进行原生质体的分离。可选取200~400目的不锈钢网或尼龙布j叭i过滤除渣,也可采用低速离心法或比重漂浮法直接获取原生质体。(4) 洗涤刚分离得到的原生质体往往还含有酶及其他不利于原生质体培养。再生的试剂,应以新的渗透压稳定剂或原生质体培养液离心洗涤2~4次。 (5) 鉴定 只有经过鉴定确认已获得原生质体后才能进行下阶段的细胞融合工作。由于已去除全部或大部分细胞壁,此时植物细胞呈圆形。如果把它放人低渗溶液中,则很容易胀破。也。'厂月荧光增白剂染色后置紫外显微镜下观察,残留的细胞壁呈现明显荧光。通过以上观测,基本上可判别是否原生质体及其百分中 此外,尚可借助台盼蓝活细胞染色、胞质环流观察以及测定人、作用、呼吸作用等参数定量检测原生质体的活力。4、 原生质体的融合(1)化学法诱导融合 化学法诱导融合无需贵重仪器,试剂易于得到,因此一直是细胞融合的主要方法。尤其是聚乙二醇(PEG)纳合成钙高pH诱导融合法已成为化学法诱导细胞融合的主流。以下简介此方法(在无菌条件下进行):按比例混合双亲原生质体-----滴加 PEG溶液,摇匀,静置----滴加高钙高pH值溶液,摇匀,静置-----滴加原生质体培养液洗涤数次-----离心获得原生质体细胞团一筛选、再生杂合细胞。(2)物理法诱导融合 1979年Senda等发明了微电极法诱导细胞融合。1981年Zi。。mann等提出了改进的平行电极法,现简介如下:将双亲本原生质体以适当的溶液悬浮混合后,插入微电极,接通一定的交变电场。原生质体极化后顺着电场排列成紧密接触的珍珠串状。此时瞬间施以适当强度的电脉冲,则使原生质体质膜被击穿而发生融合。电激融合不使用有毒害作用的试剂,作用条件比较温和,而且基本上是同步发生融合。只要条件摸索适当,亦可获得较高的融合率。上述操作实际上是供体与受体原生质体对等融合的方法。由于双方各具几万对基因,要筛选得到符合需要且能稳定传代的杂合细胞是相当困难的。最近,有人提出以X射线、伽玛射线。纺锤体毒素或染色体浓缩剂等对供体原生质体进行前处理。轻剂量处理可造成染色体不同程度的丢失、失活、断裂和损伤,融合后实现仅有少数染色体甚至是DNA片段的转移;致死量处理后合u可能产生没再仅体万染色体w划她旋余种。利用这种价值不对称融合方法,大大提高了融合体的生存率和可利用率。经过上述融合处理后再生的细胞株将可能出现以下几种类型.2) 亲本双方的细胞核和细胞质能融洽地合为一体,发育成为完全的杂合植株。这种例子不多。3) 融合细胞由一方细胞核与另一方细胞质构成,可能发育为核质异源的植株。亲缘关系越远的物种,某个亲本的染色体被丢失的现象就越严重。 4) 融合细胞由双方胞质及一方核或再附加少量他方染色体或DNA片段构成。④原生质体融合后两个细胞核尚未融合时就过早地被新出现的细胞壁分开。以后它们各自分生长成嵌合植株。5、 杂合体的鉴别与筛选双亲本原生质体经融合处理后产生的杂合细胞,一般要经含有渗透压稳定剂的原生质体培养基培养(液体或固体),再生出细胞壁后转移到合适的培养基中。待长出愈伤组织后按常规方法诱导其长芽、生根、成苗。在此过程中可对是否杂合细胞或植株进行鉴别与筛选。 (1) 杂合细胞的显微镜鉴别 根据以下特征可以在显微镜下直接识别杂合细胞:若一方细胞大,另一方细胞小,则大。小细胞融合的就是杂合细胞;若~方细胞基本无色,另一方为绿色,则自绿色结合的细胞是杂合细胞;如果双方原生质体在特殊显微镜下或双方经不同染料着色后可见不同的特征,则可作为识别杂合的标志;发现h述杂合细胞后可借助显微操作仪在显微镜下直接取出,移置再牛培养基培养。(2)以互补法筛选杂合细胞 显微鉴别法虽然比较可信,但实验者有时会受到仪器的限制,工作进度慢且未知其能否存活与个长 遗传互补法则可弥补以上不足。 遗传互补法的前提是获得各种遗传突变细胞株系。白化互补:不同基山叨的白化突变株出aBxAh,可互补为绿色细胞株AaBb。生长互补:甲细胞株缺外源激素A不能生长,乙细胞株需要提供外源激素B才能生长,则甲株与乙株融合,杂合细胞在不含激素A、B的选择培养基上可能生长。抗性互补筛选:假如某个细胞株具某种抗性(抗青霉素)另一个细胞株具另一种抗性(如抗卡那霉素),则它们的杂合株将可在含上述两种抗生素的培养基上再生与分裂。这种筛选方式即所谓的抗性互补筛选。代谢互补筛选:根据碘代乙酚胺能抑制细胞代谢的特点,用它处理受体原生质体,只有融合后的供体细胞质才能使细胞活性得到恢复,等等。 (3)采用细胞与分子生物学的方法鉴别杂合体 经细胞融合后长出的愈伤组织或植株,可进行染色体核型分析、染色体显带分析、同功酶分析以及更为精细的核酸分子杂交、限制性内切酶片段长度多态性(RFLP,见8.2.2.2)和随机扩增多态性DNA(RAPD)分析,以确定其是否结合了双亲本的遗传素质。(4)根据融合处理后再生长出的植株的形态特征进行鉴别质。
目前我们采用过柱子的方法纯化脂质体,效率不高,并且纯化产物纯度不高,想咨询一下是否可以采用制备[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]来对产物进行纯化。
请问有没有人测量脂质体的膜厚啊? 我想测量脂质体的膜厚,不知道有没有人测量过这个?我想测几个样品,有没有人知道哪里有这方面的经验?
脂质体包覆的COX-2抑制剂纳米颗粒的靶向化疗脂质体确 (liposome) 是一种磷脂和胆固醇组成的双层膜球形囊泡. 脂质体可以用天然的磷脂和磷脂乙醇胺 (phosphatidylethanolamine, 源于鸡蛋) 或纯表面活性剂, 如 DOPE (dioleolylphosphatidylethanolamine) . 脂质体通常含有一个核心的水溶液 (但这并非脂质体定义). 不含有水溶性物质的脂质双膜体被称为胶束(miscell).脂质体 (Liposome) 是由两个希腊词'脂'和 '体' 的意思构成. 脂质体本身并不表明任何大小之特点, 因此不同于纳米体 (nanosome). 1961年英国剑桥大学巴巴拉汉姆学院血液学家Bangham先生首次描述脂质体. Bangham先生与其同事Horne为了测试研究所新到的电子显微镜, 加负染色剂(三氯醋酸,TCA)于干磷脂中, 随后他们观察到一种类脂双层结构, 酷似质膜, 这就是首次显微镜照片展示的细胞膜实质性证据. 由于其独特的性能脂质体可用于药物载体, 这是由于亲水溶解溶质不能轻易通过脂质双膜, 而疏水性化学物质,可以溶解到脂质体膜内, 所以脂质体既可携带疏水性分子, 也可亲水性分子. 脂质体双层可以与其他细胞膜双层融合, 从而传递携带内含物. 用脂质体来投递DNA (lipofection) 比 单独用DNA感染细胞要有效的多. 低(或高) pH脂质体中的水溶解药物都带有电荷 (即pH值是药物的等电点范围以外) . 随着pH值自然抵销 (质子能通过膜), 因药物能自由穿过细胞膜, 中和后的脂质体药物也会自由扩散, . 这一投递是借脂质体双层膜与细胞接触来扩散脂质体药物, 而不是直接的融合. 所以这种脂质体药物的生产与使用受到时间上的限制.另一种脂质体药物投递的方式是借巨吞噬细胞作用. 一定大小范围内的脂质体可被人体中巨噬细胞吞噬. 脂质体药物在脂质体被巨噬细胞的胞溶体溶解后释放出来.加上陪体 的脂质体更易激活这种内吞噬作用.另一脂质体的好处是它的癌细胞靶向能力, 所有健康人的血管内皮都是由内皮细胞所包裹, 严密阻止任何大颗粒从血液中漏出. 但肿瘤血管则不具有相同水平的密封效果,通常小于400nm的脂质体可可迅速从患者的血液进入肿瘤. 抗癌药物如阿霉素(Doxorubicin, Doxil) 和柔红霉素 (Daunorubicin, Daunoxome ) 就是利用脂质体给药系统. 脂质体可用磷脂水经超声波而制成. 低剪切率超声波制成像洋葱多层状脂质体, 如持续用高剪切超声波则倾向于形成较小的单层脂质体 (unilamellar). 超声波法被普遍认为是"毛, 粗"的制备方法, 较新的方法, 如挤出法(extrusion)制成的脂质体药物可供人类使用.当前研究已经能够使脂质体能躲避人体的免疫系统, 成为"隐形脂质体", 即脂质体外挂上惰性聚乙二醇( PEG ), PEG脂质体延长循环中的药物运送. 但是 目前的困难是PEG涂的厚度. 太厚则阻止脂质体与细胞的接合. 为了特异性接合脂质体可挂上单克隆抗体, 或特异性抗原. 这样脂质体药物只送到病变组织.

作者:http://vpn.library.shmtu.edu.cn:2308/Images/head_pic.gif宋笑丹 http://vpn.library.shmtu.edu.cn:2308/Images/head_pic.gif刘红梅 http://vpn.library.shmtu.edu.cn:2308/Images/head_pic.gif魏华 http://vpn.library.shmtu.edu.cn:2308/Images/head_pic.gif董迪 http://vpn.library.shmtu.edu.cn:2308/Images/head_pic.gif吴琳华 Author:SONG Xiao-dan LIU Hong-mei WEI Hua DONG Di WU Lin-hua 作者单位:哈尔滨医科大学附属第二医院药学部,黑龙江省高校重点实验室,哈尔滨,摘要: 目的 考察β-榄香烯脂质体在大鼠体内的组织分布.方法 建立了大鼠体内β-榄香烯测定的HPLC.色谱条件为:Diamonsil C18色谱柱(4.6 mm×250 mm,5μm);流动相为甲醇-乙腈-水(40:57:3);检测波长:210 nm;柱温:30℃.并测定大鼠尾静脉注射β-榄香烯脂质体和榄香烯注射液后血浆及组织中的药物浓度.结果 此色谱条件下血浆与组织的标准曲线、精密度等实验结果表明,该方法适于分析生物样品中β-榄香烯含量.与榄香烯注射液相比,β-榄香烯脂质体在大鼠体内的分布特性有不同程度的改变,其中β-榄香烯脂质体在肝、脾、肾组织中分布相对较多.结论 β-榄香烯脂质体及榄香烯注射液在大鼠的心、脾、肾组织中分布具有显著性差异http://ng1.17img.cn/bbsfiles/images/2012/08/201208271803_386611_2379123_3.jpg
有个问题,脂质体的不溶性微粒检测,是跟药典里面关于脂质体的不溶性微粒检测方法一样么?有没有什么文件可以看啊,哪位大神知道,求指导
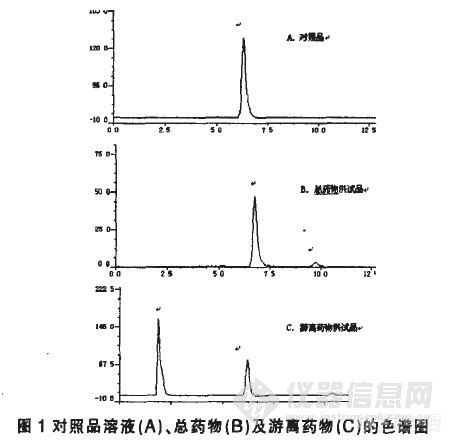
作者:李文秀;邓英杰;魏伟;高晓非;曹金娜(沈阳药科大学药学院 沈阳药科大学药学院 沈阳药科大学药学院 沈阳药科大学药学院 沈阳药科大学药学院)摘要:目的:建立灯盏花素前体脂质体胶囊的突释考察方法。方法:采用透析-高效液相色谱法(HPLC),水化前体脂质体后,用透析袋分析游离药物和脂质体,并用HPLC法测定含量。采用Diamonsil ODS C18色谱柱(4.6mm×250mm,5μm),流动相为甲醇-乙腈-40mmol/L KH2PO4(磷酸调pH至2.5)(18∶12∶70);检测波长335nm;流速1.0ml/min;柱温35℃。结果:游离药物在透析膜两侧均匀分布,而脂质体被截留于透析袋中。含量测定方法平均加样回收率为103.32%,RSD为1.12%(n=9)。结论:本法操作简便、准确,可用于灯盏花素前体脂质体胶囊突释的评价。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208211652_385078_1609970_3.jpg
如题,想问下,多相脂质体需要分析什么参数?今天被人问到,手边没有药典,不知论坛有没有做,帮忙看看药典有没有这个规定啊。看看附录里面。
如何用浊度法检测脂质体的稳定性。其中应用紫外可见分光光度计。浊度与吸光度之间有什么关系?
测脂质体内相pH用什么仪器呢
称量固体标准品配制标准曲线溶液,使用注射液脂质体来配制质控样品,怎么比较都是标准曲线高于质控,已经做过溶液准确度考察。两个处理方式不同只在于标准曲线是直接用溶液,后面再加基质,而质控是直接配制在基质中。已经做过脂质体破碎的考察,增加涡旋时间或者增加有机试剂都没有变化。前处理方式也比较过,没有变化。现在不知道原因出在哪了?
要了解脂质体毛细管电泳(LCE),首先得给大家解释一个概念:生物膜(Biomembrane)。生物膜是指组成生物体细胞各个“构件”的膜,细胞内的细胞膜、核膜以及内质网、高尔基体、线粒体等细胞器,就是这台“机器”中一些功能相关的“部件”,它们都由膜构成,这些膜的化学组成相似,基本结构大致相同,统称为生物膜。生物膜色谱(Biomembrane Chromatography)是一种新型液相色谱模式,它以天然或人工模拟生物膜为固定相,主要用来研究溶质分子与生物膜间的相互作用。目前,最常用的生物膜色谱固定相是固定化脂质体,因为它能更好的模拟生物膜的脂双层结构,并具备生物膜的流动性特征。这种人工模拟的生物膜体系不仅可以精确地模拟生物膜的化学环境,而且其物理性能也可以通过调节温度,pH、离子强度等得到有效控制。LCE就是利用脂质体作为假固定相的毛细管电泳,主要用于分离蛋白质、手性分子及模拟药物-生物膜相互作用的新型毛细管电泳。与生物膜色谱相比,LCE方法简单,可操作性强,成本低廉,尤其是测定药物的Klw 准确、重现性好,具有更好的发展前景。目前,LCE 无论在理论还是技术方面都还不太成熟,应用范围也较为有限,因而其发展空间还很广阔。
眼部疾病的常用治疗方式是局部给以药物溶液(例如滴眼液),这些传统剂型占据市售制剂的90%左右。然而,眼部的生理屏障以及候选药物的低溶解性为眼部给药系统的发展带来许多难题。 最近,各种旨在提高难溶性药物生物利用度的眼部给药方式大量出现。中科院上海药物所甘勇课题组专题综述了这些眼部给药方式,包括水凝胶、聚合物胶束、纳米混悬液和脂质纳米载体等。同时,深入阐述了脂质纳米载体,包括乳液、脂质体、立方液晶、囊泡等,为眼部药物传递提供许多优势,比如提高难溶性药物的生物利用度、靶向给药、控制药物释放以及降低全身副作用等。(相关工作主要由甘莉、王静完成:Drug Discovery Today, in press.) 依据脂质体纳米粒作为眼用载体的独特优势,上海药物所甘勇课题组设计研究了一种新型双阳离子型核壳脂质体纳米粒(DLCS-NP)。采用薄膜分散水化-挤膜法,直接将旋干的脂质膜与分散的壳聚糖纳米粒(CS-NP)混悬液水化,自组装形成核壳结构的阴离子脂质体纳米粒(LCS-NP),随后利用阳离子N--N,N,N-三甲酰丙烷甲基硫酸盐与磷脂双分子层的亲和作用,在LCS-NP表面形成正电荷磷脂修饰层,形成DLCS-NP。该具有独特双阳离子型核壳脂质体纳米粒,能够显著延长载体角膜滞留时间,提高细胞摄取量,并具有一定的溶酶体逃逸能力,取得了理想的体内外眼表基因转染效果,为眼表疾病的基因治疗开辟了新途径。(相关工作主要由蒋敏、甘莉完成:Biomaterials, 2012, 33: 7621-7630.) 该项研究取得了上海市自然科学基金 (No.11ZR1444700)、国家自然科学基金资助项目(No.81102387)、国家科技重大专项“重大新药创制” (No.2009ZX09301-01) 和国家重点基础研究发展计划 (No.2009CB930300)的资助。 全文链接 1 2 http://www.cas.cn/ky/kyjz/201211/W020121127573032605614.jpgDLCS-NP的细胞摄取及摄取机制示意图
脂质体被用作病毒体的人工模型,能够对关键的膜结合药物目标进行系统梳理。隆德大学(瑞典)质子通道研究小组的副教授Sindra Peterson Årsköld博士及其同事的工作重点从事病毒蛋白质和抗病毒剂的脂质体研究。Peterson Årsköld博士表示,如果没有马尔文Zetasizer Nano ZS纳米颗粒分析系统快速、可靠而且高资源利用率的测定性能,在各种样品条件下精确的例行样品质量控制就不可能实现。作为一名蛋白质科学家,Peterson Årsköld博士解释了样品分析成本为何对其工作如此至关重要的原因:“水中超声降解磷脂产生的脂质体被用于获取极其详细的定量生物物理数据。因此极其重要的是,每批脂质体需要在窄分布粒径和单层方面具有相同的高品质,而且其形态也需要能够复制并始终如一。在脂质体生产方法的开发以及对脂质体进行优化以获得新型蛋白质体系的过程中,对这些参数的监测也很关键。举例来说,一些条件会形成多层脂质体,像洋葱一样有许多薄层。这意味着,我们每次生产一种新样品时,我们都必须进行质量检查以确保过程的一致性。”“虽然电子显微镜检查(EM)能为我们提供更加详细的数据,但获得图像要花一整天。因此使用EM进行常规样品检测的成本很高。Zetasizer Nano ZS应用动态光散射原理(DLS),既没有破坏性也很快速。"它能够在几分钟内对我们的样品进行检测,” Peterson Årsköld博士说。“实际上,这是一种有用而且易于使用的系统,自从我购入该仪器以来,我们系的蛋白质化学家们每天都使用它,而且现在再也不愿意在没有它的情况下工作了!”作为隆德大学生物化学及结构生物系的一部分,Peterson Årsköld博士 以及质子通道研究小组一直在研究甲型流感病毒产生的M2蛋白质,一种小型单跨横跨膜(TM)蛋白质的性状。Peterson Årsköld博士共同署名,发布在国家科学院会议论文集(PNAS)上的论文指出使多个质子能够侵入甲型流感病毒,引发宿主细胞感染,而不形成较大电位的神秘过程。结果证明M2蛋白质与pH值非常复杂、功能调谐关系,能够为成功的抗病毒药物的开发提供更好的机会。
【作者】 张晓云; 倪京满; 乔华; 孟庆刚; 王荷;【机构】 兰州大学药学院药剂教研室; 兰州大学第一医院药剂科; 兰州大学药学院药剂教研室 兰州730000; 兰州730000; 兰州730000;【摘要】 采用RP-HPLC法测定鬼臼毒素纳米脂质体的重要质控指标包封率。流动相:甲醇-水=60∶40;色谱柱:D ikm a公司的D iamonsil C18(150×4.6 mm,5μm);紫外检测波长:290 nm;流速:1 m l/m in。回收率为101.1%,RSD=1.94%(n=3)。本测定方法简便、快速,准确度高,可用于鬼臼毒素纳米脂质体的含量测定。 更多还原【关键词】 高效液相色谱; 鬼臼毒素; 纳米脂质体; 包封率;
【序号】:1【作者】:[url=http://yuanjian.cnki.com.cn/Search/Result?author=%E5%BC%A0%E5%B0%8F%E6%B4%AA]张小洪[/url] 【题名】:[b]脂质体、分散体和肠溶包衣替米考星体外释放和抑菌研究[/b]【期刊】:重庆大学硕士论文【年、卷、期、起止页码】: [color=#333333]2014[/color]【全文链接】:http://cdmd.cnki.com.cn/Article/CDMD-10611-1014043590.htm
小弟以前在学校图书馆看到一本 有机中间体的制备与合成手册 是本红色封面的,现在没看到外面有卖的,不知道哪为GGJJ有没有电子版的.如果能传上来的话.不胜感激!
[size=4][/size]如题,请高手多多指教。

色谱法同时分析磷脂酰胆碱,溶血磷脂酰胆碱和游离脂肪酸 磷脂容易被氧化和水解从而降解(如下图),这就限制了有磷脂的药物制剂(脂质体、乳剂)的稳定性及保质期.http://ng1.17img.cn/bbsfiles/images/2014/11/201411281025_525018_2204138_3.jpg 溶血磷脂和脂肪酸的产生量是判断药物制剂适宜性的关键参数,如随着脂质水解程度变化脂质体分子组成由层状变为胶束就会伴随着药物释放速度的改变。有报道称大量LPC的形成会导致油滴变大导致磷脂与肠胃液稳定相的聚合和破裂,从而导致毒副作用。 美国FDA要求制药企业对于脂质体药物建立适当的储存条件,并在进行稳定性研究时对脂质体药物进行脂质成分分析。这就要求合适的方法对不同化合物的准确定性及定量分析。由于分子中缺乏足够的发色团,以至于紫外和荧光检测不适于对于脂质体的直接分析。蒸发光散射检测器(ELSD)并不需要衍生化,可作为磷脂检测的快速灵敏的手段。蒸发光散射通过测定溶剂蒸发后被检测物散发光的强度进行分析。该方法允许梯度洗脱并对流速不敏感,且相对于LC-MS更方便和便宜。 材料和方法:L-α磷脂酰胆碱、L-α溶血磷脂酰胆碱、亚油酸、油酸、棕榈酸、硬脂酸、甲醇(色谱纯)、氯仿(色谱纯)、氢氧化铵(分析纯)、去离子水。旋转蒸发仪、超声仪、沃特斯2695配低温政法光检测器、Allsphere硅胶色谱柱(150mm×4.6×5um)、Millennium32色谱工作软件。 磷脂酰胆碱脂质体悬浮液通过蒸发-水化法制备,称取0.224g PC溶解于50ml氯仿中,转移至250ml圆底烧瓶中,使用氮气流蒸发氯仿而形成薄的脂质膜,最后通过旋转蒸发仪除去痕量的氯仿,脂质膜用50ml的0.9%NaCl溶液于40℃进行水合,将脂质体浓缩至4.48mg/ml,得到的多层囊泡悬浮液经超声30分钟以获得单层脂质体,脂质体用0.1 N NaOH 调节PH在9-10之间。121℃高压灭菌15分钟。室温保存备用。 标准和样品溶液的制备: 以氯仿:甲醇(50:50%,体积/体积)为溶剂分别制备PC,LPC和亚油酸含量为5mg / mL的储备液,冷冻避光保存备用。 标准曲线系列浓度配制范围PC为82–816 μg/mL,LPC为30–250 μg/mL,亚油酸为55-290μg/mL。 混合标准为同浓度的PC、LPC亚油酸酸,油酸,硬脂酸,和棕榈酸。 FFA的样品是由相等浓度的油酸,亚油酸、硬脂酸和棕榈酸制备。 样品溶液是通过将0.5毫升脂质体加入氯仿:水(50:50%,体积/体积)的溶剂体系。 液相分析:梯度洗脱情况如下http://ng1.17img.cn/bbsfiles/images/2014/11/201411281026_525019_2204138_3.jpgA 氯仿B 氯仿:甲醇(70:30%,体积/体积)C 氯仿:甲醇:水:氢氧化铵(45:45:9.5:0.5%,体积/体积/体积/体积)流速:1.0ml/min 柱温 28度进样量20ul.ELSD条件包括:漂移管温度的40℃,增益6,雾化气体压力3.2bar. 结果与讨论: 标准的色谱图:http://ng1.17img.cn/bbsfiles/images/2014/11/201411281027_525020_2204138_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/11/201411281027_525021_2204138_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/11/201411281027_525022_2204138_3.jpg 由标准色谱图得知混合游离脂肪酸的出峰时间在6.7min,PC出峰时间为12.2min,LPC出峰时间为14.7min. 脂质体HPLC-ELSD色谱图:[a
[font=宋体]在生物医学领域中,[url=https://cn.sinobiological.com/resource/antibody-technical/pab-production][b]多克隆抗体制备[/b][/url]是一个重要的技术,广泛应用于疾病诊断、治疗和基础研究中。然而,许多初学者对于这一技术可能存在一些疑问。本文将针对多克隆抗体制备过程中的常见问题,进行详细的解答和解析,帮助读者更好地理解和应用这一技术。[/font][font=宋体] [/font][font=宋体][font=Calibri]1[/font][font=宋体]、免疫宿主该如何选择[/font][font=Calibri]?[/font][/font][font=宋体] [/font][font=宋体]选择宿主时,一般要考虑两个问题:[/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]1[/font][font=宋体])免疫效果能否保证。特别是对于蛋白抗原的情况,为了保证免疫成功,就要求宿主与抗原来源物种之间有较远的亲缘关系,如果不太能确定亲缘关系的远近,建议把抗原的序列与被免疫的宿主相应的蛋白的序列进行一个对比,优先选择同源性较低的物种进行免疫。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri](2)[/font][font=宋体]抗血清产量的问题。根据实验目的不同,抗血清的用量也有所不同。如果后续是做[/font][font=Calibri]Western Blot[/font][font=宋体],那么只需要一点点血清就够了,这个时候就可以选用小[/font][font=Calibri]Mouse[/font][font=宋体]这样的小宿主作为免疫宿主,而如果想生产二抗作为商业使用,则可选用羊、驴、马这样的大型宿主,大型宿主还可以进行多次放血,以提高宿主的利用率。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2[/font][font=宋体]、如何选择抗原?[/font][/font][font=宋体] [/font][font=宋体][font=Calibri](1)[/font][font=宋体]降解的蛋白抗原利于制备用于筛选细菌表达[/font][font=Calibri]cDNA[/font][font=宋体]文库或免疫沉淀[/font][/font][font=宋体] [/font][font=宋体][font=Calibri](2)[/font][font=宋体]用于筛选真核细胞转染系统表达的[/font][font=Calibri]cDNA[/font][font=宋体]文库或免疫沉淀,最好选用自然的蛋白抗原。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri](3)[/font][font=宋体]如果制备抗独特型抗体,所用抗原可以是可溶性[/font][font=Calibri]Ig[/font][font=宋体]分子,或者是完整的细胞,也可以是基因工程表达产品独特型决定簇、人工合成多肽及抗原化抗体等。[/font][/font][font=宋体] [/font][font=宋体]目前,以各类病原生物活体感染宿主而获得多克隆抗体(抗血清)作为检测抗体,仍是常用方法。[/font][font=宋体] [/font][font=宋体][font=Calibri]3[/font][font=宋体]、多克隆抗体有哪些优势?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]1[/font][font=宋体])成本低廉,技术门槛低,制备周期短。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]2[/font][font=宋体])能识别一个抗原上的多个表位,可在[/font][font=Calibri]IP[/font][font=宋体]等实验中获得更加理想的结果。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]3[/font][font=宋体])多抗因为靶蛋白可在多个表位上结合不止一个抗体分子,有助于放大低表达水平的靶蛋白信号。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]4[/font][font=宋体])能识别出与免疫原蛋白具有高同源性的蛋白,或者从非免疫原物种的组织样品中筛选靶蛋白,例如当未测试物种中的抗原性质未知时,有时会使用多克隆抗体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]5[/font][font=宋体])可识别多个结构域,即使原始抗原的一些空间结构或者序列发生小变化或者部分抗原决定簇变化,仍可以识别抗原,因此有更大的适应性[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4[/font][font=宋体]、多抗用来做[/font][font=Calibri]Western Blot[/font][font=宋体]检测为何有杂带出现?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]1[/font][font=宋体])你可能是用[/font][font=Calibri]ProteinA/G[/font][font=宋体]来进行抗体纯化,这种纯化方式得到的多抗掺杂有宿主本身对其自身抗原产生的抗体,这些抗体在检测中会识别样本中的蛋白而出现杂带,建议采用抗原亲和纯化来避免杂带的产生。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]2[/font][font=宋体])天然蛋白存在复杂的翻译后修饰。可以通过信息学分析来解释。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]3[/font][font=宋体])翻译后蛋白前体经切割可能会使部分蛋白分子量偏小,而天然组织中同时存在蛋白前体和切割加工后的蛋白,二者序列有相同部分,可能会产生杂带。最好是通过查阅与目的蛋白相关文献进行了解。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]4[/font][font=宋体])当目的蛋白有同源家族蛋白时,蛋白异构体的存在可能会使分子量偏离预测分子量,因为天然样本中由同一个[/font][font=Calibri]mRNA[/font][font=宋体]不同的剪接方式进行翻译形成的蛋白产物也会有相同的抗原表位,同时被抗体识别时会产生杂带。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]([/font][font=Calibri]5[/font][font=宋体])强烈的蛋白间相互作用在还原条件下也有可能不解聚导致条带偏大。如二聚体或三聚体,这些多聚体的形式通常会抵制[/font][font=Calibri]WB[/font][font=宋体]时所做的还原条件,因此造成检测的条带偏大。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]5[/font][font=宋体]、多克隆抗体如何保存及运输?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]我们的抗体是添加[/font][font=Calibri]5%[/font][font=宋体]甘油,免疫前血清和抗血清已添加[/font][font=Calibri]0.02%[/font][font=宋体]防腐剂,若客户有其他要求,会提前告知生产;抗体会超低温包装运输寄送, 收到抗体请尽快检测,建议分装成小包装(分装为每次使用量)后保存于[/font][font=Calibri]-80[/font][font=宋体]摄氏度冰箱,并避免反复冻融, 保存时间若超过[/font][font=Calibri]1[/font][font=宋体]年,使用前请先电泳检测蛋白是否降解。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]6[/font][font=宋体]、制备的多克隆抗体是否可以保证后续[/font][font=Calibri]WB[/font][font=宋体]实验?[/font][/font][font=宋体] [/font][font=宋体][font=宋体]制备抗体的抗原是原核重组表达的蛋白,与后续用于[/font][font=Calibri]WB[/font][font=宋体]的天然蛋白样品是有差异的,无法保证构象及活性与天然蛋白一致,所以不能保证后续应用于天然蛋白的[/font][font=Calibri]WB[/font][font=宋体],但可以保证制备出的抗体与抗原蛋白是[/font][font=Calibri]WB[/font][font=宋体]呈阳性的。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/polyclonal-antibody-production-services][b]多克隆抗体制备服务[/b][/url],最快仅需[/font][font=Calibri]45[/font][font=宋体]天交付抗血清或纯化抗体。您只需提供抗原的基因序列,我们就可以为您制备高亲和力的多克隆抗体,以满足您在研究或诊断方面的应用。[/font][/font]
那位有[医药中间体制备方法与加工技术及质量检测标准实用手册]第三篇、第四篇全部内容文件有:编委会、目 录、第一篇、第二篇、第三篇、第四篇、第五篇、第六篇、第七篇、第八篇、第九篇、第十篇、附 录。其它我都有了,就缺这两篇。
想请教各位制备脂质体过程中,磷脂双分子层形成的原理,教科书上没有讲清楚,在此请教各位!
脂质体化妆品及其应用LIPOSOME COSMETICS AND ITS APPLICATION2000年04期张根旺 脂质体是一种生物载体,加载活性成分的脂质体对治疗疾病和皮肤护理非常有效.本文介绍了脂质体的结构、定义、分类、制备方法及其在化妆品中的应用.Liposomes are a kind of biological carrier.Lipsomes loaded active materials are very effective in treatming disease and skin care.The structure,definition,catalogs and preparation of liposomes and its application in cosmetics are introduced in this paper. 关键词: 脂质体 , 制备 , 应用 | 全部关键词
[font=宋体][font=宋体]单克隆抗体([/font][font=Calibri]Monoclonal antibodies[/font][font=宋体],[/font][font=Calibri]mAb[/font][font=宋体])是由[/font][font=Calibri]B[/font][font=宋体]细胞产生,并能特异性靶向抗原的免疫球蛋白。单克隆抗体不仅是生物化学、分子生物学和医学研究中必不可少的工具,其在临床治疗上的应用也以革命性的速度改进了多种疑难杂症的治疗方法。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]1975[/font][font=宋体]年[/font][font=Calibri]Khler[/font][font=宋体]和[/font][font=Calibri]Milstein[/font][font=宋体]提出的杂交瘤技术([/font][font=Calibri]Hybridoma technology[/font][font=宋体]),使得大量获得单克隆抗体成为可能,为基础研究及其临床应用提供了无限潜力。其他科学和技术进步也促进了单克隆抗体的发展、丰富了单克隆抗体的制备方法。 经过近[/font][font=Calibri]50[/font][font=宋体]年的发展,单克隆抗体制备方法不再局限于免疫小鼠的淋巴细胞术,噬菌体展示技术([/font][font=Calibri]Phage display[/font][font=宋体])、人源抗体转基因小鼠([/font][font=Calibri]Human antibody-producing mice[/font][font=宋体])和单[/font][font=Calibri]B[/font][font=宋体]细胞抗体技术([/font][font=Calibri]Single B cell antibody technology[/font][font=宋体])也都陆续登上舞台。这些方法虽然有各自的局限性,但都已广泛应用于单克隆抗体筛选。同时,这些技术都不完全是独立存在的,如果能充分利用各技术的优点,采用灵活的方法将各技术优化组合就能更加高效、快速地进行抗体开发。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体]一、杂交瘤技术[/font][font=宋体] [/font][font=宋体][font=宋体]杂交瘤技术是一种将[/font][font=Calibri]B[/font][font=宋体]细胞与骨髓瘤细胞融合生产小鼠单克隆抗体的传统方法,是目前应用最广泛的单克隆生产技术。在这种技术中,首先收集免疫小鼠的[/font][font=Calibri]B[/font][font=宋体]淋巴细胞,并将其与[/font][font=Calibri]BALB/c[/font][font=宋体]小鼠骨髓瘤细胞融合,从而形成永生化的杂交瘤细胞。然后筛选杂交瘤细胞,鉴定出能生产特异性抗体的单克隆细胞株。十几年后,[/font][font=Calibri]1988[/font][font=宋体]年,兔单克隆抗体制备方法首次被《[/font][font=Calibri]Science[/font][font=宋体]》杂志报道 [/font][font=Calibri][1][/font][font=宋体]。该研究使用小鼠[/font][font=Calibri]-[/font][font=宋体]兔异种杂交瘤方法生产兔单克隆抗体,但鼠[/font][font=Calibri]-[/font][font=宋体]兔异种杂交瘤细胞分泌抗体的效率较低、不稳定,且无法长时间分泌抗体。时间进展到[/font][font=Calibri]90[/font][font=宋体]年代中期,[/font][font=Calibri]1995[/font][font=宋体]年,《[/font][font=Calibri]PNAS[/font][font=宋体]》报道了能稳定生产兔单抗的兔[/font][font=Calibri]-[/font][font=宋体]兔杂交瘤细胞。但兔杂交瘤细胞也被证明不如常规鼠杂交瘤细胞稳定,这大大阻碍了其实验室水平的广泛使用。并且,由于融合和转化效率低下,使用兔杂交瘤细胞生产单克隆抗体在应用推广中受到了极大的限制。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]经过多年发展及应用,杂交瘤技术作为一种成熟的产生鼠单克隆抗体的方法已被广泛应用于多种抗体的生产。然而,由于缺乏合适的骨髓瘤融合伴侣,杂交瘤技术一直局限于免疫啮齿动物。[/font][font=Calibri]20[/font][font=宋体]世纪[/font][font=Calibri]80[/font][font=宋体]年代,《[/font][font=Calibri]PNAS[/font][font=宋体]》报道了一种应用人杂交瘤技术生产治疗用抗体的文章 [/font][font=Calibri][3][/font][font=宋体]。利用该方法可以在无额外修饰的情况下产生天然的人源抗体,并用于临床治疗。随着融合伴侣和电融合技术的发展,人杂交瘤细胞融合成功率逐步增加,这将在未来促进治疗性抗体的开发。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体]二、噬菌体展示技术[/font][font=宋体] [/font][font=宋体][font=Calibri]1990[/font][font=宋体]年开始,噬菌体展示技术被视为一种新的产生单克隆抗体的方法。这种方法是从淋巴细胞中收获抗体可变区基因([/font][font=Calibri]V gene[/font][font=宋体])全集,克隆[/font][font=Calibri]VHs[/font][font=宋体]和[/font][font=Calibri]VLs[/font][font=宋体]的组合并与外壳蛋白融合后表达于丝状噬菌体表面,然后筛选表达特异性抗体的噬菌体。与受限于啮齿动物的杂交瘤技术相比,噬菌体展示技术已经成功用于任何已知免疫球蛋白基因的物种中筛选和分离单克隆抗体。[/font][font=Calibri]2000[/font][font=宋体]年,[/font][font=Calibri]Rader[/font][font=宋体]等人首次介绍了应用噬菌体展示技术生产兔单克隆抗体的全过程。在这篇文章中,[/font][font=Calibri]Rader[/font][font=宋体]等人用噬菌体展示技术筛选和人源化的人[/font][font=Calibri]A33[/font][font=宋体]兔抗体,不仅对人[/font][font=Calibri]A33[/font][font=宋体]抗原有高特异性,且保留高亲和力。目前,噬菌体展示技术因为其高效、简便及体外控制在原核或真核系统中原则参数的能力正逐步成为生产治疗用抗体的重要技术平台。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]随着我们对抗体结构、功能和序列多样性研究的不断深入,除了原有的抗体库外,一种新的合成抗体库技术也在不断发展。例如,[/font][font=Calibri]HuCAL&Ylanthia[/font][font=宋体]文库中,为了使筛选出的人源抗体能更好的进行分子识别,将精确设计的序列插入抗原结合位点,并优化设计多种可变重链、轻链框架区域 [/font][font=Calibri][7-10][/font][font=宋体]。随着文库设计和筛选方法的不断进步,合成抗体文库将成为快速生产具有高特异性和高亲和力单克隆抗体不可或缺的工具。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体]三、人源抗体转基因小鼠[/font][font=宋体] [/font][font=宋体][font=Calibri]1985[/font][font=宋体]年,[/font][font=Calibri]Alt[/font][font=宋体]等人首次提出将人抗体基因引入小鼠种系并使用转基因小鼠中产生人抗体的想法 [/font][font=Calibri][11,12][/font][font=宋体]。随着基因编辑技术的进步,使用人源抗体转基因小鼠生产人源化抗体已不再是天方夜谭。与其他技术相比,使用人源抗体转基因小鼠有许多优势,如无需人源化、具有更多的生物多样性,且由于体内成熟具有天然的亲和力。但是,人免疫球蛋白体量庞大对转基因小鼠抗体生产是一个巨大的挑战。为了克服这些困难,研究人员们通过使用不同策略已成功地获得转基因动物表达的人源抗体库,如全人源抗体小鼠和嵌合人源抗体小鼠等。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]四、单[/font][font=Calibri]B[/font][font=宋体]细胞抗体技术[/font][/font][font=宋体] [/font][font=宋体][font=宋体]虽然杂交瘤技术和噬菌体展示技术已经在单克隆抗体生产中广泛应用,但它们依然存在较难克服的缺点制约着抗体生产过程。近些年,为了克服杂交瘤技术细胞融合效率低,噬菌体展示技术导致重链、轻链的天然同源配对丢失等问题,单[/font][font=Calibri]B[/font][font=宋体]细胞抗体技术正被逐步开发和应用。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]简单来说,单[/font][font=Calibri]B[/font][font=宋体]细胞抗体技术包含以下几个步骤:[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]a.[/font][font=宋体]从外周血或免疫器官中初步提取淋巴细胞;[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]b.[/font][font=宋体]使用磁性活化细胞分选([/font][font=Calibri]MACS[/font][font=宋体])或荧光活化细胞分选([/font][font=Calibri]FACS[/font][font=宋体])技术鉴定和分离出特定的[/font][font=Calibri]B[/font][font=宋体]细胞;[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]c.[/font][font=宋体]将分离出的[/font][font=Calibri]B[/font][font=宋体]细胞进行单细胞培养;[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]d.[/font][font=宋体]使用逆转录聚合酶链式反应([/font][font=Calibri]RT-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url][/font][font=宋体])和抗体特异性引物鉴定单[/font][font=Calibri]B[/font][font=宋体]细胞分泌抗体的特异性;[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]e.[/font][font=宋体]扩增特异抗体基因;[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]f.[/font][font=宋体]将抗体基因克隆到表达载体中,并在细菌或细胞系统中表达;[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]g.[/font][font=宋体]纯化表达产生的抗体,并用[/font][font=Calibri]ELISA[/font][font=宋体]等方法进行评估。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]单[/font][font=Calibri]B[/font][font=宋体]细胞抗体技术现在已广泛用于人和小鼠单克隆抗体生产,如一些治疗性中和单抗,可用于治疗多种疾病,包括癌症、自身免疫性疾病和传染性疾病亡[/font][/font][font=宋体] [/font][font=宋体][font=宋体]总结[/font][font=Calibri]4[/font][font=宋体]种方式制备单克隆抗体的优缺点[/font][/font][font=宋体] [/font][font=宋体][url=https://cn.sinobiological.com/resource/antibody-technical/hybridoma-technology][b]杂交瘤技术[/b][/url]:[/font][font=宋体]优势:技术成熟、研发成本低[/font][font=宋体]劣势:周期长、融合率低、需要进行人源化[/font][font=宋体] [/font][font=宋体]人源抗体转基因小鼠:[/font][font=宋体]优势:[/font][font=宋体]①可用杂交瘤技术获得人源抗体[/font][font=宋体]②良好的免疫原性[/font][font=宋体]③亲和力高[/font][font=宋体] [/font][font=宋体]劣势:[/font][font=宋体]①存在免疫耐受[/font][font=宋体]②依然有鼠抗产生[/font][font=宋体]③难以免疫毒性抗原[/font][font=宋体] [/font][font=宋体] [/font][font=宋体][url=https://cn.sinobiological.com/resource/antibody-technical/phage-display-antibody][b]噬菌体展示技术[/b][/url]:[/font][font=宋体]优势:[/font][font=宋体]①基因来源灵活[/font][font=宋体]②随机库可以避免免疫耐受[/font][font=宋体]③可以灵活,特异得调整设计方案[/font][font=宋体]④可长时间保存[/font][font=宋体] [/font][font=宋体]劣势:[/font][font=宋体]①重链轻链非天然配对[/font][font=宋体]②展示效率具有偏好性[/font][font=宋体]③需要再次进行功能验证[/font][font=宋体] [/font][font=宋体][font=宋体]单[/font][font=Calibri]B[/font][font=宋体]细胞抗体技术:[/font][/font][font=宋体]优势:[/font][font=宋体]①无需杂交瘤融合[/font][font=宋体]②制备周期短[/font][font=宋体]③重链、轻链天然配对[/font][font=宋体]④无需合成基因[/font][font=宋体]⑤可直接获得各物种抗体[/font][font=宋体] [/font][font=宋体]劣势:[/font][font=宋体]①需要新鲜样本[/font][font=宋体]②抗原特异性细胞比例低[/font][font=宋体]③操作环境要求严格[/font][font=宋体] [/font][font=宋体][font=宋体]目前义翘神州提供[url=https://cn.sinobiological.com/services/monoclonal-antibody-production-services][b]单克隆抗体制备服务[/b][/url],同时拥有流式单[/font][font=Calibri]B[/font][font=宋体]细胞分选平台、噬菌体抗体库技术平台、杂交瘤开发平台…… 可供大家选择,有需求或者了解具体详情可以查看[/font][font=Calibri]https://cn.sinobiological.com/services/monoclonal-antibody-production-services[/font][/font][font=Calibri] [/font]
[font=宋体]目前有多种方法可用于开发单克隆抗体。杂交瘤技术是经典的抗体开发技术,但效率相对较低,而且容易丢失抗体的多样性。噬菌体展示技术广泛用于单抗开发,但容易丢失抗体的天然配对信息。[/font][font=宋体][font=宋体]一般认为,在抗体开发中,保留[/font][font=Calibri]B[/font][font=宋体]细胞的天然[/font][font=Calibri]VH[/font][font=宋体]和[/font][font=Calibri]VL[/font][font=宋体]配对是十分重要的。近年来兴起的单个[/font][font=Calibri]B[/font][font=宋体]细胞技术保留了轻重链可变区的天然配对,具有简单快捷、所需细胞数量较少、效率高等优势。该技术通过直接扩增单[/font][font=Calibri]B[/font][font=宋体]细胞的[/font][font=Calibri]VH[/font][font=宋体]和[/font][font=Calibri]VL[/font][font=宋体]编码基因,是一种从人和免疫动物中制备单克隆抗体的有力技术。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]利用单[/font][font=Calibri]B[/font][font=宋体]细胞分选平台,义翘神州可向全球客户提供单[/font][font=Calibri]B[/font][font=宋体]细胞抗体制备服务,整个过程涉及单[/font][font=Calibri]B[/font][font=宋体]细胞分离、测序、克隆和单[/font][font=Calibri]B[/font][font=宋体]细胞抗体筛选等步骤。[/font][/font][font=宋体] [/font][font=宋体][b][font=宋体]单[/font][font=Calibri]B[/font][font=宋体]细胞抗体发现的工作流程[/font][/b][/font][font=宋体] [font=Calibri]1[/font][font=宋体])单个[/font][font=Calibri]B[/font][font=宋体]细胞的分离[/font][/font][font=宋体] [/font][font=宋体][font=宋体]从外周血或淋巴组织中分离单[/font][font=Calibri]B[/font][font=宋体]细胞,有随机分离和抗原特异性分离两种方式。随机[/font][font=Calibri]B[/font][font=宋体]细胞分离,可通过显微操作、激光捕获显微切割和荧光激活细胞分选([/font][font=Calibri]FACS[/font][font=宋体])等进行细胞挑选。抗原特异性分离可通过抗原包被磁珠、多参数[/font][font=Calibri]FACS[/font][font=宋体]的荧光素标记抗原、溶血斑块实验和荧光焦点法等方法进行抗原特异性[/font][font=Calibri]B[/font][font=宋体]细胞的筛选。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]利用[/font][font=Calibri]FACS[/font][font=宋体]技术,可以根据特定细胞表面标志物的表达模式,明确区分待分选[/font][font=Calibri]B[/font][font=宋体]细胞的发育和分化阶段,几乎任何阶段的[/font][font=Calibri]B[/font][font=宋体]细胞都可以分选。为了有效获得特异性抗体,必须评估供体的免疫应答,例如,在单细胞分离之前,使用酶联免疫斑点技术([/font][font=Calibri]ELISPOT[/font][font=宋体])测定外周血中抗体特异性细胞([/font][font=Calibri]ASC[/font][font=宋体])的丰度,从而选择含抗原特异性抗体浓度较高的血样进行后续抗体制备。[/font][/font][font=宋体] [/font][font=宋体] [font=Calibri]2[/font][font=宋体])单[/font][font=Calibri]B[/font][font=宋体]细胞抗体的测序和克隆[/font][/font][font=宋体] [/font][font=宋体][font=宋体]通常在[/font][font=Calibri]96[/font][font=宋体]孔板上进行单细胞的[/font][font=Calibri]cDNA[/font][font=宋体]合成。全长[/font][font=Calibri]Ig[/font][font=宋体]基因转录产物通过巢式或半巢式[/font][font=Calibri]RT-[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url][/font][font=宋体]进行扩增。通常情况下,对抗体重链轻链可变区不同前导序列设计前向引物的混合物,反向引物特异性互补于抗体恒定区。某些情况下,如果分离和扩增不同同种型的抗体,反向引物则是特异性互补于各种同种型抗体恒定区的混合物。表达载体可直接转染至哺乳动物细胞中,用于单克隆抗体的体外表达。[/font][/font][font=宋体] [/font][font=宋体] [font=Calibri]3[/font][font=宋体])抗体的表达和筛选[/font][/font][font=宋体] [/font][font=宋体][font=宋体]鉴定抗体或片段的抗原特异性和生物活性之前,需将携带有抗体基因的表达载体在相应系统中表达。最简单和最常见表达系统是原核系统(例如大肠杆菌),而哺乳动物细胞系统(例如[/font][font=Calibri]HEK 293[/font][font=宋体]、[/font][font=Calibri]CHO[/font][font=宋体]细胞)更有利于抗体的翻译后修饰,主要是瞬时表达或稳定表达。在[/font][font=Calibri]E. coli[/font][font=宋体]中,通常抗体基因表达为抗原结合片段([/font][font=Calibri]Fab[/font][font=宋体])的形式,而在哺乳动物细胞中,以完整的[/font][font=Calibri]IgG[/font][font=宋体]形式表达。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/single-b-cell-antibody-service][b]单个[/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/services/single-b-cell-antibody-service][b]B[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/services/single-b-cell-antibody-service][b]细胞抗体服务[/b][/url],包含:流式单[/font][font=Calibri]B[/font][font=宋体]细胞服务和基于[/font][font=Calibri]Beacon[/font][font=宋体]平台的单[/font][font=Calibri]B[/font][font=宋体]细胞抗体开发,更多详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/services/single-b-cell-antibody-service[/font][/font][font=宋体] [/font][font=宋体][font=宋体]文章来源:[url=https://cn.sinobiological.com/resource/antibody-technical/single-b-cell-technology][b]单[/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/resource/antibody-technical/single-b-cell-technology][b]B[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/resource/antibody-technical/single-b-cell-technology][b]细胞抗体技术[/b][/url]:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/single-b-cell-technology[/font][/font][font=Calibri] [/font]
[font=宋体][font=宋体][url=https://cn.sinobiological.com/news/optimizing-pk-assays-with-anti-idiotype-antibodies][b]抗独特型抗体[/b][/url]在生物医学领域中具有重要地位。作为一种高度特异的免疫分子,它能够精确识别并紧密结合其他抗体或抗原的独特型位点,进而在疾病诊断、治疗和生物标志物发现等多个方面发挥关键作用。因此,在药物研发过程中,对生物药的安全性和疗效评估显得尤为关键。尤其是在对原研药和生物仿制药进行药代动力学([/font][font=Calibri]PK[/font][font=宋体])分析和抗药抗体([/font][font=Calibri]ADA[/font][font=宋体])测定时,抗独特型抗体更是衡量患者样本中抗体药物浓度的有力工具,并可用作抗药抗体([/font][font=Calibri]ADA[/font][font=宋体])的阳性对照。[/font][/font][font=宋体] [/font][font=宋体][b][font=宋体]一、药代动力学([/font][font=Calibri]PK[/font][font=宋体])分析[/font][/b][/font][font=宋体] [/font][font=宋体][font=宋体]药代动力学([/font][font=Calibri]PK[/font][font=宋体])描述并表征了药物在人或动物体内的四个不同阶段:吸收、分布、代谢和排泄(也称为[/font][font=Calibri]ADME[/font][font=宋体])。在药物开发中,[/font][font=Calibri]PK[/font][font=宋体]分析提供了药物与身体相互作用以及疗效强度和疗效持续时间的基本信息。在开发生物仿制药时,需要通过比较[/font][font=Calibri]PK[/font][font=宋体]分析来评价与原研药在生物活性的潜在差异。[/font][/font][font=宋体][font=宋体]根据结合模式和性质的不同,抗独特型抗体可分为三种类型:抗原阻断型、抗原非阻断型和药物靶标复合物型。基于这些特点,可以建立不同形式的[/font][font=Calibri]PK[/font][font=宋体]检测,以测量血清中的抗体药物含量,包括游离型、结合型或总量。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]抗独特型抗体可用于定量检测动物或人血清中的抗体药物水平,是[/font][font=Calibri]PK[/font][font=宋体]研究的关键检测试剂。抗体药物定量分析有多种分析方法,其中[/font][font=Calibri]ELISA[/font][font=宋体]为最常用的形式。在抗独特型抗体捕获[/font][font=Calibri]ELISA[/font][font=宋体]中,将抗独特型抗体包被在平板上,再将含有抗体药物的样本加入系统中,然后用特异性结合药物的标记抗独特型抗体定量抗体药物。[/font][/font][font=宋体] [/font][font=宋体][b][font=宋体]二、免疫原性[/font][font=Calibri]/[/font][font=宋体]抗药抗体([/font][font=Calibri]ADA[/font][font=宋体])检测[/font][/b][/font][font=宋体] [/font][font=宋体][font=宋体]免疫原性评价主要采用抗药抗体([/font][font=Calibri]anti-drug antibody, ADA[/font][font=宋体])分析的方法进行,这是治疗性蛋白药物(如单克隆抗体、[/font][font=Calibri]ADC[/font][font=宋体]和融合蛋白)开发过程中的关键步骤。在这些情况下,通常采用多层次递进式进行(图[/font][font=Calibri]3[/font][font=宋体])。该方法首先采用高灵敏的筛选试验鉴别阳性抗体样本,使用验证性试验尽量减少假阳性结果,然后使用表征试验评估抗体的中和能力。[/font][/font][font=宋体][font=宋体]在整个过程中,抗独特型抗体是必要的试剂。检测[/font][font=Calibri]ADA[/font][font=宋体]的检测方法有多种,包括[/font][font=Calibri]ELISA[/font][font=宋体]、放射免疫沉淀法([/font][font=Calibri]RIPA[/font][font=宋体])、表面等离子体共振([/font][font=Calibri]SPR[/font][font=宋体])和电化学发光检测([/font][font=Calibri]ECL[/font][font=宋体])。其中,桥联[/font][font=Calibri]ELISA[/font][font=宋体]是最常用方法,可用于检测所有[/font][font=Calibri]ADA[/font][font=宋体]同种型([/font][font=Calibri]IgG[/font][font=宋体]、[/font][font=Calibri]IgM[/font][font=宋体]、[/font][font=Calibri]IgA[/font][font=宋体]等)。在典型的桥联[/font][font=Calibri]ELISA[/font][font=宋体]中,将抗体药物预包被在平板上,并将标记的抗体药物与患者样本一起孵育,以检测是否存在[/font][font=Calibri]ADA[/font][font=宋体](图[/font][font=Calibri]4[/font][font=宋体])。抗独特型抗体将用作阳性对照或参比标准品,用于样本中[/font][font=Calibri]ADA[/font][font=宋体]的定性分析。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供为客户提供了从抗原制备、抗独特型抗体开发到检测方法建立和试剂盒开发的全方位、一站式的定制[url=https://cn.sinobiological.com/services/anti-idiotype-antibody-service][b]抗独特型抗体生产服务[/b][/url]。[/font][/font][font=宋体] [/font][font=宋体]①抗独特型兔多抗制备服务:[/font][font=宋体]交付内容:[/font][font=宋体]? 纯化抗体[/font][font=宋体][font=宋体]? [/font][font=Calibri]CoA[/font][/font][font=宋体] [/font][font=宋体][font=宋体]周期:[/font][font=Calibri]2-3[/font][font=宋体]个月[/font][/font][font=宋体] [/font][font=宋体]②抗独特型鼠单抗制备服务[/font][font=宋体]交付内容:[/font][font=宋体][font=宋体]? 阳性克隆,[/font][font=Calibri]2[/font][font=宋体]管细胞[/font][font=Calibri]/[/font][font=宋体]克隆[/font][/font][font=宋体][font=宋体]? 纯化抗体,[/font][font=Calibri]10 mg/[/font][font=宋体]克隆[/font][/font][font=宋体][font=宋体]? [/font][font=Calibri]ELISA[/font][font=宋体]抗体对(可选)[/font][/font][font=宋体][font=宋体]? [/font][font=Calibri]CoA[/font][/font][font=宋体] [/font][font=宋体][font=宋体]周期:[/font][font=Calibri]4~6[/font][font=宋体]个月[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多详情可以关注:抗独特型抗体[/font][font=Calibri]https://cn.sinobiological.com/news/optimizing-pk-assays-with-anti-idiotype-antibodies[/font][/font][font=Calibri] [/font]
一、新制剂品种的开发除片剂和胶囊等常用剂型外,从多种剂型、多种用药新途径和新方法考虑开发制剂以提高药效,减低副作用,改善病人用药顺应性,是开发新制剂的一个重要方面。如将雌二醇、黄体酮、甲地孕酮等开发成软胶囊,将硫酸沙丁胺醇等药物开发成鼻腔给药制剂、雾化吸入剂等,将阿昔洛韦和环孢素分别制备成缓释制剂和微乳制剂等。 儿童及老人用制剂如滴剂和栓剂,五官科用制剂如牙线、毫微粒、口胶剂、眼胶剂以及速溶、速效制剂等都是具有治疗或技术特色的制剂。除分散片外,还有多种剂型可达到速溶和速效。如含水溶性药物的软胶囊和滴剂,可溶性包合物制剂,固体分散物制剂,可溶性片等。 研究复方制剂也是国外制剂行业的重要方向。大量的OTC药物是复方制剂。与普通制剂开发相比较,国内的复方制剂较少,对开发复方制剂应有充分的临床用药依据和药效学依据,对开发治疗危重疾病的复方制剂应充分调研。开发原则是应有协同作用,减少副作用。二、口服缓释及控释制剂的发展 缓控释制剂不断增加,对其技术及质量的要求也不断提高。国外对这类制剂发展提出了更高要求,即从仅要求平稳血药浓度发展到以提高病人在疾病状态下的药效为目标。开发这类产品应解决三个关键的问题:①该制剂能否提高治疗值?即该制剂能否有治疗需要的释药速度、释药时间及部位或靶位?②该制剂如何达到以上要求?即对上述释药特征是否优化?是否经药效学和药理学实验取得了药动学与药效学的相关,特别是在疾病状态下的相关?③该制剂选择的剂型和技术是否对以上特征最适合?是否包括了对经济学、方便用药和制定剂量方案等方面的综合考虑。按此标准,仅有很少缓控释制剂符合要求。 但从现有开发角度,缓控释品种大大增加。许多作用强的药物、半衰期很短或很长的药物、抗生素药物、成瘾性药物均制成缓释制剂以适应特殊医疗应用。发展1天1次给药的缓释及控释品种、复方缓释及控释制剂、液体缓释及控释制剂是今后的重要趋势。三、注射给药剂型1、注射用微球 发展注射用微球的主要目的是为了达到缓释、长效。1986年法国Ipsen上市肌注曲普瑞林-聚丙交酯-乙交酯微球;此后又陆续生产了醋酸亮丙瑞林、布舍端林和米特瑞林肌注微球。正在研究的其它微球制剂有皮下注射的生长激素释放因子(GRF)毫微球、羧基喜树碱聚氰基丙烯酸正丁酯毫微粒、睾丸酮微球等。2、静脉注射用脂质体 各种抗癌药物等的脂质体均有研究,上市的有阿霉素、两性霉素、柔红霉素等。采用挤出冻干设备生产以及采用空白脂质体包合是发展脂质体的重要工艺改进。有报道将各种细胞因子如IFN-γ、IL-1、TNF-α等包埋于脂质体中,静脉注射达缓释效果,改变体内的分布特性,更易进入细胞发挥作用、提高受体敏感性,提高细胞毒活性。值得一提的则是脂质体用作基因治疗的载体。脂质体可携带各种基因片段,保护基因不被核酸酶降解,并且脂质与细胞膜融合将目的基因导入细胞。脂质体介导的基因转移方法被美国癌症协会批准为应用于临床基因治疗的第一方案。3、疫苗控释制剂 一次接种疫苗以达到完全免疫、提高接种类、减低接种费用是世界卫生组织疫苗发展规划的主要目标之一。目前进行的研究的疫苗控释制剂主要是微球或其它微粒制剂,通过材料的选择和包埋程度。可控制疫苗释放速度,如速释及恒释,脉冲释放等。研究的疫苗包括类毒素疫苗、病毒疫苗、核酸疫苗及人工合成疫苗等。4、脂肪乳剂 近年来已臻成熟的乳剂生产工艺和乳剂辅料为含药脂肪乳的开发生产创造了条件。如依托米酯、异丙酚、棕榈酸地塞米松脂质乳剂、氟比洛芬乙氧基α-乙酯脂质乳剂、前列腺素E1脂质乳等。
“色”路蹒跚,萧规曹随,浅谈固体制剂溶出度方法学部分题外话:我们吃的不是含量,是生物利用度;溶出度技术是评价固体制剂的灵魂与核心所在。以上是谢沐风老师说的,很在理。定义:大多数口服固体制剂在给药后必须经吸收进入血液循环,达到一定血药浓度后方能奏效,从而药物从制剂内释放出并溶解于体液是被吸收的前提,这一过程在生物药剂学中称作溶出,而溶出的速度和程度称溶出度,从药品检验的角度上讲,溶出度系指药物从片剂或胶囊等固体制剂在规定的溶剂中溶出的速度和程度。 过去认为只有难溶性药物才有溶出度的问题,但近年来研究证明,易溶性药物也会因制剂的配方和工艺不同而致药物溶出度有很大差异,从而影响药物生物利用度和疗效,在USP中规定测定溶出度的制剂有相当数量是易溶性药物。质量研究中溶出度的内容:溶出度测试方法学和溶出行为方法学。溶出度研究试验主要包括以下内容:(1)溶出介质的选择,(2)溶出介质体积的选择,(3)溶出方法(转篮法与桨法)的选择,(4)转速的选择,(5)溶出度测定方法的验证,(6)溶出度均一性试验(批内),(7)重现性试验(批间)等。检验测试方法检验方法-方法学验证1,检测波长的确定(辅料以及胶囊的干扰,胶囊一是对测试干扰,而是对样品崩解的影响)2,空白试验3,滤膜干扰验证4,线性试验5,回收率6,溶液稳定性滤膜干扰试验:对照品用离心对比。线性试验(50/60% 限度 100%)回收率溶液稳定性(0.5h 1.0h 2.0h 8.0h)溶出度方法溶出方法考察1,溶出转速选择2,溶出介质选择3,溶出限度和取样时间的确定4,溶出条件的确定5,溶出均一性考察6,三批检验溶出介质/检测波长的选择:关键点为做曲线,取样时间点5、10、20(15)、30、45、60分钟。不同的介质可能影响到波长的选择,要和对照品一致。溶出介质体积的选择:漏槽试验,参照标准。一般是500/900/1000ml溶出装置的选择:利用标准方法进行试验,做曲线。一般是胶囊或易上浮样品用篮法,片一般用桨法。具体做法篮法[font=Times New Roma
[font=宋体][font=宋体]人[/font][font=Calibri]-[/font][font=宋体]鼠嵌合抗体:利用[/font][font=Calibri]DNA[/font][font=宋体]重组技术将鼠源单抗的轻链、重链可变区插入含有人抗体恒定区的表达载体中,转化哺乳动物细胞进行表达所产生的单克隆抗体。人[/font][font=Calibri]-[/font][font=宋体]鼠嵌合抗体的人源化程度可达到[/font][font=Calibri]70%[/font][font=宋体],完整的保留了鼠源单抗的可变区及亲本活性,人抗体恒定区的引入则降低了免疫原性。[/font][/font][font=宋体] [/font][b][font=宋体]人鼠嵌合抗体基本原理[/font][/b][font=宋体][font=宋体]是从分泌某种鼠单抗的杂交瘤细胞基因组中分离并鉴定出重排的功能性鼠[/font][font=Calibri]VL[/font][font=宋体](轻链可变区)和[/font][font=Calibri]VH[/font][font=宋体](重链可变区),经过基因重组分别与人的[/font][font=Calibri]CL[/font][font=宋体](轻链恒定区)和[/font][font=Calibri]CH[/font][font=宋体](重链恒定区)区基因按照一定的方式相拼接,克隆到表达载体中构建鼠[/font][font=Calibri]/[/font][font=宋体]人轻重链基因表达载体,并转入适当的宿主细胞表达来制备特异性嵌合抗体。[/font][/font][font=宋体] [/font][font=宋体]对于其他类型的人源化抗体,其优势在于,技术路线简单,易于操作;抗体完整性好,在体内滞留时间长;鼠源抗体的亲和力和特异性都得到保留,在临床上得到了良好的反应。[/font][font=宋体] [/font][font=宋体]构建人鼠嵌合抗体主要包括:克隆鼠抗体可变区基因,钓取人抗体恒定区基因,拼接鼠抗体可变区基因与人抗体恒定区基因以及构建载体和宿主细胞。[/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体]人鼠嵌合型单克隆抗体制备优点:[/font][/b][font=宋体] [/font][font=宋体][font=宋体]①不仅保留了亲本鼠抗体的高特异性和亲和力,而且使鼠源性成分减少 [/font][font=Calibri]70%[/font][font=宋体]左右;[/font][/font][font=宋体] [/font][font=宋体][font=宋体]②其人源[/font][font=Calibri]Fc [/font][font=宋体]段能有效介导生物学效应功能,如抗体依赖性细胞介导的细胞毒作用([/font][font=Calibri]Antibody dependent cell-mediated cytotoxicity[/font][font=宋体],[/font][font=Calibri]ADCC[/font][font=宋体])、补体依赖性细胞毒作用([/font][font=Calibri]Complement dependent cytotoxicity[/font][font=宋体],[/font][font=Calibri]CDC[/font][font=宋体])等;[/font][/font][font=宋体] [/font][font=宋体]③能自由地选择抗体的型、亚型、类、亚类、大小、结构域及添加糖基化位点等,以利用其不同的生物学特点及理化特性;[/font][font=宋体] [/font][font=宋体]④由高效真核表达载体和人抗体恒定区组成的嵌合抗体表达“盒子”可以容许插入不同的鼠单克隆抗体的可变区,缩短操作和研制周期;[/font][font=宋体] [/font][font=宋体]⑤操作相对简单。[/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体][url=https://cn.sinobiological.com/resource/antibody-technical/chimeric-monoclonal-antibody]嵌合抗体[/url]主要有三种类型:[/font][/b][font=宋体] [/font][font=宋体][font=Calibri]1[/font][font=宋体]、嵌合[/font][font=Calibri]IgG[/font][font=宋体]抗体[/font][/font][font=宋体] [/font][font=宋体][font=宋体]目前嵌合抗体的研究主要集中在嵌合[/font][font=Calibri]IgG[/font][font=宋体]([/font][font=Calibri]Immunoglobulin G[/font][font=宋体])抗体。其构建基本原理是从生产某种鼠源单克隆抗体的杂交瘤细胞中得到目的抗体[/font][font=Calibri]V[/font][font=宋体]区([/font][font=Calibri]variable region[/font][font=宋体])基因,再与人类的[/font][font=Calibri]C[/font][font=宋体]区([/font][font=Calibri]constant region[/font][font=宋体])基因重组并克隆到合适载体中,然后转入受体细胞表达(如图[/font][font=Calibri]1[/font][font=宋体])。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]在构建嵌合抗体时应根据不同目的选择不同的[/font][font=Calibri]C[/font][font=宋体]片段。这是因为不同类型的人抗体[/font][font=Calibri]C[/font][font=宋体]区与补体和[/font][font=Calibri]Fc[/font][font=宋体]([/font][font=Calibri]fragment crystallizable,Fc[/font][font=宋体])相互作用的能力以及引发细胞溶解的功能不尽相同。在体内免疫系统中,抗体的[/font][font=Calibri]Fc[/font][font=宋体]段和效应细胞相互作用,发挥特异的生物学功能。例如[/font][font=Calibri]IgE[/font][font=宋体]([/font][font=Calibri]Immunoglobulin E[/font][font=宋体])可介导炎症反应等,[/font][font=Calibri]IgM[/font][font=宋体]活化补体的能力强,[/font][font=Calibri]IgG1[/font][font=宋体]的补体活化能力比[/font][font=Calibri]IgG3[/font][font=宋体]强,且在[/font][font=Calibri]ADCC[/font][font=宋体]作用([/font][font=Calibri]antibody dependent cell mediated cytotoxicity[/font][font=宋体])触发能力上也比[/font][font=Calibri]IgG3[/font][font=宋体]强。在与[/font][font=Calibri]Fc[/font][font=宋体]受体的结合能力上[/font][font=Calibri]IgG1[/font][font=宋体]和[/font][font=Calibri]IgG3[/font][font=宋体]比较强,[/font][font=Calibri]IgG4[/font][font=宋体]次之,而[/font][font=Calibri]IgG2[/font][font=宋体]几乎检测不到。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2[/font][font=宋体]、嵌合[/font][font=Calibri]Fab[/font][font=宋体]和[/font][font=Calibri]F(ab')2[/font][font=宋体]抗体[/font][/font][font=宋体] [/font][font=宋体][font=宋体]嵌合[/font][font=Calibri]Fab[/font][font=宋体]([/font][font=Calibri]antigen-binding fragment, Fab[/font][font=宋体])和[/font][font=Calibri]F(ab')2[/font][font=宋体](具有两个抗原结合表位的片段)抗体的优势就是渗透力强。[/font][font=Calibri]Fab[/font][font=宋体]嵌合抗体制备原理为:将功能性抗体[/font][font=Calibri]L,H[/font][font=宋体]链的[/font][font=Calibri]V[/font][font=宋体]区基因与人的轻链[/font][font=Calibri]k[/font][font=宋体]和[/font][font=Calibri]H[/font][font=宋体]链[/font][font=Calibri]CH1[/font][font=宋体]进行重组,克隆到表达载体中,在转入宿主细胞表达。不过对于大多数该类型的抗体来说,由于亲和力较低,分子量小,容易被肾小球过滤而从血液中消失,因此大多数不适合单独使用于临床治疗。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多[url=https://cn.sinobiological.com/services/chimeric-antibody-production-service][b]嵌合抗体生产服务[/b][/url]详情可以查看:[/font][font=Calibri]https://cn.sinobiological.com/services/chimeric-antibody-production-service[/font][/font][font=宋体][font=宋体]义翘神州利用[/font][font=Calibri]CDR[/font][font=宋体]置换技术及计算机辅助结构模拟设计可对羊驼纳米抗体、鼠源单抗进行人源化改造,保证人源化程度 [/font][font=Calibri]95%[/font][font=宋体],为客户提供优质的[url=https://cn.sinobiological.com/services/antibody-humanization-service][b]单克隆抗体人源化服务[/b][/url]。详情可关注:[/font][font=Calibri]https://cn.sinobiological.com/services/antibody-humanization-service[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]