乐枫生物 RephiQuik PES 无菌滤器试用活动开启
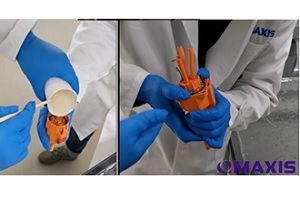
夏天悄悄离去,秋天款款而来。金黄的时节要来了,乐枫生物官网试用推广又要开始啦! 这次乐枫生物推出的活动产品是用于生命科学实验室中组织培养基、血清样品或其他生物溶液除菌过滤的RephiQuik 32mm无菌PES(聚醚砜)针头式过滤器产品。产品直径32mm,孔径有0.22 um和0.45 um两种。 想要了解与进口产品相比,过滤速度如何,过滤效果怎样,使用方便与否,试试就知道了! 2018年8月17日-2018年9月30日,点击乐枫生物官网试用中心填写试用申请表格即可参加。快快参加吧!!! 乐枫生物的RephiQuik PES无菌滤器,采用的 亲水性聚醚砜 PES 滤膜,其的不对称结构和分布规整的膜孔,使之具有高通量,高流速的优势。与其他滤膜相比,还具有低蛋白吸附,低溶出等特点。PES滤膜适用性广,通常用来做培养基,缓冲液和其他水相溶液的快速除菌过滤。结构设计精巧,制作工艺严格的RephiQuik无菌PES过滤器,给你的实验带来安全可靠的保证! 产品特点: 的设计使针式滤器拥有更大的滤膜面积及更小的死体积。 有效增加了流速和过滤量,提高了过滤效率。 加强型二次注塑工艺制作,可耐受更高的操作压力,提高过滤速度,使过滤变得更加轻松。 ETO 灭菌更为彻底。 不含热原及 RNA 酶,用于生物实验更安全可靠。 每个滤器均单独包装,方便使用。产品应用: 生命科学实验中组织培养基配置 血清样品除菌过滤 缓冲液或其他生物溶液除菌过滤 了解产品更多介绍及规格,请查看:乐枫PES无菌滤器详情 试用后购买产品,可参加乐枫9月份的开学无菌滤器促销活动。 优惠的价格和精美的礼品等你来! 更多活动详情可登录乐枫官网或拨打乐枫厂商400电话。 关于上海乐枫生物科技有限公司 上海乐枫生物专业从事高端水纯化和实验室分离纯化产品的研发、设计和制造,致力于,为生命科学和生物技术提供精锐品质、高附加值的创新产品。乐枫产品线包括实验室纯水系统、密理博纯水兼容耗材和实验室分离纯化过滤产品。成立十年,乐枫创立出了自己的品牌RephiLe(瑞枫),拥有30多项专利和多个软件著作权。产品销往全球近90个国家和地区。更多 RephiLe 产品信息,请登陆:乐枫官网关注RephiLe 企业微信:乐枫纯水。关注乐枫动态! 纯水,去离子水,DI水,蒸馏水,反渗透水,RO水,超纯水,EDI,过滤,针头式,无菌,HPLC,ICP-MS,AAS,LC-MS,生化分析仪,测序,NGS高通量测序,临床,老化机,洗瓶机,离子色谱,滤膜,空气过滤,二氧化碳培养箱,发酵罐