[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]指数法
求助 ISO 9377-2 水质.油气指数的测定.第2部分:溶剂萃取法和[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法谢谢了,我很急呀。
BS EN ISO 9377-2-2000水质.烃油指数的测定.用溶剂萃取法和气相色谱法Water quality-Deteremination of hydrocarbon oil index- Part 2: Method using solvent extraction and gas chromatography
气相色谱有参照正构烷计算的保留指数。请问液相色谱有没有类似气相的保留指数?
如题,今天看到有要求色谱柱的极性指数小于10的要求,不知道记性指数如何计算或者评估,有知道的达人能解释下吗?先行拜谢。
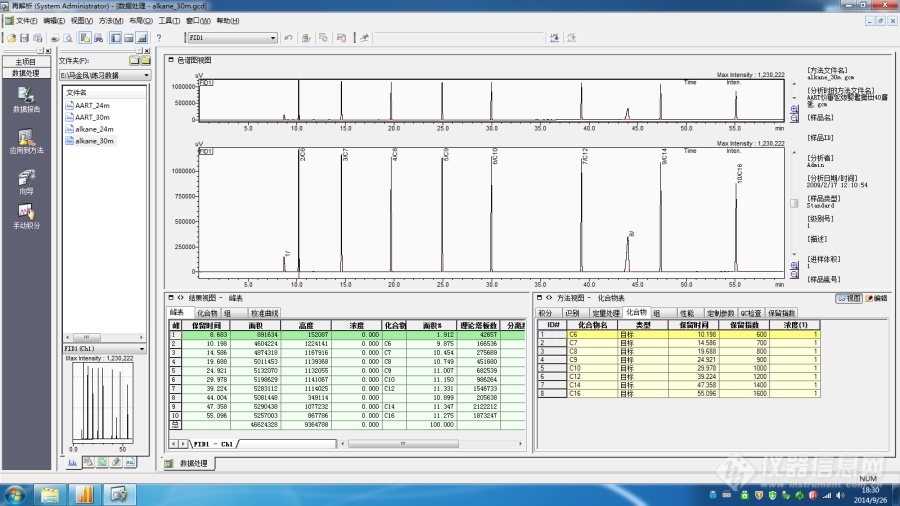
[color=black]Labsolution色谱数据工作站保留指数校正的操作方法[/color][align=center][color=black]概述[/color][/align][color=black]保留指数本质上是规范化的保留时间,在确定的分析条件下,与固定相性质相关,当色谱柱的尺度规格发生变化时,采用保留指数校正功能自动计算和校准定量方法中目标组分的保留时间。[/color][align=center][color=black]一 保留指数校正的原理介绍[/color][/align][color=black]保留指数本质上是规范化的保留时间——是以正构烷烃保留时间为标尺,规范待测组分的保留时间。对于一根确定的色谱柱,在相同的温度和流量操作条件之下,如果色谱柱的具体尺寸规格发生了一定程度的变化,并不影响待测目标物质的保留指数的具体数值。[/color][color=black]例如在农残分析的场合下,色谱工作者在一次进样中可能同时需要处理数十至数百个目标组分的分析。当方法运行一段时间之后,色谱柱需要进行维护。常见的情况下,色谱柱的长度会被明显截短,那么目标组分的保留时间会发生显著的变化。[/color][color=black]此时如果将所有目标组分的保留时间进行重新校准,无疑色谱工作者会面临较大的工作量。如果使用保留指数校正功能的话,只需要重新进样测试一下正构烷烃标准品(前提是方法最初开发时,事先进样过正构烷烃标品),修正分析方法即可,这样可以显著的提高分析效率。[/color][color=black]下文以Labsolution Workstation为例予以说明。[/color][align=center][color=black]二 Labsolution 色谱数据工作站的操作步骤[/color][/align][color=black]假设某项色谱分析,色谱柱原始长度为30m,进样正构烷烃标品获得数据文件为alkane-30.gcd;进样标准样品获得数据文件为AART-30m.gcd。[/color][color=black]当分析进行一段时间之后,色谱柱经过不断维护后长度变成24m。此时进样正构烷烃标品,获得数据文件alkane-24.gcd;进样标准样品获得数据文件为AART-24m.gcd。[/color][color=black]然后基本操作步骤如下:[/color][color=black]2.1 输入原始正构烷烃的保留指数[/color][color=black]进入Labsolution的“再解析”模块,打开alkane-30m.gcd此数据文件,在“方法”界面下,编辑化合物表。此时将正构烷烃的化合物名称、保留时间和保留指数输入到表格中。[/color][color=black]然后保存此数据。[/color][align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108261803071420_5701_1604036_3.png[/img][/align][color=black]2.2 标准样品的保留指数计算[/color][color=black]打开标准样品数据AART-30m.gcd,然后点击“方法”界面下的“保留指数”选项卡,点击“从数据文件加载”图标,并选择“alkane-30m”此数据文件。[/color][align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108261803072435_8318_1604036_3.png[/img][/align][align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108261803072559_6125_1604036_3.png[/img][/align]然后点击“助手栏”中的“向导”图标,依次点击“下一步”,创建完成方法文件,并保存。此时Labsolution色谱柱数据工作站会自动计算出各个目标组分的保留指数。此时保存方法文件为“标样采集方法”。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108261803074199_3900_1604036_3.png[/img][/align]2.3 保留指数的校正当色谱柱长度变为24m后,标样数据中的待测物质保留时间均发生缩短。此时打开柱长24m获得的正构烷烃数据“alkane-24m.gcd”,然后编辑化合物表,填写保留指数,并保存数据问题。然后点击“编辑”菜单,选择“自动修改保留时间AART”。在依次点击“下一步”,此时方法文件中所有目标组分的保留时间,已经同时自动修正为24m下的保留时间。[align=center]小结[/align][color=black]利用保留指数校正功能,可以明显缩短[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析方法修改消耗的时间,以提升分析效率。[/color][align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108261803075254_5487_1604036_3.png[/img][/align]
[color=#444444]Kovats 指数可以用于液相色谱定性分析吗?请给出具体原因,谢谢[/color]
有机分子的色谱保留指数与分子量和结构有关吗?理论依据是什么?
N2000色谱工作站中的面积指数法为什么不能用?
用FID分析含有不稳定物质3-羟基丙醛的混合液体,如何确定色谱图中的哪一个峰对应这种物资,此物质没有标准样品,保留指数也没有查到(FFAP),除了色质联用以外,还有没有比较简单的方法可以快速确定?另外,要对购买的有机物液体进行成分鉴定(已知主要成分),在北京的哪些机构可以进行
摘 要:利用固相微萃取技术-[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法(SPME-GC)研究了多环芳烃(PAHs)的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]保留行为特征.结果表明,在利用SPMC-GC分析PAH过程中,计算得的PAHs的Lee保留指数与传统的直接分析PAHs溶液所得的保留指数一致;同时,在不同色谱操作条件(如恒流,恒压和程序升压),利用SPMC-GC分析所得的保留指数再现性很好,所有上述不同操作条件下,PAHs的保留指数均能保持在1个指数单位范围内,能够满足定性分析的要求.关键词:固相微萃取;多环芳烃;保留指数中图分类号:X132 文献标识码:B 文章编号:1006—5776(1999)02—0014—02 固相微萃取技术(Solid-phase microextraction,SPME)是八十年代代末发展起来的一项新型的无溶剂化样品前处理技术,它集萃取、浓缩和解吸于一体,与上述传统的方法相比具有许多优点,如无需溶剂、不需复杂的仪器设备、且灵敏度高、经济、样品需要量小、无需对样品进行预处理、可实现自动化等诸多优点.它可以与[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]和液相色谱联用快速有效地分析样品中痕量有机组份[1~3]. 多环芳烃(PAHs)是一类广泛存在的典型环境污染物,环境样品组成复杂,对PAHs组分进行定性历来是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析PASs的最困难的问题,目前主要是通过GC-MC结合[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]保留指数来解决[4]. 固相微萃取技术-[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法(SPME-GC)与原有的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析技术具有很大的区别.其中之一就是样品进行色谱分析过程中不需溶剂,这就涉及一个问题即原有的保留指数与利用SPME-GC分析所得PAHs的保留指数是否一致.因此,本文在不同色谱条件下,考察了利用PAHs溶液直接分析和SPMC-GC分析两种方法之间保留指数的差异.1 实验部分1.1 试剂与仪器 分别配制一定浓度的多环芳烃萘、联苯、二氢苊、芴、菲、蒽、荧蒽、芘、苯并(a)蒽、、苯(并k)荧蒽、苯并(e)芘、苯并(a)芘、苝、苉的苯溶液和水溶液. HP6 890[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url](Hewlett Packard Inc.)配氢火焰检测器和化学工作站,SE-54(30 m×0.25 mmi.d.,0.25 μm,J&WScientificInc.USA)石英毛细管柱. [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]用固相微萃取器及萃取头(Supelco,Inc.).1.2 实验方法 色谱条件:进样器和检测器温度分别300℃和320℃,柱温于50℃保持2 min后,以10℃/min的速率升至315℃后保持5 min,氮气作为载气. 恒压方式:柱头压力保持84 kPa,线速度为28 cm/s 恒流方式:升温过程保持流速28 cm/s 程序升压方式:柱头压力于53 kPa保持2 min后,以0.9 kPa/min的速率升至110 kPa并保持5 min.分别在上述条件下对pHAs的苯溶液进行色谱分析. SPME苯取器的中心部件是一段长1 cm的涂渍过固定相的熔融石英纤维,其固定在不锈钢针头上,置于套管内,并可以方便地在特制的注射手柄上装卸.根据萃取方法的不同,SPME可分成两种:即将萃取头直接浸入液相进行萃取的浸入式SPME法,和将萃取头置于样品瓶中液面之上进行萃取的顶空SPME法.为了达到对预分析化合物进行有效的萃取,通常可以选择涂有不同固定相的萃取头.本文采用PDMS-7的萃取头利用浸入式SPME方式对水溶液中的PAHs进行固相微萃取,萃取过程中对溶液实施搅拌,磁力搅拌器的转速为100 rpm ,萃取时间为15 min.最后,在色谱进样口进行热解吸,解吸时间为2 min.2 结果与讨论 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]是分离分析PAHs的最强有力的手段,但是由于PAHs的种类繁多,环境样品组成更为复杂.一般需要借助GC-MS来对其进行定性,然而在目前情况下,即使高分辨率质谱仪对于PAHs同分异构体的分析仍然十分困难.虽然色谱-富利叶变换红外仪联用技术可以解决这类同分异构体的定性问题,但利用GC-FTIR来解决痕量组分PAHs的定性问题技术上尚未成熟.对于上述同分异构体的定性,目前主要是通过GC-MS结合[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]保留指数来解决.由于PAHs样品沸程较宽,一般需要在程序升温条件下完成对PAHs分离分析,曾经采用经典的Kovats保留指数体系对其进行定性[5].1979年,MiltonL.Lee等提出了Lee保留指数体系,即采用PAHs中的萘、菲、、和作为标准参考物,该体系所受影响条件较小,因此在PAHs分析中得到广泛的应用[6]. 本文在研究PAHs的保留行为过程中,同样采用的是Lee保留指数体系,并分别计算出不同条件下PAHs的保留指数(见表1).从表1中数据可见,在恒压、恒流和程序升压条件下,利用传统的GC分析方法和采用SMPE-GC技术所得的PAHs保留指数均能稳合得很好,保留指数偏差维持在1个保留指数单位范围内.因此,在利用SPMC-GC技术对PAHs进行定性分析过程中,可以方便地采用文献中已有的保留指数数据. 目前,一些新型[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]可以采用温度、压力等多种程序控制技术以达到进一步改善[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的分离效率或提高分离速度.有关文献已经报导了利用传统的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析方法在不同操作模式下PAHs保留行为的研究[7].本文进一步考察了SPMC-GC分析PAHs过程中,其保留行为的特征. 由表1可见,采用恒流、恒压和程序升压方式,利用SPME-GC技术分析PAHs所得的保留指数同样相差不大,能保持在1个保留指数单位范围内.图1为利用SMPE-GC方法所得的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]图.表1 不同分析条件下多环芳烃保留指数的比较 编号 化合物 恒压 溶流恒流 升压 恒压 SPME恒流 升压 1 萘 200.00 200.00 200.00 200.00 200.00 200.00 2 联苯 235.98 236.15 235096 236.07 236.25 236.00 3 二氢苊 254.33 254.33 254.42 254.36 254.39 254.44 4 芴 270.20 270.26 270.26 270.24 270.31 270.26 5 菲 300.00 300.00 300.00 300.00 300.00 300.00 6 蒽 301.5 301.59 301.57 301.55 301.55 301.50 7 荧蒽 344.73 344.67 344.77 344.78 344.76 344.74 8 芘 352.76 352.54 352.81 352.84 352.66 352.82 9 苯并(a)蒽 398.42 398.51 398.48 398.33 398.47 398.28 10 400.00 400.00 400.00 400.00 400.00 400.00 11 苯并(k)荧蒽 446.33 446.12 446.09 446.14 446.23 446.19 12 苯并(e)芘 455.49 4455.67 455.85 455.71 455.77 455.55 13 苯并(a)芘 457.20 457.63 457.31 457.43 457.92 457.40 14 460.92 460.80 461.08 460.95 460.80 461.17 15 500.00 500.00 500.00 500.00 500.00 500.00 图1 SPME-GC方法所得PAHs的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]图 从有关分析结果可以看出,无论是色谱操作条件的改变,还是SPMC-GC分析技术的引入,对于原有的PAHs的Lee保留指数体系均无明显影响,这很好地满足了已有保留指数数据在新的分析条件的和分析技术中对PAHs定性分析的需要.
偶然见了这么一段话:以无硫天然气为底气,用静态配气法配制硫化物的标准样品,在前述的操作条件下,将已知浓度的气样注入色谱柱中,以适当的衰减记录各硫化物的谱峰,将所得相应硫化物量和峰高的数据用曲线拟合法计算比例常数k和应答指数n。 其中应答指数只得是什么。请赐教。
用TG-5MS 色谱柱测出的物质的保留指数是不是可以参考HP-5ms的保留指数,两者差别大吗?在NIST网站上几乎所有的物质都查不到TG-5MS色谱柱的保留指数信息
各位老师,小弟在坛子里阅读了大量关于用AMDIS软件计算保留指数的帖子,也查阅了一些文献,但心中仍有写疑团尚未打开,现列于此处,请大家帮忙解决,谢谢。1.用于测定保留指数所用的正构烷烃的标准品,其碳数范围应当如何选择,目前看到的有C6-C20,C7-C30,还有买两种一起使用的,如C7-C20和C21-C40,是否碳数范围越宽则测定的保留指数就越准确,如此理解是否正确?2.由于不同厂家的正构烷烃的标准品浓度有所差异,应当如何对标准品进行处理,稀释倍数当如何确定,是否一定要设为0.05%?3.正构烷烃标准品与样品应当在一致的色谱条件下进行分析,则如用SPME分析某样品的挥发性成分,使用的内径为0.75mm的衬管,可否在此情形下直接进正构烷烃标准品?4.保留指数分为恒温保留指数和程序升温保留指数,由AMDIS软件得出的保留指数是否就是程序升温保留指数呢?5.是否需要购买待分析挥发性物质的标准品,验证保留指数准确性,辅助定性呢?另外文献中所列的保留指数,是否可以直接与仪器测得的保留指数比较呢?
RCONH22 确定初始操作条件主要包括进样口温度、检测器温度、色谱柱温度和载气流速。分流进样的进样量一般不超过2μL ,最好控制在 0 .5 μL 以下 ,进样量还和分流比有关 ,分流比大时 ,进样量可大一些 ;进样口温度应接近或高于样品中最重组分的沸点 ;对于一个未知的新样品, 可将进样口温度设置为 300 ℃;常用毛细管GC 所用柱内载气线流速为:氮气 20~40 cm/s。隔垫吹扫设定为 2 ~5 mL/min , 分流比依据样品情况(如待测组分浓度等)、进样量大小和分析要求来改变, 选择一个合适的折衷分流比,用分流比范围 20∶1 ~200∶1 ,待测组分浓度大或进样量大时, 分流比可相应增大,反之则减小,用大口径柱时分流比小一些,用微型柱做快速GC 时,分流比要求很大,流比小时, 分流歧视效应可能小,但初始谱带(主要是溶剂谱带)宽度大,分流比大时,初始谱带(主要是溶剂谱带)宽度小,但分流歧视效应可能大。检测器温度可参照色谱柱的最高温度设定,而不必优化。色谱柱温度,组成简单的样品最好用恒温分析;组成复杂的样品,常需要用程序升温分离;色谱柱的初始温度应接近样品中最轻组分的沸点, 最终温度取决于最重组分沸点;升温速率依样品的复杂程度而定,建议毛细管柱的尝试温度条件设置为OV -1或SE-54 柱 :从 50 ~280 ℃,升温速率 10 ℃/min ,V - 17(OV -1701)柱:从60 ~260 ℃, 升温速率 8 ℃/ min ,PEG -20M 柱:从60 ~200 ℃,升温速率 8 ℃/ min 。这是方法开发时的初始参考条件,具体工作中再根据样品的实际分离情况来优化设定。3 尝试性分析上述初始条件设定后,便可以进行样品的尝试性分析。一般先分离标准样品,然后分析实际样品。在此过程中,还要根据分离情况不断进行优化。GC的分离优化就是要在保证分离度和灵敏度的前提下,实现快速分析。在实际工作中,一般是首先满足分离度的要求,然后提高分析灵敏度,最后再考虑尽可能缩短分析时间。改变柱温和载气流速可改变分离度;内径越小,或者填料粒度越小,柱效越高;薄液膜色谱柱的柱效高于厚液膜柱;更换色谱柱可改变分离度;用化学作用如通过生化反应改变待测物结构;程序升温是GC分离复杂混合物的有效方法;进样量小一些、进样口温度高一些、载器气流速快一些、汽化室体积小一些,分流比大一些,对窄的初始谱带宽度有利。4 气相色谱定性与定量分析对于简单的样品,可通过标准物质对照来定性。对于复杂的样品, 则要通过保留指数定性和或GC/MS来定性。对于基层监测站,气相色谱定性分析最主要是依据保留值定性,即在相同的条件下,分别注入标准样品和实际样品,根据保留值确定色谱图上哪个峰是要分析的组分。但必须注意,在同一根色谱柱上,不同的化合物可能有相同的保留值,对未知样品的定性仅仅用一个保留值还不够。双柱或多柱保留指数定性是气相色谱定性分析较为可靠的方法,不同的化合物在不同色谱柱上具有相同保留值的几率要小的多。建议对复杂的样品采用双柱或多柱保留指数法定性。气相色谱定量方法包括面积百分比法、归一化法、外标法、内标法、标准加入法。基层监测站最常用的方法是外标法,只要用一系列浓度的标准样品做出工作曲线, 就可以在完全一致的条件下对未知样品进行定量
保留指数应用(6)----不同极性柱子的保留指数关系( 本文只是一种探讨交流,可能有不足不妥之处,欢迎批评指正。未经同意,请勿转载。多谢合作!)保留指数作为气质定性一个强有力的辅助手段,在天然香精油,香气香味材料,香精产品等的分析鉴定中广泛应用。当然应用范围远不止这些。对于异构体,同系物和结构特征相似的化合物,由于其质谱图非常相似,谱库检索结果匹配度,排列次序都很接近,检索给出的顺序也不一定正确。但它们的保留时间可能会不同,但保留时间只能在特定色谱条件下不变,而保留指数在固定相相同下有可比性。虽然在相同的柱子上和相同的色谱条件下,两个不同的化合物的保留指数有可能相同。但两个化合物同时具有相同的保留指数(或保留时间)和相同的质谱图的不可能性极小。虽然保留时间也可以帮助确认,但保留时间会随着柱子使用的不同阶段新旧等因素而变化,但保留指数是和固定相为主要因素的一个值,相对比较固定不变。所以才有保留指数辅助定性更具有优势。在谱库检索的基础上,用保留指数来确认结果。是一种很重要的手段。本篇主要探讨同系物的保留指数推测估算。这在知道部分同系物的保留指数时候,去推测估算别的同系物里面的化合物的保留指数很有用。有时候可能您正好缺一个标样或以前没有测定过它的保留指数,这时候可能就非常有用。 一、基本概念保留指数retention index或KovatsIndex(RI或KI)概念是由Kovats在1958年提出。是把组分的保留值用两个分别前后靠近它的正构烷烃来标定(这比仅用一个参比物质的相对保留值定向更为精确)。正构烷烃的保留指数规定为等于该烷烃分子中碳原子数的100倍。例如正己烷的RI为600,正庚烷为700,正十五烷为1500.正构烷烃的RI与所用的色谱柱,柱温及其它操作条件无关。保留指数(RI)的计算公式如下:I=100Z+100R(x)-logt’R(z)]/ R(z+1)- logt’R(z)] (恒温分析)式中:t’R为校正保留时间;Z和Z+1分别为目标化合物(X)流出前后的正构烷烃所含碳原子的数目;这里:t’R(z) t’R(x) t’R(z+1), 一般正构烷烃所含碳原子的数目Z大于4.以上的保留指数(RI)的计算只用于恒温分析。对于沸点范围较宽的复杂组分混合物的分析,一般采用程序升温的方法。在程序升温时,组分的保留指数的测定有所不同。两者有差异,需要校正。1963年Van Den Dool 等经过推算(详细的推导过程略)引入线性程序升温保留指数的概念。I[sup]T[/sup]=100Z+100[TR(x)-TR(z)]/[TR(z+1)-TR(z)] (线性程序升温) 式中:TR(x),TR(z),TR(z+1)分别代表组分及碳数为Z,Z+1正构烷的保留温度。且TR(z)
[align=center][b]保留指数应用(14)----直链脂肪酸乙酯计算保留指数2(非极性柱子)[/b][/align][b] [/b]保留指数作为[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]定性一个强有力的辅助手段,在天然香精油,香气香味材料,香精产品等的分析鉴定中广泛应用。当然应用范围远不止这些。对于异构体,同系物和结构特征相似的化合物,由于其质谱图非常相似,谱库检索结果匹配度,排列次序都很接近,检索给出的顺序也不一定正确。但它们的保留时间可能会不同,但保留时间只能在特定色谱条件下不变,而保留指数在固定相相同下有可比性。虽然在相同的柱子上和相同的色谱条件下,两个不同的化合物的保留指数有可能相同。但两个化合物同时具有相同的保留指数(或保留时间)和相同的质谱图的不可能性极小。虽然保留时间也可以帮助确认,但保留时间会随着柱子使用的不同阶段新旧等因素而变化,但保留指数是和固定相为主要因素的一个值,相对比较固定不变。所以才有保留指数辅助定性更具有优势。在谱库检索的基础上,用保留指数来确认结果。是一种很重要的手段。前面三篇分别探讨了利用直链饱和脂肪酸甲酯(FAME,Fat AcidMethyl Ester)计算极性和非极性柱子计算保留指数,以及利用直链脂肪酸乙酯计算极性柱子的保留指数的相关问题。本篇主要探讨利用直链脂肪酸乙酯(FAEE, Fat Acid Ethyl Ester)来计算非极性柱子的保留指数。并讨论和用正构烷烃计算保留指数的区别和相关性。 附:保留指数基本概念保留指数retention index或KovatsIndex(RI或KI)概念是由Kovats在1958年提出。是把组分的保留值用两个分别前后靠近它的正构烷烃来标定(这比仅用一个参比物质的相对保留值定向更为精确)。正构烷烃的保留指数规定为等于该烷烃分子中碳原子数的100倍。例如正己烷的RI为600,正庚烷为700,正十五烷为1500.正构烷烃的RI与所用的色谱柱,柱温及其它操作条件无关。保留指数(RI)的计算公式如下:I=100Z+100[logt’[sub]R(x)[/sub]-logt’[sub]R(z)[/sub]]/ [logt’[sub]R(z+1)[/sub]- logt’[sub]R(z)[/sub]] (恒温分析) (1)式中:t’[sub]R[/sub]为校正保留时间 Z和Z+1分别为目标化合物(X)流出前后的正构烷烃所含碳原子的数目 这里:t’[sub]R(z)[/sub] t’[sub]R(x)[/sub] t’[sub]R(z+1)[/sub], 一般正构烷烃所含碳原子的数目Z大于4.以上的保留指数(RI)的计算只用于恒温分析。对于沸点范围较宽的复杂组分混合物的分析,一般采用程序升温的方法。在程序升温时,组分的保留指数的测定有所不同。两者有差异,需要校正。1963年Van Den Dool 等经过推算(详细的推导过程略)引入线性程序升温保留指数的概念。I[sup]T[/sup]=100Z+100[T[sub]R(x)[/sub]-T[sub]R(z)[/sub]]/[T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]] (线性程序升温) (2) 式中:T[sub]R(x)[/sub][sub],[/sub]T[sub]R(z)[/sub][sub],[/sub]T[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留温度。且T[sub]R(z)[/sub]T[sub]R(x)[/sub]T[sub]R(z+1)[/sub][sub]。[/sub][sub] [/sub] 一般讲,保留温度的测量比保留时间的测定要麻烦一点。由于保留温度和保留时间通常具有高度的相关性,所以用保留时间代替上式中的保留温度来进行计算保留指数。I[sup]RT[/sup]=100Z+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/[RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]] (线性程序升温) (3)式中:RT[sub]R(x)[/sub][sub],[/sub]RT[sub]R(z)[/sub][sub],[/sub]RT[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留时间。且RT[sub]R(z)[/sub]RT[sub]R(x)[/sub]RT[sub]R(z+1)[/sub][sub]。[/sub][b]保留指数与保留时间的转换[/b]从I[sup]T[/sup]=100Z+100[T[sub]R(x)[/sub]-T[sub]R(z)[/sub]]/ [T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]](3)式可以导出:T[sub]R(x)[/sub]= [I[sup]T[/sup]-100Z]*[T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]]/100+T[sub]R(z) [/sub](4)[sub] [/sub][align=center][b](14)直链饱和脂肪酸乙酯(FAEE)计算保留指数2(非极性柱子)[/b][/align]一般是使用正构烷烃来计算化合物的保留指数,但也有人使用直链饱和脂肪酸甲酯或乙酯及某些系列化合物(例如苯系列等)来计算保留指数。脂肪酸乙酯很常见,可能更容易得到。如果使用直链饱和脂肪酸乙酯(FAEE)计算保留指数,把公式(3)改成I[sup]RT[/sup]=100Z+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/[RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]] (线性程序升温) (5)式中:RT[sub]R(x)[/sub][sub],[/sub]RT[sub]R(z)[/sub][sub],[/sub]RT[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1的直链饱和脂肪酸乙酯保留时间。且RT[sub]R(z)[/sub] RT[sub]R(x)[/sub]RT[sub]R(z+1)[/sub][sub]。[/sub]或者:I[sup]RT[/sup]=100(Z+N)+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/ [RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]](线性程序升温) (6)式中:N为调整的碳数(为了和正构烷计算保留指数校正对应)[b]1试验部分[/b]1.1 仪器与装置美国安捷伦6890N/5973I[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱联用仪。1.2样品和标样、试剂所用香气化合物标准品均来自Sigma-Aldrich等主要试剂公司,少数为实验室内部精制标样。C6-C24正构烷混合标准物来自上海安谱,直链饱和脂肪酸乙酯标品来自上海甄准。TBME来自安谱。1.3 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/MS条件1.3.1 色谱条件:色谱柱:HP-Innowax (60m×0. 25 mm ( i.d.)×0.25μm)毛细管柱;升温程序: 60℃保持0 min,以3 ℃/min升至250℃,保持26 min;载气(He, 纯度99.999%以上)流速1.9 mL/min 进样口温度250℃,分流进样,分流比20:1,进样量1ul;1.3.2质谱条件: 电子轰击(EI)离子源;电子能量70eV;传输线温度280℃;离子源温度230℃;四级杆温度150℃。SCAN扫描范围:29-400。EMV:1655V。1.4 标样配制正构烷混合标准混合物,直链饱和脂肪酸乙酯标准混合物和香气化合物化合物标准稀释配制在TBME中,约0.1%浓度。[b]2 结果与讨论[/b]采用正构烷保留时间和利用公式(5)和(6)计算脂肪酸乙酯(FAEE)保留指数(正构烷形式),结果如表1。[align=center]表1 正构烷和直链饱和脂肪酸乙酯(FAEE)测定的保留时间和其保留指数对照表[/align][align=center](非极性柱子)[/align][align=left][table=620][tr][td=4,1]正构烷保留指数[/td][td=6,1]直链饱和脂肪酸乙酯(FEMA)非极性柱子保留指数[/td][/tr][tr][td]保留时间[/td][td]定义保留指数[/td][td]保留时间[/td][td]定义保留指数[/td][td]校正定义保留指数[/td][td]正构烷计算的保留指数[/td][/tr][tr][td]正构烷[/td][td]正构烷碳数[/td][td]RT(min)[/td][td]RI[/td][td]FAEE[/td][td]FEMA碳数[/td][td]RT(min)[/td][td]Rifaee (N=1)[/td][td]RIfaee_c (N=1.8)[/td][td]RIa[/td][/tr][tr][td]正庚烷[/td][td]7[/td][td]2.258[/td][td]700[/td][td]丁酸乙酯[/td][td]6[/td][td]2.924 [/td][td]600[/td][td]780[/td][td]785[/td][/tr][tr][td]正辛烷[/td][td]8[/td][td]3.061[/td][td]800[/td][td]戊酸乙酯[/td][td]7[/td][td]4.260 [/td][td]700[/td][td]880[/td][td]888[/td][/tr][tr][td]正壬烷[/td][td]9[/td][td]4.442[/td][td]900[/td][td]己酸乙酯[/td][td]8[/td][td]6.141 [/td][td]800[/td][td]980[/td][td]986[/td][/tr][tr][td]正癸烷[/td][td]10[/td][td]6.437[/td][td]1000[/td][td]庚酸乙酯[/td][td]9[/td][td]8.416 [/td][td]900[/td][td]1080[/td][td]1082[/td][/tr][tr][td]碳11烷[/td][td]11[/td][td]8.866[/td][td]1100[/td][td]辛酸乙酯[/td][td]10[/td][td]11.026 [/td][td]1000[/td][td]1180[/td][td]1183[/td][/tr][tr][td]碳12烷[/td][td]12[/td][td]11.483[/td][td]1200[/td][td]壬酸乙酯[/td][td]11[/td][td]13.626 [/td][td]1100[/td][td]1280[/td][td]1282[/td][/tr][tr][td]碳13烷[/td][td]13[/td][td]14.113[/td][td]1300[/td][td]癸酸乙酯[/td][td]12[/td][td]16.093 [/td][td]1200[/td][td]1380[/td][td]1378[/td][/tr][tr][td]碳14烷[/td][td]14[/td][td]16.688[/td][td]1400[/td][td]碳11酸乙酯[/td][td]13[/td][td]18.612 [/td][td]1300[/td][td]1480[/td][td]1480[/td][/tr][tr][td]碳15烷[/td][td]15[/td][td]19.114[/td][td]1500[/td][td]碳12酸乙酯[/td][td]14[/td][td]20.965 [/td][td]1400[/td][td]1580[/td][td]1580[/td][/tr][tr][td]碳16烷[/td][td]16[/td][td]21.442[/td][td]1600[/td][td]碳13酸乙酯[/td][td]15[/td][td]23.160 [/td][td]1500[/td][td]1680[/td][td]1678[/td][/tr][tr][td]碳17烷[/td][td]17[/td][td]23.658[/td][td]1700[/td][td]碳14酸乙酯[/td][td]16[/td][td]25.292 [/td][td]1600[/td][td]1780[/td][td]1778[/td][/tr][tr][td]碳18烷[/td][td]18[/td][td]25.767[/td][td]1800[/td][td]碳15酸乙酯[/td][td]17[/td][td]27.305 [/td][td]1700[/td][td]1880[/td][td]1877[/td][/tr][tr][td]碳19烷[/td][td]19[/td][td]27.777[/td][td]1900[/td][td]碳16酸乙酯[/td][td]18[/td][td]28.074 [/td][td]1800[/td][td]1980[/td][td]1976[/td][/tr][tr][td]碳20烷[/td][td]20[/td][td]29.695[/td][td]2000[/td][td]碳17酸乙酯[/td][td]19[/td][td]31.152 [/td][td]1900[/td][td]2080[/td][td]2080[/td][/tr][tr][td]碳21烷[/td][td]21[/td][td]31.529[/td][td]2100[/td][td]碳18酸乙酯[/td][td]20[/td][td]32.905 [/td][td]2000[/td][td]2180[/td][td]2179[/td][/tr][tr][td]碳22烷[/td][td]22[/td][td]32.282[/td][td]2200[/td][td] [/td][td] [/td][td] [/td][td] [/td][td] [/td][td] [/td][td] [/td][/tr][/table] [/align][align=left]2.1正构烷和直链饱和脂肪酸乙酯测定的非极性柱子的保留时间和其保留指数对比2.1.1从上面的表可以看出,在线性程序升温时候,直链饱和脂肪酸乙酯化合物的非极性柱子保留时间也是基本随碳数等距离增加,和正构烷的出峰时间的趋势一样。2.1.2直链饱和脂肪酸乙酯化合物的非极性柱子保留时间和正构烷保留时间的碳数差不多相差1-2。[b][u]而不是脂肪酸甲酯的整数值。也不是极性柱子的碳数相差4-5。[/u][/b]2.1.3直链饱和脂肪酸乙酯化合物的非极性柱子保留指数加约180和相同碳数的正构烷保留指数很接近。[b][u]不是极性柱子保留指数加约440和相同碳数的正构烷保留指数很接近。也不是直链饱和脂肪酸甲酯化合物的非极性柱子的保留指数加500和相同碳数的正构烷保留指数很接近的情况。[/u][/b]****************************************************************************2.2 部分挥发性香气化合物乙酸酯的非极性柱子保留指数举例用公式(3),(5)和(6)来计算部分挥发性香气化合物保留指数。[/align][align=center]表2部分挥发性香气化合物乙酸酯的非极性柱子保留指数举例[/align][table=520][tr][td]保留时间[/td][td]正构烷计算保留指数[/td][td]FEMA计算保留指数[/td][td]FEMA计算校正保留指数[/td][/tr][tr][td]化合物名称[/td][td]RT(min)[/td][td]RI[/td][td]Rifaee (N=1)[/td][td]RIfaee_c (N=1.8)[/td][/tr][tr][td]butyl acetate[/td][td]3.043[/td][td]800[/td][td]609[/td][td]789[/td][/tr][tr][td]Hexanol[/td][td]3.804[/td][td]855[/td][td]666[/td][td]846[/td][/tr][tr][td]alpha-pinene[/td][td]5.124[/td][td]935[/td][td]765[/td][td]945[/td][/tr][tr][td]ehthyl capronoate[/td][td]5.323[/td][td]945[/td][td]757[/td][td]937[/td][/tr][tr][td]benzyl alcohol[/td][td]6.712[/td][td]1012[/td][td]825[/td][td]1005[/td][/tr][tr][td]Limonene[/td][td]6.931[/td][td]1021[/td][td]835[/td][td]1015[/td][/tr][tr][td]gamma-terpinene[/td][td]7.759[/td][td]1055[/td][td]871[/td][td]1051[/td][/tr][tr][td]Linalool[/td][td]8.440 [/td][td]1083[/td][td]901[/td][td]1081[/td][/tr][tr][td]PEA[/td][td]8.586[/td][td]1089[/td][td]907[/td][td]1087[/td][/tr][tr][td]methyl salicylate[/td][td]10.528[/td][td]1164[/td][td]881[/td][td]1061[/td][/tr][tr][td]geranial[/td][td]12.680 [/td][td]1246[/td][td]1064[/td][td]1244[/td][/tr][tr][td]Triactin[/td][td]14.509[/td][td]1316[/td][td]1136[/td][td]1316[/td][/tr][tr][td]Caroyphenen[/td][td]16.875[/td][td]1409[/td][td]1231[/td][td]1411[/td][/tr][tr][td]amyl cinnamic aldehyde[/td][td]22.318[/td][td]1640[/td][td]1461[/td][td]1641[/td][/tr][tr][td]Tonalide[/td][td]26.661[/td][td]1845[/td][td]1667[/td][td]1847[/td][/tr][tr][td]Benzyl Cinnamate[/td][td]30.638[/td][td]2052[/td][td]1883[/td][td]2063[/td][/tr][/table]从表2看出,直链饱和脂肪酸乙酯计算挥发性香气化合物的非极性柱子的保留指数加约[b][u]18[/u][/b]0(FAEE校正保留指数,[b][u]N=1.8[/u][/b])和相同碳数的正构烷保留指数很接近。[b][u]而不是极性柱子的保留指数加440(FAEE校正保留指数,N=4.4)和相同碳数的正构烷保留指数很接近。比极性柱子的乙酯计算的保留指数值偏差小一些。[/u][/b]在实际应用中可以考虑相互参照参考或甚至相互代用。
保留指数应用----同系物保留指数推测估算1 保留指数作为气质定性一个强有力的辅助手段,在天然香精油,香气香味材料,香精产品等的分析鉴定中广泛应用。当然应用范围远不止这些。对于异构体,同系物和结构特征相似的化合物,由于其质谱图非常相似,谱库检索结果匹配度,排列次序都很接近,检索给出的顺序也不一定正确。但它们的保留时间可能会不同,但保留时间只能在特定色谱条件下不变,而保留指数在固定相相同下有可比性。虽然在相同的柱子上和相同的色谱条件下,两个不同的化合物的保留指数有可能相同。但两个化合物同时具有相同的保留指数(或保留时间)和相同的质谱图的不可能性极小。虽然保留时间也可以帮助确认,但保留时间会随着柱子使用的不同阶段新旧等因素而变化,但保留指数是和固定相为主要因素的一个值,相对比较固定不变。所以才有保留指数辅助定性更具有优势。在谱库检索的基础上,用保留指数来确认结果。是一种很重要的手段。本篇主要探讨同系物的保留指数推测估算。这在知道部分同系物的保留指数时候,去推测估算别的同系物里面的化合物的保留指数很有用。有时候可能您正好缺一个标样或以前没有测定过它的保留指数,这时候可能就非常有用。 一、基本概念保留指数retention index或KovatsIndex(RI或KI)概念是由Kovats在1958年提出。是把组分的保留值用两个分别前后靠近它的正构烷烃来标定(这比仅用一个参比物质的相对保留值定向更为精确)。正构烷烃的保留指数规定为等于该烷烃分子中碳原子数的100倍。例如正己烷的RI为600,正庚烷为700,正十五烷为1500.正构烷烃的RI与所用的色谱柱,柱温及其它操作条件无关。保留指数(RI)的计算公式如下:I=100Z+100R(x)-logt’R(z)]/ R(z+1)- logt’R(z)] (恒温分析)式中:t’R为校正保留时间;Z和Z+1分别为目标化合物(X)流出前后的正构烷烃所含碳原子的数目;这里:t’R(z) t’R(x) t’R(z+1), 一般正构烷烃所含碳原子的数目Z大于4.以上的保留指数(RI)的计算只用于恒温分析。对于沸点范围较宽的复杂组分混合物的分析,一般采用程序升温的方法。在程序升温时,组分的保留指数的测定有所不同。两者有差异,需要校正。1963年Van Den Dool 等经过推算(详细的推导过程略)引入线性程序升温保留指数的概念。I[sup]T[/sup]=100Z+100[TR(x)-TR(z)]/[TR(z+1)-TR(z)] (线性程序升温) 式中:TR(x),TR(z),TR(z+1)分别代表组分及碳数为Z,Z+1正构烷的保留温度。且TR(z)
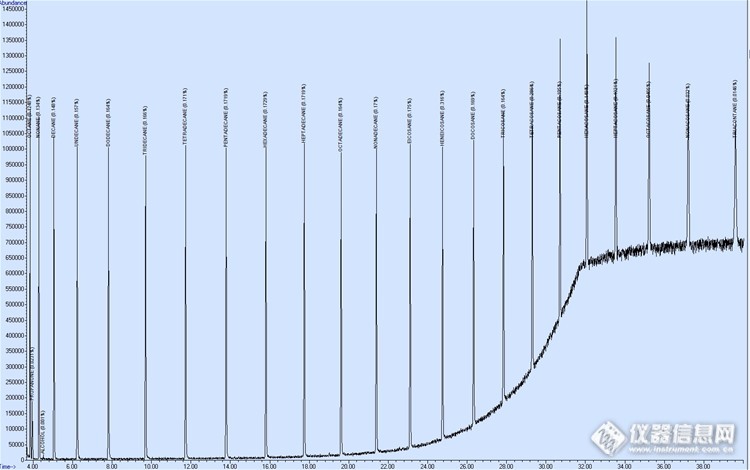
保留指数应用--不同升温速率对保留指数影响小观察 保留指数作为气质定性一个强有力的辅助手段,在天然香精油,香气香味材料,香精产品等的分析鉴定中广泛应用。当然应用范围远不止这些。对于异构体,同系物和结构特征相似的化合物,由于其质谱图非常相似,谱库检索结果匹配度,排列次序都很接近,检索给出的顺序也不一定正确。但它们的保留时间可能会不同,但保留时间只能在特定色谱条件下不变,而保留指数在固定相相同下有可比性。虽然在相同的柱子上和相同的色谱条件下,两个不同的化合物的保留指数有可能相同。但两个化合物同时具有相同的保留指数(或保留时间)和相同的质谱图的不可能性极小。虽然保留时间也可以帮助确认,但保留时间会随着柱子使用的不同阶段新旧等因素而变化,但保留指数是和固定相为主要因素的一个值,相对比较固定不变。所以才有保留指数辅助定性更具有优势。在谱库检索的基础上,用保留指数来确认结果。是一种很重要的手段。本篇主要是粗略考察程序升温的升温速率对保留指数影响。 (附:基本概念保留指数retention index或KovatsIndex(RI或KI)概念是由Kovats在1958年提出。是把组分的保留值用两个分别前后靠近它的正构烷烃来标定(这比仅用一个参比物质的相对保留值定向更为精确)。正构烷烃的保留指数规定为等于该烷烃分子中碳原子数的100倍。例如正己烷的RI为600,正庚烷为700,正十五烷为1500.正构烷烃的RI与所用的色谱柱,柱温及其它操作条件无关。)1 试验部分1.1 仪器与装置美国安捷伦6890N/5975C气相色谱-质谱联用仪,带有德国Gerstel的MPS2多功能自动进样系统。1.2标样市场样品。所有香气化合物标准品均来自Sigma-Aldrich等主要试剂公司,少数为实验室内部精制标样。C7-C30正构烷烃来自安谱公司。均配成0.05-0.1%的特丁基甲醚稀释液,正构烷为0.05%的正戊烷溶液。1.3GC/MS条件1.3.1 色谱条件:色谱柱:安捷伦HP-Innowax(60m×0. 25 mm( i.d.)×0.25μm)毛细管柱;升温程序: 60℃,以3 ℃/min或6℃/min升至250℃,保持一定时间至所以组分流出;载气(He,纯度99.999%以上)流速1.8 mL/min;进样口温度250℃,分流进样,分流比100:1;进样量:1μl。1.3.2质谱条件:电子轰击(EI)离子源;电子能量70eV;传输线温度280℃;离子源温度230℃;四级杆温度150℃,EMV:1378V。SCAN扫描范围:29-400。**************2. 分析结果及讨论2.1 正构烷标样结果在上述1.3的相同条件下,进C7-C30正构烷烃标样,得到其保留时间,用于计算其它化合物的保留指数。http://ng1.17img.cn/bbsfiles/images/2016/10/201610272221_615272_0_3.jpg图1 60℃,以3 ℃/min升至250℃的正构烷总离子色谱图TIC表1. 60℃,以3 ℃/min升至250℃的正构烷数据表:正构烷名称RIRT(min)HEPTANE7003.623CYCLOHEXANE7573.723OCTANE8003.938PROPANONE8104.078NONANE9004.505DECANE10005.536UNDECANE11007.256DODECANE12009.786TRIDECANE130013.033TETRADECANE140016.737PENTADECANE150020.627HEXADECANE160024.522HEPTADECANE170028.318OCTADECANE180031.977NONADECANE190035.493EICOSANE200038.858HENEICOSANE210042.088DOCOSANE220045.190TRICOSANE230048.172TETRACOSANE240051.041PENTACOSANE250053.807HEXACOSANE260056.481HEPTACOSANE270059.050OCTACOSANE280061.548NONACOSANE290063.973TRIACONTANE300066.661http://ng1.17img.cn/bbsfiles/images/2016/10/201610272221_615272_0_3.jpg图2 60℃,以6℃/min升至250℃正构烷总离子色谱图TIC表2. 60℃,以6 ℃/min升至250℃的正构烷数据表:正构烷名称RIRT(min)OCTANE8003.846PROPANONE8103.963NONANE9004.295ALCOHOL9344.522DECANE10005.061UNDECANE11006.239DODECANE12007.825TRIDECANE13009.706TETRADECANE140011.733PENTADECANE150013.788HEXADECANE160015.804HEPTADECANE170017.748OCTADECANE180019.614NONADECANE190021.401EICOSANE200023.116HENEICOSANE210024.756DOCOSANE[/
[align=center][b]保留指数应用(13)----直链脂肪酸乙酯计算保留指数1(极性柱子)[/b][/align][b] [/b]保留指数作为[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]定性一个强有力的辅助手段,在天然香精油,香气香味材料,香精产品等的分析鉴定中广泛应用。当然应用范围远不止这些。对于异构体,同系物和结构特征相似的化合物,由于其质谱图非常相似,谱库检索结果匹配度,排列次序都很接近,检索给出的顺序也不一定正确。但它们的保留时间可能会不同,但保留时间只能在特定色谱条件下不变,而保留指数在固定相相同下有可比性。虽然在相同的柱子上和相同的色谱条件下,两个不同的化合物的保留指数有可能相同。但两个化合物同时具有相同的保留指数(或保留时间)和相同的质谱图的不可能性极小。虽然保留时间也可以帮助确认,但保留时间会随着柱子使用的不同阶段新旧等因素而变化,但保留指数是和固定相为主要因素的一个值,相对比较固定不变。所以才有保留指数辅助定性更具有优势。在谱库检索的基础上,用保留指数来确认结果。是一种很重要的手段。前面两篇探讨了利用直链饱和脂肪酸甲酯(FAME)计算保留指数的相关问题。本篇主要探讨利用直链脂肪酸乙酯(FAEE, Fat Acid Ethyl Ester)来计算保留指数。并讨论和用正构烷烃计算保留指数的区别和相关性。 附:保留指数基本概念保留指数retention index或KovatsIndex(RI或KI)概念是由Kovats在1958年提出。是把组分的保留值用两个分别前后靠近它的正构烷烃来标定(这比仅用一个参比物质的相对保留值定向更为精确)。正构烷烃的保留指数规定为等于该烷烃分子中碳原子数的100倍。例如正己烷的RI为600,正庚烷为700,正十五烷为1500.正构烷烃的RI与所用的色谱柱,柱温及其它操作条件无关。保留指数(RI)的计算公式如下:I=100Z+100[logt’[sub]R(x)[/sub]-logt’[sub]R(z)[/sub]]/ [logt’[sub]R(z+1)[/sub]- logt’[sub]R(z)[/sub]] (恒温分析) (1)式中:t’[sub]R[/sub]为校正保留时间 Z和Z+1分别为目标化合物(X)流出前后的正构烷烃所含碳原子的数目 这里:t’[sub]R(z)[/sub] t’[sub]R(x)[/sub] t’[sub]R(z+1)[/sub], 一般正构烷烃所含碳原子的数目Z大于4.以上的保留指数(RI)的计算只用于恒温分析。对于沸点范围较宽的复杂组分混合物的分析,一般采用程序升温的方法。在程序升温时,组分的保留指数的测定有所不同。两者有差异,需要校正。1963年Van Den Dool 等经过推算(详细的推导过程略)引入线性程序升温保留指数的概念。I[sup]T[/sup]=100Z+100[T[sub]R(x)[/sub]-T[sub]R(z)[/sub]]/[T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]] (线性程序升温) (2) 式中:T[sub]R(x)[/sub][sub],[/sub]T[sub]R(z)[/sub][sub],[/sub]T[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留温度。且T[sub]R(z)[/sub]T[sub]R(x)[/sub]T[sub]R(z+1)[/sub][sub]。[/sub][sub] [/sub] 一般讲,保留温度的测量比保留时间的测定要麻烦一点。由于保留温度和保留时间通常具有高度的相关性,所以用保留时间代替上式中的保留温度来进行计算保留指数。I[sup]RT[/sup]=100Z+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/[RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]] (线性程序升温) (3)式中:RT[sub]R(x)[/sub][sub],[/sub]RT[sub]R(z)[/sub][sub],[/sub]RT[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留时间。且RT[sub]R(z)[/sub]RT[sub]R(x)[/sub]RT[sub]R(z+1)[/sub][sub]。[/sub][b]保留指数与保留时间的转换[/b]从I[sup]T[/sup]=100Z+100[T[sub]R(x)[/sub]-T[sub]R(z)[/sub]]/ [T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]](3)式可以导出:T[sub]R(x)[/sub]= [I[sup]T[/sup]-100Z]*[T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]]/100+T[sub]R(z) [/sub](4)[sub] [/sub][align=center][b](13)直链饱和脂肪酸乙酯(FAEE)计算保留指数1(极性柱子)[/b][/align]一般是使用正构烷烃来计算化合物的保留指数,但也有人使用直链饱和脂肪酸甲酯或乙酯及某些系列化合物(例如苯系列等)来计算保留指数。脂肪酸乙酯很常见,可能更容易得到。如果使用直链饱和脂肪酸乙酯(FAEE)计算保留指数,把公式(3)改成I[sup]RT[/sup]=100Z+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/[RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]] (线性程序升温) (5)式中:RT[sub]R(x)[/sub][sub],[/sub]RT[sub]R(z)[/sub][sub],[/sub]RT[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1的直链饱和脂肪酸乙酯保留时间。且RT[sub]R(z)[/sub] RT[sub]R(x)[/sub]RT[sub]R(z+1)[/sub][sub]。[/sub]或者:I[sup]RT[/sup]=100(Z+N)+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/ [RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]](线性程序升温) (6)式中:N为调整的碳数(为了和正构烷计算保留指数校正对应)[b]1试验部分[/b]1.1 仪器与装置美国安捷伦6890N/5973I[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱联用仪。1.2样品和标样、试剂所用香气化合物标准品均来自Sigma-Aldrich等主要试剂公司,少数为实验室内部精制标样。C6-C24正构烷混合标准物来自上海安谱,直链饱和脂肪酸乙酯标品来自上海甄准。TBME来自安谱。1.3 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/MS条件1.3.1 色谱条件:色谱柱:HP-Innowax (60m×0. 25 mm ( i.d.)×0.25μm)毛细管柱;升温程序: 60℃保持0 min,以3 ℃/min升至250℃,保持26 min;载气(He, 纯度99.999%以上)流速1.9 mL/min 进样口温度250℃,分流进样,分流比20:1,进样量1ul;1.3.2质谱条件: 电子轰击(EI)离子源;电子能量70eV;传输线温度280℃;离子源温度230℃;四级杆温度150℃。SCAN扫描范围:29-400。EMV:1655V。1.4 标样配制正构烷混合标准混合物,直链饱和脂肪酸乙酯标准混合物和香气化合物化合物标准稀释配制在TBME中,约0.1%浓度。[b]2 结果与讨论[/b]采用正构烷保留时间和利用公式(5)和(6)计算脂肪酸乙酯(FAEE)保留指数(正构烷形式),结果如表1。[align=center]表1 正构烷和直链饱和脂肪酸乙酯(FAEE)测定的保留时间和其保留指数对照表[/align][table=619][tr][td=4,1]正构烷保留指数[/td][td=6,1]直链饱和脂肪酸乙酯(FAEE)保留指数[/td][/tr][tr][td]保留时间[/td][td]定义保留指数[/td][td]保留时间[/td][td]定义保留指数[/td][td]校正定义保留指数[/td][td]正构烷计算的保留指数[/td][/tr][tr][td]正构烷[/td][td]正构烷碳数[/td][td]RT(min)[/td][td]RI[/td][td]FAEE[/td][td]FAEE碳数[/td][td]RT(min)[/td][td]RIfaee[/td][td]RIfaee_c (N=4.4)[/td][td]RIa[/td][/tr][tr][td]正辛烷[/td][td]8[/td][td]4.112[/td][td]800[/td][td]乙酸乙酯[/td][td]4[/td][td]4.631[/td][td]400[/td][td]840[/td][td]881[/td][/tr][tr][td]正壬烷[/td][td]9[/td][td]4.76[/td][td]900[/td][td]丙酸乙酯[/td][td]5[/td][td]5.457[/td][td]500[/td][td]940[/td][td]960[/td][/tr][tr][td]正癸烷[/td][td]10[/td][td]5.92[/td][td]1000[/td][td]丁酸乙酯[/td][td]6[/td][td]6.582[/td][td]600[/td][td]1040[/td][td]1035[/td][/tr][tr][td]碳11烷[/td][td]11[/td][td]7.811[/td][td]1100[/td][td]戊酸乙酯[/td][td]7[/td][td]8.541[/td][td]700[/td][td]1140[/td][td]1127[/td][/tr][tr][td]碳12烷[/td][td]12[/td][td]10.515[/td][td]1200[/td][td]己酸乙酯[/td][td]8[/td][td]12.034[/td][td]800[/td][td]1240[/td][td]1245[/td][/tr][tr][td]碳13烷[/td][td]13[/td][td]13.89[/td][td]1300[/td][td]庚酸乙酯[/td][td]9[/td][td]15.059[/td][td]900[/td][td]1340[/td][td]1331[/td][/tr][tr][td]碳14烷[/td][td]14[/td][td]17.659[/td][td]1400[/td][td]辛酸乙酯[/td][td]10[/td][td]19.265[/td][td]1000[/td][td]1440[/td][td]1441[/td][/tr][tr][td]碳15烷[/td][td]15[/td][td]21.575[/td][td]1500[/td][td]壬酸乙酯[/td][td]11[/td][td]22.432[/td][td]1100[/td][td]1540[/td][td]1522[/td][/tr][tr][td]碳16烷[/td][td]16[/td][td]25.369[/td][td]1600[/td][td]癸酸乙酯[/td][td]12[/td][td]26.683[/td][td]1200[/td][td]1640[/td][td]1632[/td][/tr][tr][td]碳17烷[/td][td]17[/td][td]29.263[/td][td]1700[/td][td]碳11酸乙酯[/td][td]13[/td][td]30.723[/td][td]1300[/td][td]1740[/td][td]1740[/td][/tr][tr][td]碳18烷[/td][td]18[/td][td]32.914[/td][td]1800[/td][td]碳12酸乙酯[/td][td]14[/td][td]34.141[/td][td]1400[/td][td]1840[/td][td]1835[/td][/tr][tr][td]碳19烷[/td][td]19[/td][td]36.421[/td][td]1900[/td][td]碳13酸乙酯[/td][td]15[/td][td]37.765[/td][td]1500[/td][td]1940[/td][td]1940[/td][/tr][tr][td]碳20烷[/td][td]20[/td][td]39.78[/td][td]2000[/td][td]碳14酸乙酯[/td][td]16[/td][td]41.099[/td][td]1600[/td][td]2040[/td][td]2041[/td][/tr][tr][td]碳21烷[/td][td]21[/td][td]42.996[/td][td]2100[/td][td]碳15酸乙酯[/td][td]17[/td][td]44.418[/td][td]1700[/td][td]2140[/td][td]2146[/td][/tr][tr][td]碳22烷[/td][td]22[/td][td]46.086[/td][td]2200[/td][td]碳16酸乙酯[/td][td]18[/td][td]48.758[/td][td]1800[/td][td]2240[/td][td]2250[/td][/tr][tr][td]碳23烷[/td][td]23[/td][td]49.055[/td][td]2300[/td][td]碳17酸乙酯[/td][td]19[/td][td]50.623[/td][td]1900[/td][td]2340[/td][td]2355[/td][/tr][tr][td]碳24烷[/td][td]24[/td][td]51.906[/td][td]2400[/td][td]碳18酸乙酯[/td][td]20[/td][td]53.551[/td][td]2000[/td][td]840[/td][td]2460[/td][/tr][tr][td] [/td][td] [/td][td] [/td][td] [/td][/tr][/table]2.1正构烷和直链饱和脂肪酸乙酯测定的保留时间和其保留指数对比2.1.1从上面的表可以看出,在线性程序升温时候,直链饱和脂肪酸乙酯化合物的保留时间也是基本随碳数等距离增加,和正构烷的出峰时间的趋势一样。2.1.2直链饱和脂肪酸乙酯化合物的保留时间和正构烷保留时间的碳数差不多相差4-5。[b][u]而不是脂肪酸甲酯的整数值。[/u][/b]2.1.3直链饱和脂肪酸乙酯化合物的保留指数加440和相同碳数的正构烷保留指数很接近。[b][u]而不是直链饱和脂肪酸甲酯化合物的保留指数加500和相同碳数的正构烷保留指数很接近的情况。[/u][/b]****************************************************************************2.2 部分挥发性香气化合物保留指数举例用公式(3),(5)和(6)来计算部分挥发性香气化合物保留指数。[table=520][tr][td]保留时间[/td][td]正构烷计算保留指数[/td][td]FAEE计算保留指数[/td][td]FEMA计算校正保留指数[/td][/tr][tr][td]化合物名称[/td][td]RT(min)[/td][td]RI[/td][td]RIfaee[/td][td]RIfaee_c (N=4.4)[/td][/tr][tr][td]ethyl acetate[/td][td]4.631[/td][td]881[/td][td]400[/td][td]840[/td][/tr][tr][td]Ethanol[/td][td]5.166[/td][td]935[/td][td]495[/td][td]905[/td][/tr][tr][td]alpha-pinene[/td][td]6.526[/td][td]1032[/td][td]595[/td][td]1035[/td][/tr][tr][td]butyl acetate[/td][td]6.658[/td][td]1039[/td][td]604[/td][td]1044[/td][/tr][tr][td]Limonene[/td][td]10.515[/td][td]1200[/td][td]757[/td][td]1197[/td][/tr][tr][td]isoamyl alcohol[/td][td]10.852[/td][td]1210[/td][td]766[/td][td]1206[/td][/tr][tr][td]ehthyl capronoate[/td][td]12.034[/td][td]1245[/td][td]805[/td][td]1245[/td][/tr][tr][td]Hexanol[/td][td]16.001[/td][td]1356[/td][td]822[/td][td]1362[/td][/tr][tr][td]Linalool[/td][td]23.483[/td][td]1549[/td][td]1125[/td][td]1565[/td][/tr][tr][td]PG[/td][td]24.729[/td][td]1581[/td][td]1154[/td][td]1593[/td][/tr][tr][td]Caroyphenen[/td][td]24.924[/td][td]1586[/td][td]1158[/td][td]1598[/td][/tr][tr][td]methyl salicylate[/td][td]31.271[/td][td]1755[/td][td]1316[/td][td]1756[/td][/tr][tr][td]benzyl alcohol[/td][td]35.999[/td][td]1888[/td][td]1451[/td][td]1891[/td][/tr][tr][td]Triactin[/td][td]41.999[/td][td]2069[/td][td]1627[/td][td]2067[/td][/tr][/table]从表2看出,直链饱和脂肪酸乙酯计算挥发性香气化合物的保留指数加[b][u]44[/u][/b]0(FAEE校正保留指数,[b][u]N=4.4[/u][/b])和相同碳数的正构烷保留指数很接近。在实际应用中可以考虑相互参照参考或甚至相互代用。但乙酸乙酯的保留指数值相差比较大,偏差较大。(下次讨论非极性柱子上面用直链脂肪酸乙酯来计算保留指数。并讨论和用正构烷烃计算保留指数的区别和相关性。)
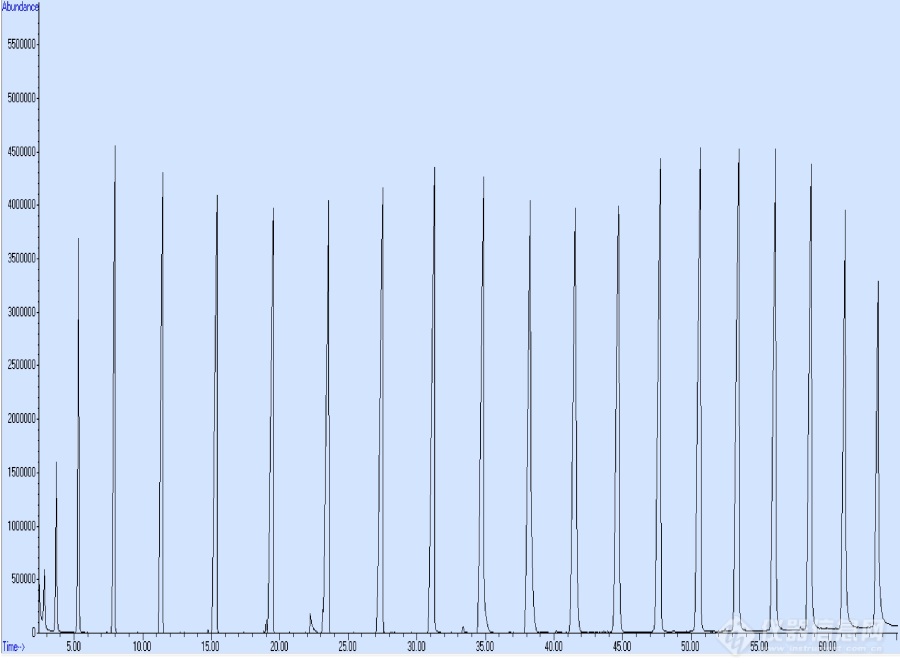
[align=center][b]保留指数应用(15)--固定相差异的保留指数粗略比较[/b][/align][b] [/b]保留指数作为[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]定性一个强有力的辅助手段,在天然香精油,香气香味材料,香精产品等的分析鉴定中广泛应用。当然应用范围远不止这些。对于异构体,同系物和结构特征相似的化合物,由于其质谱图非常相似,谱库检索结果匹配度,排列次序都很接近,检索给出的顺序也不一定正确。但它们的保留时间可能会不同,但保留时间只能在特定色谱条件下不变,而保留指数在固定相相同下有可比性。虽然在相同的柱子上和相同的色谱条件下,两个不同的化合物的保留指数有可能相同。但两个化合物同时具有相同的保留指数(或保留时间)和相同的质谱图的不可能性极小。虽然保留时间也可以帮助确认,但保留时间会随着柱子使用的不同阶段新旧等因素而变化,但保留指数是和固定相为主要因素的一个值,相对比较固定不变。所以才有保留指数辅助定性更具有优势。在谱库检索的基础上,用保留指数来确认结果。是一种很重要的手段。本篇主要是粗略比较固定相差异引起保留指数变化的差异。 附:基本概念保留指数retention index或KovatsIndex(RI或KI)概念是由Kovats在1958年提出。是把组分的保留值用两个分别前后靠近它的正构烷烃来标定(这比仅用一个参比物质的相对保留值定向更为精确)。正构烷烃的保留指数规定为等于该烷烃分子中碳原子数的100倍。例如正己烷的RI为600,正庚烷为700,正十五烷为1500.正构烷烃的RI与所用的色谱柱,柱温及其它操作条件无关。)保留指数(RI)的计算公式如下:I=100Z+100[logt’[sub]R(x)[/sub]- logt’[sub]R(z)[/sub]]/[logt’[sub]R(z+1)[/sub]- logt’[sub]R(z)[/sub]] (恒温分析)式中:t’[sub]R[/sub]为校正保留时间 Z和Z+1分别为目标化合物(X)流出前后的正构烷烃所含碳原子的数目 这里:t’[sub]R(z)[/sub] t’[sub]R(x)[/sub]t’[sub]R(z+1)[/sub], 一般正构烷烃所含碳原子的数目Z大于4.以上的保留指数(RI)的计算只用于恒温分析。对于沸点范围较宽的复杂组分混合物的分析,一般采用程序升温的方法。在程序升温时,组分的保留指数的测定有所不同。两者有差异,需要校正。1963年Van Den Dool 等经过推算(详细的推导过程略)引入线性程序升温保留指数的概念。I[sup]T[/sup]=100Z+100[T[sub]R(x)[/sub]-T[sub]R(z)[/sub]]/[T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]] (线性程序升温) 式中:T[sub]R(x)[/sub][sub],[/sub]T[sub]R(z)[/sub][sub],[/sub]T[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留温度。且T[sub]R(z)[/sub]T[sub]R(x)[/sub]T[sub]R(z+1)[/sub][sub]。[/sub][sub] [/sub] 一般讲,保留温度的测量比保留时间的测定要麻烦一点。由于保留温度和保留时间通常具有高度的相关性,所以用保留时间代替上式中的保留温度来进行计算保留指数。I[sup]RT[/sup]=100Z+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/[RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]] (线性程序升温)式中:RT[sub]R(x)[/sub][sub],[/sub]RT[sub]R(z)[/sub][sub],[/sub]RT[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留温度。且RT[sub]R(z)[/sub]RT[sub]R(x)[/sub]RT[sub]R(z+1)[/sub][sub]。[/sub][b]1 试验部分[/b]1.1 仪器与装置美国安捷伦6890N/5975C[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱联用仪,带有德国Gerstel的MPS2多功能自动进样系统。1.2标样所有香气化合物标准品均来自Sigma-Aldrich等主要试剂公司,少数为实验室内部精制标样。C6-C26正构烷烃来自安谱公司。香气化合物均配成0.05-0.1%的特丁基甲醚稀释液,正构烷为0.05%的正戊烷溶液。1.3 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/MS条件1.3.1 色谱条件:色谱柱:(1)极性柱子:安捷伦HP-Innowax (30m×0.25 mm( i.d.)×0.25μm)毛细管柱和VF-Wax (30m×0. 25 mm( i.d.)×0.25μm)毛细管柱;升温程序: 40℃,以3 ℃/min升至230℃,保持一定时间至所有组分流出;载气(He,纯度99.999%以上),恒流模式:流速1.8 mL/min进样口温度250℃,分流进样,分流比100:1 进样量:1μl。1.3.2质谱条件:电子轰击(EI)离子源;电子能量70eV;传输线温度280℃;离子源温度230℃;四级杆温度150℃,EMV:1428V。SCAN扫描范围:29-400。**************2. 分析结果及讨论2.1 极性柱子恒流模式正构烷标样结果在上述1.3的相同条件下,进C6-C26正构烷烃标样,得到其保留时间,用于计算其它化合物的保留指数。[img=,690,514]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171502470938_7611_1615838_3.jpg!w690x514.jpg[/img]图1 HP-Innowax极性柱子的正构烷(C8-C26)总[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]图TIC[img=,690,514]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171503045225_3984_1615838_3.jpg!w690x514.jpg[/img]图2 VF-WAXms极性柱子的正构烷(C8-C26)总[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]图TIC2.2. 两种极性柱子恒流模式保留指数的对比部分香气化合物的保留指数结果线性程序升温保留指数计算公式:I[sup]RT[/sup]=100Z+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/[RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]] (线性程序升温)式中:RT[sub]R(x)[/sub][sub],[/sub]RT[sub]R(z)[/sub][sub],[/sub]RT[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留温度。且RT[sub]R(z)[/sub] RT[sub]R(x)[/sub]RT[sub]R(z+1)[/sub][sub]。[/sub]用上面的线性程序升温保留指数计算公式来计算部分香气化合物的保留指数如下:表 部分香气化合物的保留指数[table=340][tr][td]No[/td][td]Name[/td][td]HP-Innowax[/td][td]VF-WAXms[/td][/tr][tr][td]1[/td][td]ethyl acetate[/td][td]879[/td][td]879[/td][/tr][tr][td]2[/td][td]myrcene[/td][td]1159[/td][td]1161[/td][/tr][tr][td]3[/td][td]alpha-terpinene[/td][td]1181[/td][td]1176[/td][/tr][tr][td]4[/td][td]limonene[/td][td]1206[/td][td]1198[/td][/tr][tr][td]5[/td][td]eucalyptol[/td][td]1212[/td][td]1206[/td][/tr][tr][td]6[/td][td]gamma-terpinene[/td][td]1246[/td][td]1241[/td][/tr][tr][td]7[/td][td]acetic acid[/td][td]1453[/td][td]1446[/td][/tr][tr][td]8[/td][td]furfural[/td][td]1469[/td][td]1463[/td][/tr][tr][td]9[/td][td]decenal[/td][td]1497[/td][td]1495[/td][/tr][tr][td]10[/td][td]benzaldehyde[/td][td]1530[/td][td]1520[/td][/tr][tr][td]11[/td][td]linalool[/td][td]1543[/td][td]1549[/td][/tr][tr][td]12[/td][td]octanol[/td][td]1564[/td][td]1558[/td][/tr][tr][td]13[/td][td]caryoppyllene[/td][td]1591[/td][td]1584[/td][/tr][tr][td]14[/td][td]acetophenone[/td][td]1653[/td][td]1641[/td][/tr][tr][td]15[/td][td]Neral[/td][td]1680[/td][td]1673[/td][/tr][tr][td]16[/td][td]ethyl maltol[/td][td]2020[/td][td]2015[/td][/tr][tr][td]17[/td][td]triacetin[/td][td]2080[/td][td]2077[/td][/tr][tr][td]18[/td][td]vanillin[/td][td]2556[/td][td]2548[/td][/tr][/table]从上面看出HP-Innowax和VF-WAXms两种极性柱子在恒流模式的保留指数有一些差异,但差异非常小。这种小的差异不影响两种柱子的保留指数的相互替换和使用。这两种柱子的固定相都是PEG20M,但制作工艺和方法可能有所差别,原来属于不同的制造商,后来随合并,但仍然保留原来的制作方法,保留原来的商品名称,都是不错的柱子。在实际使用时候,两者的保留指数可以相互参照或应用。
酸性法高锰酸盐指数用的葡萄糖配的质控练习,碱性法的质控怎么自制?怎么加氯离子?
L.R.Snyder和J.J.Kirkland是谁我想不用我再介绍了吧,本书是两位从事色谱分析顶级专家撰写的一本关于色谱法应用的专属,虽然时间有点老(1988),但是这仍是一本色谱分析工作者必读之书,先上传以供大家交流。当然,现在该书的中文译本也已经有了,是由科学出版社出版,王杰等译,《实用高效液相色谱法的建立》[~86685~]
请问在同一设备,同一色谱柱条件下,不同的升温程序会改变物质的保留指数么?与nist库里的保留指数进行比对,是否在同一色谱柱的条件下,就有参考意义?还是必须在同一升温程序下才有意义?
( 本文只是一种探讨交流,可能有不足不妥之处,欢迎批评指正。未经同意,请勿转载。多谢合作!)保留指数应用(七)保留指数估算(1)----非极性或弱极性柱子上面部分化合物的保留指数的估算保留指数作为气质定性一个强有力的辅助手段,在天然香精油,香气香味材料,香精产品等的分析鉴定中广泛应用。当然应用范围远不止这些。对于异构体,同系物和结构特征相似的化合物,由于其质谱图非常相似,谱库检索结果匹配度,排列次序都很接近,检索给出的顺序也不一定正确。但它们的保留时间可能会不同,但保留时间只能在特定色谱条件下不变,而保留指数在固定相相同下有可比性。虽然在相同的柱子上和相同的色谱条件下,两个不同的化合物的保留指数有可能相同。但两个化合物同时具有相同的保留指数(或保留时间)和相同的质谱图的不可能性极小。虽然保留时间也可以帮助确认,但保留时间会随着柱子使用的不同阶段新旧等因素而变化,但保留指数是和固定相为主要因素的一个值,相对比较固定不变。所以才有保留指数辅助定性更具有优势。在谱库检索的基础上,用保留指数来确认结果。是一种很重要的手段。 一、基本概念保留指数retention index或Kovats Index(RI或KI)概念是由Kovats在1958年提出。是把组分的保留值用两个分别前后靠近它的正构烷烃来标定(这比仅用一个参比物质的相对保留值定向更为精确)。正构烷烃的保留指数规定为等于该烷烃分子中碳原子数的100倍。例如正己烷的RI为600,正庚烷为700,正十五烷为1500.正构烷烃的RI与所用的色谱柱,柱温及其它操作条件无关。 保留指数(RI)的计算公式如下:I=100Z+100R(x)- logt’R(z)]/R(z+1)- logt’R(z)] (恒温分析)式中:t’R为校正保留时间;Z和Z+1分别为目标化合物(X)流出前后的正构烷烃所含碳原子的数目;这里:t’R(z) t’R(x)
NIST05谱库没有保留指数,想问问大家检索时候都有应用保留指数来定性吗?正在建立自建库,想把保留指数也加入谱库中,避免以后又的重新一个一个加入库中,工作量太大。在网上理解了一下,保留指数的加入后,做样品往往有不同的升温程序,这个不影响保留指数?保留指数较适用于课题研究嘛?
[align=center][b]保留指数应用(9)----利用已知保留指数化合物反推正构烷的出峰时间[/b][/align][b] [/b]保留指数作为[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]定性一个强有力的辅助手段,在天然香精油,香气香味材料,香精产品等的分析鉴定中广泛应用。当然应用范围远不止这些。对于异构体,同系物和结构特征相似的化合物,由于其质谱图非常相似,谱库检索结果匹配度,排列次序都很接近,检索给出的顺序也不一定正确。但它们的保留时间可能会不同,但保留时间只能在特定色谱条件下不变,而保留指数在固定相相同下有可比性。虽然在相同的柱子上和相同的色谱条件下,两个不同的化合物的保留指数有可能相同。但两个化合物同时具有相同的保留指数(或保留时间)和相同的质谱图的不可能性极小。虽然保留时间也可以帮助确认,但保留时间会随着柱子使用的不同阶段新旧等因素而变化,但保留指数是和固定相为主要因素的一个值,相对比较固定不变。所以才有保留指数辅助定性更具有优势。在谱库检索的基础上,用保留指数来确认结果。是一种很重要的手段。本篇主要探讨利用已知保留指数化合物来反推正构烷的出峰时间。有时候由于条件限制而无法测定到或得到正构烷系列的保留时间。如果推算估算出这个条件下的正构烷的保留时间,然后利用这些保留时间值去进行其它化合物保留指数的相关计算,这时候可能就非常有用。 附:保留指数基本概念保留指数retention index或KovatsIndex(RI或KI)概念是由Kovats在1958年提出。是把组分的保留值用两个分别前后靠近它的正构烷烃来标定(这比仅用一个参比物质的相对保留值定向更为精确)。正构烷烃的保留指数规定为等于该烷烃分子中碳原子数的100倍。例如正己烷的RI为600,正庚烷为700,正十五烷为1500.正构烷烃的RI与所用的色谱柱,柱温及其它操作条件无关。保留指数(RI)的计算公式如下:I=100Z+100[logt’[sub]R(x)[/sub]-logt’[sub]R(z)[/sub]]/ [logt’[sub]R(z+1)[/sub]- logt’[sub]R(z)[/sub]] (恒温分析) (1)式中:t’[sub]R[/sub]为校正保留时间 Z和Z+1分别为目标化合物(X)流出前后的正构烷烃所含碳原子的数目 这里:t’[sub]R(z)[/sub] t’[sub]R(x)[/sub] t’[sub]R(z+1)[/sub], 一般正构烷烃所含碳原子的数目Z大于4.以上的保留指数(RI)的计算只用于恒温分析。对于沸点范围较宽的复杂组分混合物的分析,一般采用程序升温的方法。在程序升温时,组分的保留指数的测定有所不同。两者有差异,需要校正。1963年Van Den Dool 等经过推算(详细的推导过程略)引入线性程序升温保留指数的概念。I[sup]T[/sup]=100Z+100[T[sub]R(x)[/sub]-T[sub]R(z)[/sub]]/[T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]] (线性程序升温) (2) 式中:T[sub]R(x)[/sub][sub],[/sub]T[sub]R(z)[/sub][sub],[/sub]T[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留温度。且T[sub]R(z)[/sub]T[sub]R(x)[/sub]T[sub]R(z+1)[/sub][sub]。[/sub][sub] [/sub] 一般讲,保留温度的测量比保留时间的测定要麻烦一点。由于保留温度和保留时间通常具有高度的相关性,所以用保留时间代替上式中的保留温度来进行计算保留指数。I[sup]RT[/sup]=100Z+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/[RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]] (线性程序升温) (3)式中:RT[sub]R(x)[/sub][sub],[/sub]RT[sub]R(z)[/sub][sub],[/sub]RT[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留时间。且RT[sub]R(z)[/sub]RT[sub]R(x)[/sub]RT[sub]R(z+1)[/sub][sub]。[/sub][b]保留指数与保留时间的转换[/b]从I[sup]T[/sup]=100Z+100[T[sub]R(x)[/sub]-T[sub]R(z)[/sub]]/ [T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]](3)式可以导出:T[sub]R(x)[/sub]= [I[sup]T[/sup]-100Z]*[T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]]/100+T[sub]R(z) [/sub](4)[sub] [/sub]
国家环境保护总局新颁布的《室内环境空[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]量技术规范》(HJ/T167-2004)中规定作TVOC要用非极性柱(极性指数小于10)。什么是毛细管柱的极性指数?这个是商业名词,还是专业术语,我在《现代实用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法》(许国旺)没有查到。请教给位高手,谢谢。
GCMS在分析数据给物质定性时,我一般根据质谱检索到的相似度以及物质的元素种类来判断化合物是否需要,同时也会知道物质的保留指数,那么保留指数在这里该怎么利用呢?
[center]色谱定性分析(一)利用纯物质对照定性在一定色谱条件下,一个未知物只有一个确定的保留时间。因此将已知纯物质在相同的色谱条件下的保留时间与未知物的保留时间进行比较,就可定性鉴定未知物。若二者相同,则未知物可能是已知的纯物质;不同,则未知物就不是该纯物质。纯物质对照法定性只适用于组分性质已有所了解,组成比较简单,且有纯物质的未知物。 (二)相对保留值法相对保留值是指组分i与基准物s调整保留值的比值,即: 它仅随固定液及柱温变化而改变,与其它操作条件无关。相对保留值的测定方法:在某一固定相及柱温下,分别测出组分i和基准物质s的调整保留值,再按公式可求出的值。 (三)加入已知物增加峰高法当未知样品中组分较多,所得色谱过密,用上述方法不易辨认时,或仅作未知样品指定项目分析时均可用此法。首先作出未知样品的色谱图,然后在未知样品中加入某已知物,又得一色谱图。峰高的增加的组分即可能为这种已知物。 (四)保留指数定性法保留指数(retention index) I 是柯瓦(Kovats)于1958年所提出的,所以又称柯瓦指数。它表示物质在固定液上的保留值行为,是目前使用最广泛并被国际上公认的定性指针。它具有重现性好、标准统一及温度系数小等优点。保留指数的物理意义在于:它是与被测物质具有相同调整保留时间的假想的正构烷烃的碳数乘以100。保留指数仅与固定相的性质、柱温有关,与其它实验条件无关。其准确度和重现性都很好。 (五)其它方法 除利用保留值定性外,尚可利用检测的选择性响应的特点将未知物大致分类,还可与化学反应结合起来,是一种简便、有效的定性方法。此外,还可与别的方法,如红外光谱法(IR)、质谱法(MS)、核磁共振波谱法(NMR)等结合进行定性鉴定。[/center]