推荐厂家
暂无
暂无





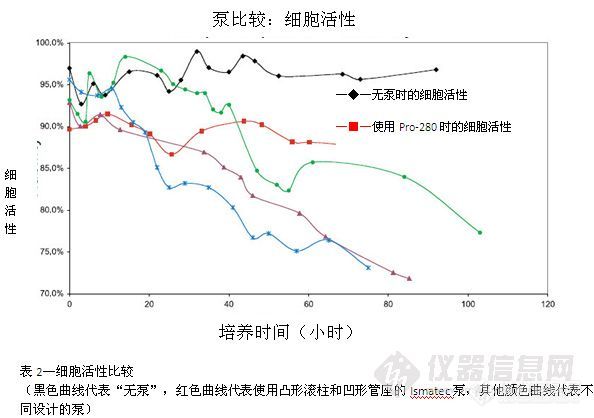
随着全球对生物技术和生物替代燃料开发的日益重视,使用包含生物材料的流体进行的分析工作也越来越多。无论该种分析涉及血细胞计数还是细菌培养(涉及许多其他生命科学应用),它们都有一个共同点,这就是经常需要将生物样本从一个地方转移到另一个地方。有时这种转移可手动完成(例如手持式移液器),但对高通量的需求持续推动着人们开发更加自动化的技术。目前很多研究人员面临的挑战就是,各种泵送技术对细胞物质造成的负面影响:· 往复泵——生命科学分析工作中最常使用的两种往复泵为隔膜泵和柱塞/注射泵。隔膜泵通常由单向阀和一个柔性膜片(安装在驱动电机轴上)组成,该隔膜通过自身“脉冲”动作推动液体在泵内进出。柱塞/注射泵则将正排量活塞或柱塞与某些类型的旋转剪切阀结合,通过活塞或柱塞的移动推动液体移动。这两种类型的往复泵都会带来细胞活性的问题,这是由于细胞会暴露在较强的真空力和剪切力下。这些力量会使细胞破裂,从而大大降低细胞活性以及进行更长期试验的可能性。此外这两种泵送技术还会造成清洁困难,从而导致样本夹带和交叉污染的可能性增加。· 齿轮泵——齿轮泵通过两个(或多个)啮合齿轮的高速旋转进行工作。随着“主动”齿轮和“从动”齿轮在高速旋转时相互接合,流体也在轮齿间向前移动。由于流体在高速转移时会受到物理应力的影响,因此这种泵送方式会为生物样本带来一些问题。例如轮齿经常会剪切细胞物质,从而导致分析样本或液体失效。此外,由于流体会接触泵的机械部分,样本间的交叉污染也难以避免。目前运用日益普遍的一种泵送技术采用了蠕动泵。蠕动泵通过一系列滚柱,很容易地对软壁管道进行压缩和扩展。该种泵送技术具有维持细胞活性和减少样本间交叉污染的多种优势:· 真空力小——蠕动泵通常采用软壁弹性管道。这种管道很容易被压缩,并可以很快恢复原始形状。蠕动泵使用的滚柱能够在管座下旋转的同时完全压缩流路管道。压缩后滚柱继续移动,管道也会重新扩张至原始形状,形成的低真空则可以在下一个滚柱再次压缩管道前将液体拉进管道。管道重复扩张形成的低真空足以移动液体但不会损害细胞物质。· 剪切力小——蠕动泵可保持相当一致的流量(泵的固有脉动效应除外)并避免流体与泵的机械部件直接接触。这两种特性都能将样本可能承受的剪切力减到最小,并帮助增加样本存活率。· 管道压缩点数量最少——由于软壁蠕动管道仅在有限的点完全压缩,大部分管道保持开放,从而降低了生物材料被压缩和损害的可能性。· 仅使用管道流路——蠕动泵的一个独特设计在于只有管道与被转移材料接触,被转移的材料不会接触泵的机械部分。这将使管道能够在用于不同分析工作前进行清洗、灭菌或更换,从而消除了样本间交叉污染的可能性。滚柱和管座设计也是大部分单通道Ismatec®泵的特色,它们通过滚柱在管座上推压管道。目前的很多泵都采用平面滚柱和管座,而大部分Ismatec单通道泵采用凸面滚柱和有一定弧度的凹面管座。Ismatec的滚柱在接触管道时仅会压缩管道中心,生物材料可通过缝隙进入管道壁以避免受到损害或破坏。(见下图1)http://ng1.17img.cn/bbsfiles/images/2017/01/201701191653_630768_1587_3.jpg为对比此种滚柱/管座设计与其他设计而进行的独立研究清楚表明,该种设计可以同时提高细胞浓度(培养期间)和细胞活性。(见下表1和2)http://ng1.17img.cn/bbsfiles/images/2017/10/201105201109396510_01_1587_3.jpghttp://ng1.17img.cn/bbsfiles/images/2017/10/201105201110103059_01_1587_3.jpg蠕动泵也存在需要考虑的一些缺陷,例如泵在工作时经受的压差十分有限。另外管道本身也需要克服一些挑战,例如弹性管道的化学兼容性不够广泛,使用过程中也会发生磨损,从而导致管道在使用期间流量不稳定及/或发生变化。事实上最重要的或许是蠕动泵需要承受脉动,这是其工作过程中的固有现象。脉动流会在离开管道流路时导致液体“喷洒”,另外分析腔内流量的不断变化也会导致实时流量分析无法提供确定的结果。虽然蠕动泵技术的这些局限阻碍了其在一些应用中的使用,但对很多应用—尤其是那些因涉及生物样本而被分类为“生命科学”的应用—蠕动泵是最佳选择。

采集病原微生物样本应当具备下列条件:http://ng1.17img.cn/bbsfiles/images/2014/12/201412150942_527186_2433088_3.jpg
基质辅助激光解吸电离飞行时间质谱(matrix-assisted laser desorption/ionization-time of flight mass spectrometry, MALDI-TOF MS)是20世纪80年代发展起来的一种新型软电离有机质谱, 作为一种新兴的蛋白质组学检测技术, 现已广泛应用于生命科学及相关领域。同时作为一项新兴的微生物鉴定技术, 受到了国内外的广泛关注。与传统的生化表型鉴定方法和分子生物学方法相比, MALDI-TOF MS具有操作简单、快速、准确和经济的特点。早在1975年, ANHALT等[1]利用质谱仪结合高温裂解技术第1次完成了细菌的鉴定, 从此拉开了质谱鉴定细菌的“ 序幕” 。随着质谱检测技术的不断完善和发展, 近年来, MALDI-TOF MS已经成功应用于微生物的鉴定, 显示了其在细菌、酵母菌等鉴定方面均具有良好的应用价值。众多的研究表明, MALDI-TOF MS技术对培养出的纯菌落进行菌种鉴定具有很高的稳定性及准确性, 对常见细菌和酵母菌的属的鉴定率能达到97%~99%, 种的鉴定率也能达到85%~97% 另外, MALDI-TOF MS大大缩短了细菌鉴定的时间, 而且其成本也较常规鉴定方法低[2, 3]。除此之外, MALDI-TOF MS已经能够成功地用于部分微生物亚种水平的鉴定和细菌耐药性的检测, 但这种方法在大多数情况下是应用于培养出的纯菌落的鉴定[3]。 如果能够从临床样本中直接检测细菌/真菌, 突破细菌/真菌培养阳性率低、培养时间长的瓶颈, 为细菌/真菌感染性疾病的诊疗提供更快、更准确的病原学依据, 将对临床及时控制细菌/真菌感染性疾病起到更大的作用。国内外学者已尝试将质谱技术应用于临床样本的直接检测, 并取得了显著的进展。本文就MALDI-TOF MS技术在临床样本的直接检测应用作一综述。一、MALDI-TOF MS检测原理 MALDI-TOF MS技术用于微生物鉴定的实质就是检测具有属、种或亚型特异性的生物标志的质量信号, 主要是微生物菌体内高丰度、表达稳定和进化保守的核糖体蛋白。MALDI-TOF MS 仪器主要由基质辅助激光解吸离子源(MALDI)和飞行时间质量检测器(TOF)两部分组成。MALDI的原理是用一定强度的激光照射样本与基质形成的共结晶薄膜, 基质从激光中吸收能量而汽化, 并迅速降解, 使样本分解吸附, 基质和样本之间发生电荷转移从而使样本分子发生电离 TOF的原理是带有电荷的样本分子在电场作用下加速飞过飞行管道, 因为离子的质荷比与离子的飞行时间呈正比, 所以不同质量的离子因达到检测器的飞行时间不同而被检测, 以离子峰为纵坐标、离子质荷比为横坐标形成特征性的质量图谱。将不同种属微生物经MALDI-TOF分析所形成的质量图谱与数据库中的参考图谱进行比较, 从而实现对目标微生物种或菌株的区分和鉴定[2]。二、MALDI-TOF MS直接检测临床样本的流程 临床样本直接检测的流程主要包括3个部分:临床样本的预处理、样本上机检测和对比蛋白质指纹图谱数据库得出鉴定结果。由于目前报道最多的临床样本是阳性血培养瓶和中段尿样本, 下面将以这二者为例介绍其直接检测的流程, 其它临床样本的检测流程与之类似。(一)临床样本预处理 MALDI-TOF MS直接用于临床样本的检测有2个基本的要求:(1)临床样本中细菌的量。为了得到准确的鉴定图谱, MALDI-TOF MS技术对置于靶板上的细菌的最低检测限约为(1× 104)~(1× 106)cfu/mL。若要直接检测拟似血流感染的血液样本以及拟似泌尿系统感染的中段尿等临床样本中的病原菌, 首先必须富集细菌 (2)临床样本的质。由于血液和血培养瓶中的大分子成分如血红蛋白和其它蛋白成分、尿液中的白细胞等有机成分会干扰细菌的谱峰, 所以直接检测前需要采取预处理措施去除这些干扰因素。1.阳性血培养瓶直接检测 直接检测阳性血培养瓶的细菌浓度常常需要1× 107 cfu/mL[2, 4]。由于在血流感染患者血液中的细菌量常常很低(最低可 1~10 cfu/mL), 因此对血样本的直接检测需要一个增菌的过程, 即采用血培养瓶增菌。目前已报道的阳性血培养病原菌预处理程序各不相同, 但预处理过程主要包含了以下2个步骤:(1)将细菌从血细胞中分离出来。先应用温和去污剂(如吐温-80、十二磺基硫酸钠、皂素等)将血液中的血细胞溶解, 然后通过不同的流程(离心、洗涤)去除其它的干扰因素, 纯化要鉴定的细菌样本 (2)将菌体中的蛋白质抽提出来。最常用的是混合溶剂处理法, 使用甲酸/乙腈溶液对样本进行处理来抽提蛋白, 利用2种溶剂的混合作用将菌体表面的蛋白和存在于细胞内的低相对分子质量的高丰度蛋白提取出来, 实现对菌株的鉴定。虽然至今尚没有规范化的处理程序, 不过目前市场上已有商品化的阳性血培养瓶预处理试剂盒Sepsityper kit(Bruker)可以提高鉴定分数和鉴定准确率, 但是花费比较高, 处理程序也费时较长[5]。另外, HAMMARSTR? M等[6]建立了一种基于声学捕捉和集成选择性富集目标(integrated selective enrichment target, ISET)的新方法用于富集样本中的细菌, 快速、准确并且简化了人工操作, 有望替代传统的以离心为基础的分离方法。2.中段尿样本 要取得一个较高的鉴定成功率, 直接检测中段尿样本中病原菌至少需要的细菌数量是1× 105 cfu/mL[7, 8]。对尿样本的预处理程序较为简单, 主要有下面几个步骤:低速离心去除白细胞, 高速离心收集细菌, 沉淀, 经过洗涤、离心之后进行蛋白质的提取(常用的是甲酸、乙腈), 经高速离心后取1 μ L上清涂布到MALDI的靶板上, 在室温下干燥后即可进行检测。

 400-696-6689
400-696-6689
 留言咨询
留言咨询

 400-838-7877
400-838-7877
 留言咨询
留言咨询

 400-860-5168转5960
400-860-5168转5960
 留言咨询
留言咨询


