全自动层析分离纯化系统和制备液相是一样的吗?有什么区别?
美国如何买层析柱(玻璃柱):做色谱层析分离用的
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=81329]薄层色谱分析在层析分离过程中的应用[/url]
我要测土壤中的抗生素含量,目前计划流程是这样的:提取——HLB固相萃取——凝胶层析——LC/MS/MS检测因为腐植酸会对色谱影响很大,所以有人建议我用分子排阻滤掉大分子,但是我能查到的资料都是用凝胶色谱测定大分子的,想知道如果我只是要层析分离不用测定,是不是也要用专门的凝胶色谱柱?还是买了填料自己做个层析柱就可以?自己做的话怎么控制洗脱时间?从来没接触过凝胶,还请大大们指点!
请问一下,有没有用过国产液相色谱层析仪来纯化蛋白质的?仪器的性能如何?上海沪析好象有,但以前用的是pharmacia的AKTA,不知道国产的能不能用,不敢买,大家给提供一下意见吧
紫外吸收剂液相色谱怎么做?用什么方法分离
我选用紫外分光光度仪测量溶液的吸收度,从200——400nm全程扫描。用A(混合液)和B(由A混合液通过凝胶层析柱按时间段分别收集)两个样品分别测试,发现,B的某个时间段里收集的样品在275nm时有个较明显的峰,而在A中却没有发现,我想请问一下这样的情况是正常的吗?为什么会有这样的情况呢(混合物里没有,而分离物里有,而且经过凝胶层析分离物质结构应该不会改变呀)?望能得到专家的指点。
常说的过柱子应该叫柱层析分离,也叫柱色谱。我们常用的是以硅胶或氧化铝作固定相的吸附柱。 柱子可以分为:加压,常压,减压。 压力可以增加淋洗剂的流动速度,减少产品收集的时间,但是会减低柱子的塔板数。所以其他条件相同的时候,常压柱是效率最高的,但是时间也最长,比如天然化合物的分离,一个柱子几个月也是有的。 减压柱能够减少硅胶的使用量,感觉能够节省一半甚至更多,但是由于大量的空气通过硅胶会使溶剂挥发(有时在柱子外面有水汽凝结),以及有些比较易分解的东西可能得不到,而且还必须同时使用水泵抽气(很大的噪音,而且时间长)。以前曾经大量的过减压柱,对它有比较深厚的感情,但是自从尝试了加压后,就几乎再也没动过减压的念头了。 加压柱是一种比较好的方法,与常压柱类似,只不过外加压力使淋洗剂走的快些。压力的提供可以是压缩空气,双连球或者小气泵(给鱼缸供气的就行)。特别是在容易分解的样品的分离中适用。压力不可过大,不然溶剂走的太快就会减低分离效果。个人觉得加压柱在普通的有机化合物的分离中是比较适用的。 关于柱子的尺寸,应该是粗长的最好。 柱子长了,相应的塔板数就高。柱子粗了,上样后样品的原点就小(反映在柱子上就是样品层比较薄),这样相对的减小了分离的难度。试想如果柱子十厘米,而样品就有二厘米,那么分离的难度可想而知,恐怕要用很低极性的溶剂慢慢冲了。而如果样品层只有0.5厘米,那么各组分就比较容易得到完全分离了。当然采用粗大的柱子要牺牲比较多的硅胶和溶剂了,不过这些成本相对于产品来说也许就不算什么了(有些不环保的说,不过溶剂回收重蒸后也就减小了部分浪费)。 现在见到的柱子径高比一般在1:5~10,书中写硅胶量是样品量的30~40倍,具体的选择要具体分析。如果所需组分和杂质分的比较开(是指在所需组分rf在0.2~0.4,杂质相差0.1以上),就可以少用硅胶,用小柱子(例如200毫克的样品,用2cm×20cm的柱子);如果相差不到0.1,就要加大柱子,我觉得可以增加柱子的直径,比如用3cm的,也可以减小淋洗剂的极性等等关于无水无氧柱,适用于对氧,水敏感,易分解的产品。 可以湿柱,也可以干柱。不过在样品之前至少要用溶剂把柱子饱和一次,因为溶剂和硅胶饱和时放出的热量有可能是产品分解,毕竟要分离的是敏感的东东,小心不为过。也是因为分离的东西比较敏感,所以接收瓶一定要用可密封的,遵循schlenk操作。至于是加压、常压、减压,随需而定。因为是schlenk操作,所以点板是个问题,如果样品是显色的,恭喜了,不用点板,直接看柱子上的色带就行了。如果样品无色,只好准备几十个schlenk瓶,一瓶一瓶的点,不过几次之后就知道样品在哪,也就可以省些了。像我以前过一根无水无氧柱,需要六个schlenk,现在只一个就能把所要的全收集到。 无水无氧柱中用的比较多的是用氧化铝作固定相。因为硅胶中有大量的羟基裸露在外,很容易是样品分解,特别是金属有机化合物和含磷化合物。而氧化铝可以做成碱性、中性和酸性的,选择余地比较大,但是比硅胶要贵些。
从96年开始过柱子,差点就八年抗战了。常说的过柱子应该叫柱层析分离,也叫柱色谱。我们常用的是以硅胶或氧化铝作固定相的吸附柱。由于柱分的经验成分太多,所以下面我就几年来过柱的体会写些心得,希望能有所帮助。柱子可以分为:加压,常压,减压。压力可以增加淋洗剂的流动速度,减少产品收集的时间,但是会减低柱子的塔板数。所以其他条件相同的时候,常压柱是效率最高的,但是时间也最长,比如天然化合物的分离,一个柱子几个月也是有的。减压柱能够减少硅胶的使用量,感觉能够节省一半甚至更多,但是由于大量的空气通过硅胶会使溶剂挥发(有时在柱子外面有水汽凝结),以及有些比较易分解的东西可能得不到,而且还必须同时使用水泵抽气(很大的噪音,而且时间长)。以前曾经大量的过减压柱,对它有比较深厚的感情,但是自从尝试了加压后,就几乎再也没动过减压的念头了。加压柱是一种比较好的方法,与常压柱类似,只不过外加压力使淋洗剂走的快些。压力的提供可以是压缩空气,或双连球(给鱼缸供气的就行)。特别是在容易分解的样品的分离中适用。压力不可过大,不然溶剂走的太快就会减低分离效果。个人觉得加压柱在普通的有机化合物的分离中是比较适用的。关于柱子的尺寸, 应该是粗长的最好。柱子长了,相应的塔板数就高。柱子粗了,上样后样品的原点就小(反映在柱子上就是样品层比较薄),这样相对的减小了分离的难度。试想如果柱子十厘米,而样品就有二厘米,那么分离的难度可想而知,恐怕要用很低极性的溶剂慢慢冲了。而如果样品层只有0.5厘米,那么各组分就比较容易得到完全分离了。当然采用粗大的柱子要牺牲比较多的硅胶和溶剂了,不过这些成本相对于产品来说也许就不算什么了(有些不环保的说,不过溶剂回收重蒸后也就减小了部分浪费)。现在见到的柱子径高比一般在1:5~10,书中写硅胶量是样品量的30~40倍,具体的选择要具体分析。如果所需组分和杂质分的比较开(是指在所需组分rf在0.2~0.4,杂质相差0.1以上),就可以少用硅胶,用小柱子(例如200毫克的样品,用2cm×20cm的柱子);如果相差不到0.1,就要加大柱子,我觉得可以增加柱子的直径,比如用3cm的,也可以减小淋洗剂的极性等等。关于无水无氧柱。 适用于对氧,水敏感,易分解的产品。可以湿柱,也可以干柱。不过在样品之前至少要用溶剂把柱子饱和一次,因为溶剂和硅胶饱和时放出的热量有可能是产品分解,毕竟要分离的是敏感的东东,小心不为过。也是因为分离的东西比较敏感,所以接收瓶一定要用可密封的,遵循schlenk操作。至于是加压、常压、减压,随需而定。因为是schlenk操作,所以点板是个问题,如果样品是显色的,恭喜了,不用点板,直接看柱子上的色带就行了。如果样品无色,只好准备几十个schlenk瓶,一瓶一瓶的点,不过几次之后就知道样品在哪,也就可以省些了。像我以前过一根无水无氧柱,需要六个schlenk,现在只一个就能把所要的全收集到。无水无氧柱中用的比较多的是用氧化铝作固定相。因为硅胶中有大量的羟基裸露在外,很容易是样品分解,特别是金属有机化合物和含磷化合物。而氧化铝可以做成碱性、中性和酸性的,选择余地比较大,但是比硅胶要贵些。听说有个方法,就是用石英做柱子,然后用HF254做固定相,这样在柱子外面用紫外灯一照就知道产品在哪里了,没有验证过。哪位做过可以提出来大家参详参详。关于湿法、干法上样。 湿法省事,一般用淋洗剂溶解样品,也可以用二氯甲烷、乙酸乙酯等,但溶剂越少越好,不然溶剂就成了淋洗剂了。很多样品在上柱前是粘乎乎的,一般没关系。可是有的上样后在硅胶上又会析出,这一般都是比较大量的样品才会出现,是因为硅胶对样品的吸附饱和,而样品本身又是比较好的固体才会发生,这就应该先重结晶,得到大部分的产品后再柱分,如果不能重结晶那就不管它了,直接过就是了,样品随着淋洗剂流动会溶解的。仪器仪表有些样品溶解性差,能溶解的溶剂又不能上柱(比如DMF,DMSO等,会随着溶剂一起走,显色是一个很长的脱尾),这时就必须用干法上柱了。样品和硅胶的量有一种说法是1:1,我觉得是越少越好,但是要保证在旋干后,不能看到明显的固体颗粒(那说明有的样品没有吸附在硅胶上)。溶剂的选择。 当然是最便宜,最安全,最环保的了。所以大多选用石油醚,乙酸乙酯。文献中有写用正己烷的,太贵了,除非特别需要不要用不然银子哗哗的,流的比淋洗剂还快,不过因为极性很小,有时还是非它不可。乙醚也可以用,但是就是容易睡觉,注意保持清醒别让溶剂流干了,那样柱子也就不爽了。二氯甲烷也有用的,但是要知道,它和硅胶的吸附是一个放热过程,所以夏天的时候经常会在柱子里产生气泡,天气冷的时候会好一些。甲醇,据说能溶解部分的硅胶,所以产品如果想过元素分析的话要留神,应该经过后继处理,比如说重结晶等。其他的溶剂用的相对较少,要依个人的不同需要选择了。由于某些原因,用到的淋洗剂多是大包装的(便宜嘛),我们这里是用10升或25升的塑料桶装的,就要注意这些工业品
我最近对一种物质进行检测,发现用紫外光谱仪和液相色谱的紫外检测器扫描出来的最大吸收波长不一致,相差2~3nm,这样的话哪个数据更准确些呢?而且峰形也有点不同,紫外检测器扫描的是单峰,而紫外光谱仪扫描出来的是有重叠的双峰。
[b]高效液相色谱紫外检测器需要信噪比指标[/b][i]法洋,许旭,雷晓玲[/i]摘 要:紫外吸收光学检测器是高效液相色谱中最常用的检测器。厂家采用的性能指标包括检测器的噪音,基线漂移等。考虑到该仪器用于分析测试实验的需求,增加信噪比指标可以较全面的评价不同型号检测器的性能差异。关键词:紫外吸收光学检测器 高效液相色谱 信噪比1 引 言紫外检测器是高效液相色谱中最常用的检测器,目前市场上生产厂家及型号很多,厂家通常采用检测器的噪音,基线漂移等技术参数作为产品的灵敏度性能评价指标。考虑到样品的紫外吸收响应值主要与样品有关,与仪器的关系不大,一般认为这可以基本反映仪器在灵敏度方面的性能。本文在实验的基础上证明对同一样品各检测器的响应值实际上也存在不同程序的差异,说明仅使用噪音和基线漂移的指标不能准确显示仪器在灵敏度方面的性能差异,因此,提出用信噪比来评价仪器的灵敏度性能。2 灵敏度评价指标设置的目的和依据高效液相色谱及其紫外检测器主要用于化学样品的分析测试。其评价指标必然与其用途相关联。一个分析方法对检测器的要求主要在灵敏度、选择性、精确度和准确性方面。在色谱分析中灵敏度是非常重要的指标。对于灵敏度,在分析测试方法研究中主要使用信噪比、最低检测限,或最低定量限来评价。其中信噪比是评价的核心,因为最低检测限和最低定量限通常用信噪比在2~3和10的量来定义。但目前厂家通常采用检测器的噪音,基线漂移等技术参数作为产品的灵敏度性能评价指标。这实际上是基于样品的紫外吸收响应值主要与样品有关,与仪器关系不大的假设。根据朗伯比尔定律,对于同样长度的检测池,同样浓度的样品溶液应该具有相同的吸光度。这样,对同样浓度的样品溶液,检测器的响应值应该是相同的,所以上述噪音,基线漂移的参数应该可以用来评价检测器的灵敏度性能。
作者:偶志红,徐丹丹,郭薇 来源:中国论文下载中心【摘要】 目的 建立薄层层析-紫外分光光度法测定香丹注射液中原儿茶醛的含量。方法 以原儿茶醛为对照品,展开剂为二氯甲烷-乙酸乙酯-甲酸(8∶5∶0.8)分离得到原儿茶醛,采用紫外分光光度法,检测波长281nm,测定原儿茶醛的含量。结果 原儿茶醛在0.55~4.95μg/ml 范围内线性关系良好,r=0.9998。平均含量为0.174mg/ml,加样回收率为97.3%~102.3%,RSD为1.6%。结论 实验结果表明,薄层层析-紫外分光光度法测定香丹注射液中原儿茶醛的含量,方法操作简便,准确度高,精密度好,可作为样品的检测方法。 【关键词】 香丹注射液;原儿茶醛;薄层层析-紫外分光光度法;含量测定
突然断电,高效液相色谱的紫外检测器会出现什么故障,如何解决。(比如:电压为零,基线永远是直线)
高效液相色谱法分离/蒸发光散射和紫外检测法 测定天麻中天麻甙含量 魏 泱 丁明玉* 李红霞 (清华大学化学系,北京,100084) 关键词 高效液相色谱法;蒸发光散射检测法;紫外检测法;天麻;天麻甙 中图分类号 O658 天麻(Gastrodia elata Blume)系兰科多年生寄生植物,用于治疗头昏,眩晕,肢体麻木等症。冯孝章等 [1]和周俊等 [2]分离并鉴定出天麻的活性成分有天麻甙(对羟甲基苯 b-D-吡喃葡萄糖甙,亦称天麻素)、 天麻甙元(对羟基苯甲醇)等.其中天麻甙为主要成分。之后的一些药理实验[3]也证实了这一点. 在测定天麻甙含量的方法中, 高效液相色谱法(HPLC)采用得最多. 正相HPLC[4]和反相HPLC[5]都可用于天麻及其制剂中天麻甙的分离,通常采用紫外检测法,检测波长在220 nm或270 nm处. 蒸发光散射检测器(ELSD)作为一种半通用型质量检测器,可用于检测类酯[6]、糖[7]等物质. 近年来,它在对天然药物的检测方面应用也越来越多,如对人参皂甙[8]、银杏内酯[9]的检测。HPLC/ELSD测定天麻甙尚未见报道. 1.实验与方法 1.1仪器与试剂 HP1100高效液相色谱仪(美国Hewlett Packard公司产品)配有四元梯度泵、二极管阵列检测器(DAD)和化学工作站. 另配有Alltech 500 ELSD(美国Alltech公司产品). 天麻甙为分析纯,购自中国药品生物制品检定所;对羟基苯甲醇和对羟基苯甲醛为分析纯,购自Sigma公司;甲醇为色谱纯,其他试剂均为国产分析纯试剂. 流动相使用前用0.45 mm滤膜过滤. 天麻原药材购自四川省,并经中国中医研究院鉴定. 1.2 色谱条件 ELSD和DAD检测均使用同样的色谱条件. 色谱柱: Zorbax RX-SIL (4.6 mm i. d. ´ 25 cm, 5 mm)硅胶柱,HP公司产品;配有预柱Micro Pak SI-5 (4 mm i. d. ´ 4 cm, 5 mm)硅胶柱,Parker公司产品. 流动相:正己烷/甲醇/乙酸乙酯(体积比6:3:2),流速0.8 mL/min;进样量20 mL;ELSD参数:漂移管温度65 ℃,氮气流速1.55 L/min;DAD检测波长270 nm。 1.3 样品处理 天麻干燥块茎粉碎后,准确称取100 g. 用70%的乙醇水溶液热回流3次,每次回流后再用超声提取. 提取液过滤后经浓缩得浓缩液. 浓缩液用甲醇稀释至适当浓度,放入冰箱冷冻。澄清液经0.45 mm滤膜过滤后直接进行HPLC分析。 1.4 标准溶液的配制 分别称取89.0 mg和21.3 mg的天麻甙溶于100 mL甲醇中配制成两个储备液. 使用前以甲醇稀释成适当浓度的工作溶液. 2. 结果与讨论 2.1 天麻甙的分离 天麻的乙醇提取物中成分很多. 当流动相正己烷/甲醇/乙酸乙酯的体积比为5:3:2时,从DAD检测的色谱图来看,各种物质已经得到了较好的分离,但从ELSD检测色谱图上发现,天麻甙峰左侧有肩峰,说明有弱极性物质与天麻甙分离不完全,只是该物质在270 nm处无紫外吸收。增大正己烷比例,当正己烷/甲醇/乙酸乙酯的体积比达6:3:2时,无论从DAD检测结果〔图1(B)〕,还是ELSD检测结果〔图2(B)〕来看,提取物中的天麻甙与其他成分完全分离。从图1(B)可知,天麻提取物中的天麻甙元和对羟基苯甲醛与其后相邻的其他组分的分离不完全,因为本文的重点是比较ELSD和DAD检测天麻甙,故未对其它组分的分离条件进行优化。继续增大正己烷比例,各组分之间的分离度可进一步提高,但将导致分析时间过长。天麻甙也可以使用反相条件进行分离. 由于反相条件下,流动相中含水较多,ELSD工作时需要较高的漂移管温度和氮气气速,从而降低天麻甙的检测灵敏度. 故我们选用正相色谱条件来分离天麻甙. 天麻甙元和对羟基苯甲醛的挥发性较大, 即使在正相色谱条件下,也不能被ELSD检测. Fig.1 The chromatograms of the standards(A) and ethanol extracts of Gastrodia elata Blume.(B) detected by DAD 1. 4-hydroxybenzyl alcohol 2. 4-hydroxybenzaldehyde 3. Gastrodin. Fig.2 The chromatograms of the standards(A) and ethanol extracts of Gastrodia elata Blume.(B) detected by ELSD 1. Gastrodin 2.unknown. 3.2 ELSD条件优化 通过改变漂移管温度和氮气流速,选定在较小噪音水平上产生最大检测响应值的条件为:漂移管温度65 ℃,氮气流速1.55 L/min。 3.3 线性关系考察 将贮备液稀释配成21.3-890 mg/L的一系列浓度,依次进样20 mL,根据ELSD和DAD测得的峰面积对相应的标准溶液浓度进行线性回归。将最小浓度的标准溶液再逐级稀释,依次进样20 mL,计算当信噪比为3时,对应的标准溶液的浓度以确定检出下限。结果见表1. Table 1 Some parameters of gastrodin for quantitative analysis by ELSD and DAD Detector Linear range /(mg L-1) Calibration curve Calibration coefficient (r) Detection limit / (mg L-1) ELSD 21.3~890 Y=-56720.51+2534.46X 0.998 3.0 DAD 21.3~890 Y=-89.31+4.75X 0.999 1.0 3.4 天麻样品的测定 同一份样品重复进样5次,用ELSD和DAD测定其峰面积,取5次测定平均值计算样品中天麻甙含量. 在样品溶液中加入已知量的天麻甙标准溶液,测定回收率. 结果见表2. Table 2 Determination results of gastrodin in Gastrodia elata Blume by ELSD and DAD Detector Mass fraction (%) Recovery (%) RSD (%) ELSD 1.39 104.22 2.79 DAD 1.21 97.65 2.99 3.5 ELSD和DAD检测的比较 ELSD和DAD作为两种不同类型的检测器,其适用范围不尽相同. DAD所能检测的物质必须具有紫外吸收,而所采用的流动相应当在检测波长下无紫外吸收. 对于无紫外吸收的物质,可以通过衍生化的方法接上生色团. ELSD要求被测物比流动相难于挥发,对于一些半挥发性的物质,其检测灵敏度很低。同时,应当尽量避免使用高沸点的溶剂作为流动相. 对于一些分离中常加入的添加剂,如乙酸盐,磷酸盐等,ELSD检测时应用易挥发的盐来代替. 使用DAD和ELSD同时检测, 可以获得更多的物质信息, 且可以获得更准确的定量结果.
你用过紫外检测器的液相色谱吗?使用的方法是什么?用于分析什么样品?[em0815]
[color=#444444]新和成了一种物质,想要液相色谱分析一下纯度,但不知道最大吸收波长,用紫外分光光度计做波长扫描,在330nm有最大吸收,可以在这个波长下用液相色谱分析吗?我也不知道这样做对不对[/color]
制备型加压液相色谱,按照色谱柱和样品量的大小,分为:(1)低压液相色谱;(2)中压液相色谱;(3)高压液相色谱;(4)快速色谱。低压、中压与高压液相色谱的压力范围之间会存在一定交叠,没有统一、明确的标准。1快速色谱柱压通常为2bar(或30psi)左右,对于那些容易分离的简单混合物,由于快速色谱具有操作简便、经济等优点,常常是实验室的首选。但快速色谱不同于一般的层析分离,这种分离没有压力,而快速分离通常使用瓶装氮气加压,使流动相具有一定的流速,从而缩短了分离时间。Still等人率先于1978年详细研究了快速色谱,并于1981年获得了专利保护(美国专利4,293,422)。快速色谱使用的柱子一般是玻璃柱,柱直径为3~10cm.长度为7~15cm。快速色谱中使用最广泛的固定相为硅胶。采用的粒径通常为:25~40μm,40~63μm或63~200μm的球形固定相。其它如键合相、氧化铝、聚酰胺吸附剂也常用作快速色谱的固定相使用。2低压色谱(LPLC)柱压一般低于5bar(或75psi)。低压色谱一般是由蠕动泵、进样阀和检测器组成,可以连续化,实现自动的梯度淋洗和馏分收集等操作。色谱柱管一般是玻璃或聚合物材料的,长度一般为240-440mm,内径为10-40mm。对于大多数在紫外区有吸收的物质,光学检测器很常用。填料一般使用软质的葡聚糖、琼脂糖、纤维素、合成高聚物或离子交换剂,粒径一般为40-60μm。3中压液相色谱(MPLC)柱压在5-20bar(或75-300psi)之间,广泛用于实验室和工业规模的生物制品(如动物脏器提取液、浓缩液、体液、植物提取液、生物技术发酵液等--往往需要经过滤膜作初级净化)的处理,以提取或纯化所需的产品。中压液相制备色谱的主要部件为输液泵、进样阀、检测器、馏分收集器等,比如瑞士公司的早期的中压液相制备色谱,其输液泵最大流速可达156mL/min,并配有阻尼器,以保证液流的稳定;进样器配有0.5-50mL的不同体积的定量管;检测器有紫外和示差折光检测器,流通池体积比较大,允许大流量流动相通过而无需分流;馏分收集器有原盘式和排式两种,原盘式的接收管最多达80个,而后者则更多;色谱柱内径9-105mm,长度250-1760mm不等。对于一般中压制备色谱,当色谱柱直径较大时,柱头往往设计成锥形或有类似于伞状的液流导向结构,使得当大量样品进入到柱头上时,能迅速地分散到整个柱横截面上,及时被流动相冲走,避免了因样品的局部过浓而引起柱超负荷和谱带加宽。柱子填料则采用比较耐压的交联改性的多糖凝胶(如Sepharose CL,Superose等),聚合物微球,复合材料介质或硬质SiO2基体的化学键合相等,粒径一般在25~40μm(最常用的填料尺寸是15-25μm,25-40μm或40-63μm),可采用湿法或干法装柱。4高压液相色谱(HPLC)是指柱压一般大于20bar(或300psi)的“高压(或高效)液相色谱”,通常指所用色谱柱的塔板数大于2000,一般是在2,000~20,000的范围之间。当需要从大量的物质中分离纯化不足1%的所需成分时,分离工作将会十分困难,往往在纯化的最后阶段需要使用10μm或更小颗粒的高效填料。为获得所需微量组分,可采用如下分离手段:制备型分离→半制备型分离→分析型分离→产物。为提高每次分离获得纯品的数量,制备型高压液相色谱分离通常在超载情况下运行。高压液相色谱,即目前常用的高效液相色谱。色谱柱内填装的是粒度范围较窄的微小颗粒固定相(3~30μm),为使流动相流出,需采用较高的压力,同时系统的复杂性及成本亦增大,但分辨率可得到较大的提高。而填装较大颗粒的固定相时,如中压液相色谱系统,装柱较容易,柱的通透性较高(只需较低的泵压力),可采用更大的色谱柱和更经济的仪器,由此分辨率也较低。5用分析型高压液相色谱进行制备型分离当所需纯化合物的量很少时(微克级至几毫克),可用分析型色谱柱进行多次分离。效果和利用大直径色谱柱进行一次性分离相同。采用小直径色谱柱时,可利用已有的分析型仪器,而无需在色谱柱、填料及附件方面投入更大资金;另外,还可在很大程度上避免由于放大所产生的问题,使分离速度加快。小直径色谱柱的尺寸一般为250×4.6mm,通常装有反相填料,每次可进样5~100ug,通过多次进样分离,可获得足够的纯品。例如,Suzuki等(1994)报道从豆科植物羽扇豆(Lupinus Hirsutus)中分离一羽扇豆生物碱糖苷时,其最后的分离步骤采用LiChrosorb Si60,5μm,250×4.6mm色谱柱进行高压液相色谱分离,洗脱剂为含25%甲醇的yi醚溶液-5%氨水50:1。经常需用分析型色谱柱进行分离的一个领域是对肽类化合物的纯化。生物活性肽的含量通常很低,用分析型高压液相色谱作为最后的纯化手段时,不会使色谱柱超载。为了提高分离效率,可将分析型高压液相色谱柱连接起来使用。此时可采用颗粒度在20~30μm的填料,以保持适当的通透性,尤其是当使用含水溶剂时。当使用己烷等有机溶剂时,由于流动相的粘度较低,可使用颗粒度为10μm的填料。然而由于分析型色谱系统无法提供大规模制备型分离所需的流速,其应用受到一定限制。(来源:分析测试百科网)
如何确定液相色谱紫外灯能量,在2000小时外可以继续使用,能量衰减后对检测结果(杂质和含量)基本无影响?以及相应依据?
使用过紫外检测器的液相色谱吗?来探讨一下吧!
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=86892]薄层层析分离氨基酸.ppt [/url]
液相色谱紫外检测器与通用型检测器 液相色谱现在用的最多的是紫外检测器,约占总数的85%,然而液相色谱的通用型检测器却没有紫外检测器。液相的通用型检测器常见的有示差折光检测器,蒸发光散射检测器等,这些检测器在液相色谱的用量和使用范围都不是很广。 示差折光检测器稳定性较好,但使用条件如对温度、气泡、压力等要求较高,不能采用梯度洗脱方式,灵敏度相对不高,一般多用在没有紫外吸收的糖类物质的检测。蒸发光散射检测器灵敏度较高,可以采用梯度洗脱方式,但它需要纯度较高的气源,有污染气体排出,稳定性不够理想,问题较高,对气体压力、流量要求较高,一般多用于二十几种药物检测。 而紫外检测器虽然不是通用型检测器,但它能检测大多数的有机物,约80%以上。而且它的灵敏度较高,稳定性较好,能采用梯度洗脱方法,对实验条件及环境要求也不是很高,造价不高,维护、维修简单、方便,危险性较低等种种优势。所以成为液相色谱首选的检测器。 当然液相色谱用的荧光检测器也有很多优点,比如灵敏度极高,能到十的十二十三次方,可以检测具有荧光效应的有机物,属于选择性检测器,稳定性较好线性较宽较好、使用方便等。另外通用型检测器也还有很多种,也还有很多值得开发、改进的,发展空间很宽广、很有前途。 希望液相色谱明天会更好,通用型检测器更通用、更强大、完美!选择性检测器选择性更强、更专业!
我们公司买了一套上海天普分析仪器有限公司的LC2900型高效液相色谱仪一直以来都使用正常,前天按照原来的步骤打开仪器的时候,发现UV2930紫外分光检测器显示屏显示成这样了 前两部正常 到 Please Wait 后出现 WL CALIB ERROR R:02019 S:02019 请问这是什么原因各位大虾们帮帮忙,帮我解决一下。
高效液相色谱仪HPLC紫外灯的维护和更换一. HPLC紫外灯的维护对紫外灯的最根本维护就是在不进行测定时应及时关灯。具体的做法为:1.缩短检测前的开灯时间尽量在检测前1小时开紫外灯,具体时间根据系统的稳定时间而定。太早会缩短灯的使用寿命太晚会浪费流动相,对色谱柱也不好。2.检测结束后的关灯在检测结束后应立即关灯,最好采用仪器自动关灯。有人提出如果当天还有检测工作怎么办?一般认为频繁的开关对灯显然也不利,立即关灯当然是指一天的检测都结束后。在一天工作开始时应考虑工作量让液相在合适的时候开始工作,保证检测的连续性,缩短开灯时间。如果必须在中间停一段时间,则应视所停时间而定。二. HPLC紫外灯的更换 紫外灯何时更换说法不一。原先一般建议的使用时间为2000小时,现在不少液相厂家建议最好使用1000小时后更换。每个灯质量都不一样,具体时间可视灯的能量而定,如有人定的标准为800,每周一次检测灯能量并记录,当能量不足800时立即更换。
液相色谱紫外检测器的使用方法大家来探讨一下吧!
[color=#DC143C] 过柱的经验之谈过柱的经验之谈从96年开始过柱子,差点就八年抗战了。常说的过柱子应该叫柱层析分离,也叫柱色谱。我们常用的是以硅胶或氧化铝作固定相的吸附柱。由于柱分的经验成分太多,所以下面我就几年来过柱的体会写些心得,希望能有所帮助。柱子可以分为:加压,常压,减压。压力可以增加淋洗剂的流动速度,减少产品收集的时间,但是会减低柱子的塔板数。所以其他条件相同的时候,常压柱是效率最高的,但是时间也最长,比如天然化合物的分离,一个柱子几个月也是有的。减压柱能够减少硅胶的使用量,感觉能够节省一半甚至更多,但是由于大量的空气通过硅胶会使溶剂挥发(有时在柱子外面有水汽凝结),以及有些比较易分解的东西可能得不到,而且还必须同时使用水泵抽气(很大的噪音,而且时间长)。以前曾经大量的过减压柱,对它有比较深厚的感情,但是自从尝试了加压后,就几乎再也没动过减压的念头了。加压柱是一种比较好的方法,与常压柱类似,只不过外加压力使淋洗剂走的快些。压力的提供可以是压缩空气,双连球或者小气泵(给鱼缸供气的就行)。特别是在容易分解的样品的分离中适用。压力不可过大,不然溶剂走的太快就会减低分离效果。个人觉得加压柱在普通的有机化合物的分离中是比较适用的。关于柱子的尺寸, 应该是粗长的最好。柱子长了,相应的塔板数就高。柱子粗了,上样后样品的原点就小(反映在柱子上就是样品层比较薄),这样相对的减小了分离的难度。试想如果柱子十厘米,而样品就有二厘米,那么分离的难度可想而知,恐怕要用很低极性的溶剂慢慢冲了。而如果样品层只有0.5厘米,那么各组分就比较容易得到完全分离了。当然采用粗大的柱子要牺牲比较多的硅胶和溶剂了,不过这些成本相对于产品来说也许就不算什么了(有些不环保的说,不过溶剂回收重蒸后也就减小了部分浪费)。现在见到的柱子径高比一般在1:5~10,书中写硅胶量是样品量的30~40倍,具体的选择要具体分析。如果所需组分和杂质分的比较开(是指在所需组分rf在0.2~0.4,杂质相差0.1以上),就可以少用硅胶,用小柱子(例如200毫克的样品,用2cm×20cm的柱子);如果相差不到0.1,就要加大柱子,我觉得可以增加柱子的直径,比如用3cm的,也可以减小淋洗剂的极性等等。关于无水无氧柱。 适用于对氧,水敏感,易分解的产品。可以湿柱,也可以干柱。不过在样品之前至少要用溶剂把柱子饱和一次,因为溶剂和硅胶饱和时放出的热量有可能是产品分解,毕竟要分离的是敏感的东东,小心不为过。也是因为分离的东西比较敏感,所以接收瓶一定要用可密封的,遵循schlenk操作。至于是加压、常压、减压,随需而定。因为是schlenk操作,所以点板是个问题,如果样品是显色的,恭喜了,不用点板,直接看柱子上的色带就行了。如果样品无色,只好准备几十个schlenk瓶,一瓶一瓶的点,不过几次之后就知道样品在哪,也就可以省些了。像我以前过一根无水无氧柱,需要六个schlenk,现在只一个就能把所要的全收集到。无水无氧柱中用的比较多的是用氧化铝作固定相。因为硅胶中有大量的羟基裸露在外,很容易是样品分解,特别是金属有机化合物和含磷化合物。而氧化铝可以做成碱性、中性和酸性的,选择余地比较大,但是比硅胶要贵些。听说有个方法,就是用石英做柱子,然后用HF254做固定相,这样在柱子外面用紫外灯一照就知道产品在哪里了,没有验证过。哪位做过可以提出来大家参详参详。关于湿法、干法上样。 湿法省事,一般用淋洗剂溶解样品,也可以用二氯甲烷、乙酸乙酯等,但溶剂越少越好,不然溶剂就成了淋洗剂了。很多样品在上柱前是粘乎乎的,一般没关系。可是有的上样后在硅胶上又会析出,这一般都是比较大量的样品才会出现,是因为硅胶对样品的吸附饱和,而样品本身又是比较好的固体才会发生,这就应该先重结晶,得到大部分的产品后再柱分,如果不能重结晶那就不管它了,直接过就是了,样品随着淋洗剂流动会溶解的。有些样品溶解性差,能溶解的溶剂又不能上柱(比如DMF,DMSO等,会随着溶剂一起走,显色是一个很长的脱尾),这时就必须用干法上柱了。样品和硅胶的量有一种说法是1:1,我觉得是越少越好,但是要保证在旋干后,不能看到明显的固体颗粒(那说明有的样品没有吸附在硅胶上)。溶剂的选择。 当然是最便宜,最安全,最环保的了。所以大多选用石油醚,乙酸乙酯。文献中有写用正己烷的,太贵了,除非特别需要不要用不然银子哗哗的,流的比淋洗剂还快,不过因为极性很小,有时还是非它不可。乙醚也可以用,但是就是容易睡觉,注意保持清醒别让溶剂流干了,那样柱子也就不爽了。二氯甲烷也有用的,但是要知道,它和硅胶的吸附是一个放热过程,所以夏天的时候经常会在柱子里产生气泡,天气冷的时候会好一些。甲醇,据说能溶解部分的硅胶,所以产品如果想过元素分析的话要留神,应该经过后继处理,比如说重结晶等。其他的溶剂用的相对较少,要依个人的不同需要选择了。由于某些原因,用到的淋洗剂多是大包装的(便宜嘛),我们这里是用10升或25升的塑料桶装的,就要注意这些工业品的纯度是较低的。经常能够从送来的大桶底部看见有色的杂质,其他的杂质就可想而知了,所以在比较严格的柱分时就要对溶剂重蒸。当然过原料时就可以免去这一步了,反正下面还有提纯的方法。另外溶剂在过柱子后最好也回收使用,一方面环保,另一方面也能节省部分经费,缺点是要消耗一定的人工。这里要注意的是,一般在过柱同时进行的是减压旋蒸,石油醚和乙酸乙酯的比例由于挥发度的不同会导致极性的变化,一般会使得极性变大,在梯度淋洗时比较合适,正好极性越来越大了。在过完柱子后,溶剂最后回收要采用常压,因为在减压旋蒸时会有部分低沸点的杂质一起出来,常压时就会减少这种现象,如果杂质和你下面要过的样品有反应那就惨了。关于操作问题。1、 装柱。柱子下面的活塞一定不要涂润滑剂,会被淋洗剂带到产品中的,可以采用四氟节门的。干法和湿法装柱觉得没什么区别,只要能把柱子装实就行。装完的柱子应该要适度的紧密(太密了淋洗剂走的太慢),一定要均匀(不然样品就会从一侧斜着下来)。书中写的都是不能见到气泡,我觉得在大多数情况下有些小气泡没太大的影响,一加压气泡就全下来了。当然如果你装的柱子总是有气泡就说明需要多练习了。但是柱子更忌讳的是开裂,甭管竖的还是横的,都会影响分离效果,甚至作废!2、 加样。用少量的溶剂溶样品加样,加完后将下面的活塞打开,待溶剂层下降至石英砂面时,再加少量的低极性溶剂,然后再打开活塞,如此两三次,一般石英砂就基本是白色的了。加入淋洗剂,一开始不要加压,等溶样品的溶剂和样品层有一段距离(2~4cm就够了),再加压,这样避免了溶剂(如二氯甲烷等)夹带样品快速下行。3、 淋洗剂的选择。感觉上要使所需点在rf0.2~0.3左右的比较好。不要认为在板上爬高了分的比较开,过柱子就用那种极性,如果rf在0.6,即使相差0.2也不容易在柱子上分开,因为柱子是一个多次爬板的状态,可以通过公式的比较:0.6/0.8一次的分离度,肯定不如(0.2/0.3)的三次方或四次方大。4 、样品的收集。用硅胶作固定相过柱子的原理是一个吸附与解吸的平衡。所以如果样品与硅胶的吸附比较强的话,就不容易流出。这样就会发生,后面的点先出,而前面的点后出。这时可以采用氧化铝作固定相。另外,收集的试管大小要以样品量而定,特别是小量样品,如果用大试管,可能一根就收到了三个样品,wuwu。如果都用小试管那工作量又太大。5 、最后的处理。柱分后的产品,由于使用了大量的溶剂,其中的杂质也会累积到产品中,所以如果想送分析,最好用少量的溶剂洗涤一下,因为大部分的杂质是溶在溶剂里的,一洗基本就没了,必要时进行重结晶。[/color]请楼主下次发帖或者上传资料时,看清自己发的内容。此文非HPLC过柱经验!
HP 1050 液相色谱仪,紫外检测器 filter error怎么解决?
目的要求(1)了解克隆基因表达的方法和意义。(2)了解重组蛋白亲和层析分离纯化的方法。实验原理克隆基因在细胞中表达对理论研究和实验应用都具有重要的意义。通过表达能探索和研究基因的功能以及基因表达调控的机理,同时克隆基因表达出所编码的蛋白质可供作结构与功能的研究。大肠杆菌是目前应用最广泛的蛋白质表达系统,其表达外源基因产物的水平远高于其它基因表达系统,表达的目的蛋白量甚至能超过细菌总蛋白量的80%。本实验中,携带有目标蛋白基因的质粒在大肠杆菌BL21中,在 37℃,IPTG诱导下,超量表达携带有6个连续组氨酸残基的重组氯霉素酰基转移酶蛋白,该蛋白可用一种通过共价偶连的次氨基三乙酸(NTA)使镍离子(Ni2+)固相化的层析介质加以提纯,实为金属熬合亲和层析(MCAC)。蛋白质的纯化程度可通过聚丙烯酰胺凝胶电泳进行分析。试剂和器材一、试剂 LB液体培养基:Trytone 10g, yeast extract 5g, NaCl 10g, 用蒸馏水配至1000mL. 氨苄青霉素:100mg/mL 上样缓冲液:100 mM NaH2PO4, 10 mMTris, 8M Urea, 10 mM2-ME, pH8.0 Washing Buffer:100 mM NaH2PO4, 10 mM Tris, 8 M Urea, pH6.3 Elution Buffer:100 mM NaH2PO4, 10 mMTris, 8M Urea, 500 mM Imidazole, pH8.0 IPTG二、器材摇床,离心机,层析柱(1′10 cm)操作方法一、氯霉素酰基转移酶重组蛋白的诱导1. 接种含有重组氯霉素酰基转移酶蛋白的大肠杆菌BL21菌株于5mL LB液体培养基中(含100ug/mL 氨苄青霉素),37℃震荡培养过夜。2. 转接1mL过夜培养物于100mL(含100ug/mL 氨苄青霉素)LB液体培养基中,37℃震荡培养至OD600 = 0.6 - 0.8。取10ul 样品用于SDS-PAGE 分析。3. 加入IPTG至终浓度0.5 mmol/l, 37℃继续培养1-3h.4. 12,000rpm 离心10 min, 弃上清,菌体沉淀保存于-20℃或-70℃冰箱中。二、氯霉素酰基转移酶重组蛋白的分离、纯化1. NTA层析柱的准备:在层析柱中加入1mL NTA介质,并分别用8mL 去离子水,8mL上样缓冲液洗涤。2. 重组蛋白的变性裂解:在冰浴中冻融菌体沉淀,加入5mL上样缓冲液, 用吸管抽吸重悬,超声波破裂菌体,用振荡器等轻柔的混匀样品60min, 4℃ 12000rpm 离心 30 min, 将上清吸至一个干净的容器中,并弃沉淀。取10ul 上清样品用于SDS-PAGE 分析。3. 上清样品以10-15mL/h 流速上Ni2+-NTA柱,收集流出液,取10ul样品用于SDS-PAGE 分析。4. 洗脱杂蛋白:用Washing Buffer以10-15mL/h流速洗柱,直至OD280 = 0.01.分步收集洗脱液,约3-4h,取10ul洗脱开始时的样品用于SDS-PAGE 分析。5. 洗脱目标蛋白:用Elution Buffer洗柱,收集每1 mL 级分,分别取10ul样品用于SDS-PAGE 分析。
请问液相色谱紫外检测器灵敏度要怎么计算呢,比如我进1×10-4的萘甲醇
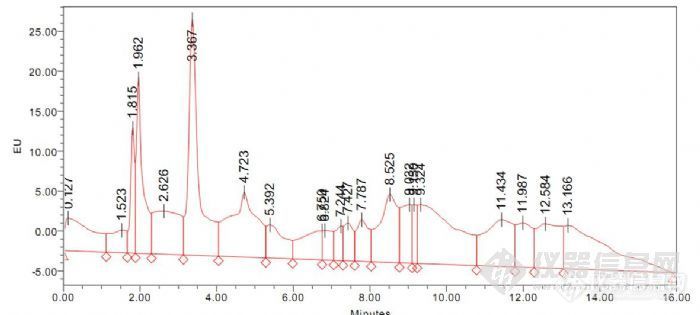
利用紫外和荧光光谱扫描技术开发高效液相色谱-荧光检测方法全过程荧光是光致发光中的一种,荧光过程是物质吸收入射光进入激发态,从激发态回到基态并发出波长更长得光的过程,在此过程中,物质吸收的光为激发光,发出的光为发射光(这个定义并不准确,有兴趣的版友可以参照相关教科书)。荧光检测在高效液相色谱中是比紫外检测更灵敏的检测方法,但是能够发出荧光的物质并不多,如何判断分析物有没有荧光特性并优化荧光检测器参数是荧光检测方法开发过程的重要内容。荧光检测方法优化的最重要两个参数是确定激发波长和发射波长。二极管阵列检测器(DAD)可以提供分析物在流动相的紫外吸收光谱,基于提取的紫外吸收光谱在日常高效液相色谱分分析中主要有两大作用:1.发现并确定紫外检测器的最佳检测波长;2进行进一步的运算做峰纯度检查,判断有没有共流出物。在这里通过实例向大家介绍二极管阵列检测器的另一用处:二极管阵列检测器辅助荧光检测器开发分析物的高效液相色谱-荧光检测方法。1实验设备和基本实验条件:Waters 2695分离单元Waters 2996 二极管阵列检测器Waters 2475 荧光检测器二极管阵列检测器和荧光检测器串列,荧光检测器在后(检测池耐压较差)二者之间死体积为1ml/min×0.1min。分析物为两种原料药色谱柱:C18,4.6×150mm,5μm柱温:30℃流动相:乙腈:醋酸盐缓冲溶液=65:352实验A:二极管阵列检测器获取紫外吸收光谱,荧光检测器扫描发射光谱实验仪器设置 :2996 3D采集模式,获取210-400nm紫外吸收谱图2475 3D采集模式,固定激发波长220nm(一般有紫外吸收的物质在210-230nm都有吸收),获取250-650nm发射光谱。利用二极管阵列检测器来判断化合物的出峰时间,图1是在254nm下提取的分析物1和分析物2的色谱图,信号很弱。依照二极管整列检测器提取的色谱图,根据连接二极管阵列检测器和荧光检测器的管路体积,推算二者之间死时间约为0.1min。在荧光检测器中调出发射波长3D图,在250-650nm每间隔50nm提取一次色谱图(即250nm,300nm,350nm…),根据紫外色谱图的分析物保留时间,确定荧光色谱图中分析物的出峰时间。http://ng1.17img.cn/bbsfiles/images/2011/12/201112130845_337609_2265735_3.jpg图1 二极管阵列检测器色谱图和提取的分析物紫外吸收色谱图在提取的荧光色谱图中,分析物1有荧光(300nm,图2),而分析物2没有。在荧光检测中,会有很多杂质峰出现(图3,在发射400nm提取的色谱图),而紫外检测器中不一定会发现,利用二极管阵列检测器获得的谱图有利于准确定位分析物在荧光色谱图出现的位置,排除杂质干扰(图3)。http://ng1.17img.cn/bbsfiles/images/2011/12/201112130846_337610_2265735_3.jpg图2 从激发波谱300nm发射光提取的色谱图http://ng1.17img.cn/bbsfiles/images/2011/12/201112130848_337612
1 引 言紫外检测器是高效液相色谱中最常用的检测器,目前市场上生产厂家及型号很多,厂家通常采用检测器的噪音,基线漂移等技术参数作为产品的灵敏度性能评价指标。考虑到样品的紫外吸收响应值主要与样品有关,与仪器的关系不大,一般认为这可以基本反映仪器在灵敏度方面的性能。本文在实验的基础上证明对同一样品各检测器的响应值实际上也存在不同程序的差异,说明仅使用噪音和基线漂移的指标不能准确显示仪器在灵敏度方面的性能差异,因此,提出用信噪比来评价仪器的灵敏度性能。2 灵敏度评价指标设置的目的和依据高效液相色谱及其紫外检测器主要用于化学样品的分析测试。其评价指标必然与其用途相关联。一个分析方法对检测器的要求主要在灵敏度、选择性、精确度和准确性方面。在色谱分析中灵敏度是非常重要的指标。对于灵敏度,在分析测试方法研究中主要使用信噪比、最低检测限,或最低定量限来评价。其中信噪比是评价的核心,因为最低检测限和最低定量限通常用信噪比在2~3和10的量来定义。但目前厂家通常采用检测器的噪音,基线漂移等技术参数作为产品的灵敏度性能评价指标。这实际上是基于样品的紫外吸收响应值主要与样品有关,与仪器关系不大的假设。根据朗伯比尔定律,对于同样长度的检测池,同样浓度的样品溶液应该具有相同的吸光度。这样,对同样浓度的样品溶液,检测器的响应值应该是相同的,所以上述噪音,基线漂移的参数应该可以用来评价检测器的灵敏度性能。但是,实验中发现,同一样品溶液在不同检测器中响应实际上存在明显差异,表1显示对于同一种样品溶液,不同厂家和型号检测器的响应值可能相差3倍以上。这时,由于色谱分析主要使用相对比较的间接测定方法,其使用实际上并没有受到多少影响。难以简单认定仪器存在问题。但因为信噪比发生了变化,上述噪音、基线漂移的参数就不能用来评价检测器的灵敏度性能了。此时,直接使用信噪比来评价检测器的灵敏度性能才是可靠和准确的方法。3 信噪比指标评价方法评价信噪比需要测定响应值,需要选定样品,推荐萘和L-苯丙氨酸等在254nm附近有吸收的样品,前者常用于色谱柱性能评价;后者无毒,且对仪器可能存在的偏振现象敏感。当然,即使使用不同的评价样品,只要固定浓度和溶剂,也可以用分光光度计来校正和比较。根据现有信噪比测定方法,在选定特定浓度的样品后,先在选定波长平衡检测器(此时检测器中的溶液为溶解评价样品的溶剂),待基线稳定后,将配制好的样品溶液直接灌注到仪器的流路并充满其中,注意不要灌入气泡,信号稳定后再用溶剂将样品溶液冲出来。测定基线上下波动的幅度为噪音值(N),测定基线中值与样品信号中值的差为信号值(S)。则信噪比为两者的比值(SN)。4 结 论使用信噪比(SN)指标评价检测器,可以更准确全面地评价各种检测器的灵敏度性能。评价时可以参考现有的信噪比测定方法,建议用254nm作为检测波长,选择简单易得的样品,浓度值的选定应使信噪比SN的值在10以内,以方便测量。配制特定浓度的评价溶液后,以灌注法测定此时相对溶剂的响应值S,测定和计算出信噪比SN的值,作为该检测器对特定评价样品溶液的信噪比评价指标的值。