找寻有关清华大学开发的二维红外相关光谱分析软件
聚甲基丙烯酸叔丁酯薄膜的二维红外相关谱分析[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=151883]聚甲基丙烯酸叔丁酯薄膜的二维红外相关谱分析[/url]
采用二维相关红外技术,并借助于变温过程所跟踪的动态光谱进行分析研究。生川乌和制川乌的一维谱图较相似,而二维红外相关谱则差别较大,在880cm-1和1500cm-1波数范围内,生川乌只在1150cm-1和1080cm-1附近有较强的自动峰;而制川乌除在1150cm-1和1080cm-1附近有较强的自动峰外,并在1220cm-1、1240cm-1和1420cm-1附近有更强的自动峰,而生川乌则相对较弱。因此,凭借二维红外相关谱上的自动峰和交叉峰可以较直观的鉴别生川乌和制川乌,而且还可以揭示其两者相应各官能团的变化规律。该法快速、准确,可为鉴别药材加工后结构的变化规律提供一种新的方法和手段。
以下内容摘自《土壤近红外光谱检测》宋海燕著|化学工业出版社二维相关光谱分析技术提高了光谱分辨率,增强了其对谱图的分辨能力,并在揭示分子内和分子间的相互作用及判断分子中各官能团反应的先后顺序的研究中发挥了重要作用,因此该技术在各个研究领域均得到广泛的应用。如:Krzysztof Zdzislaw Haufa等,采用二维相关近红外光谱分析了不同水分含量对1,2-丙二醇和1,3-丙二醇结构的影响。结果发现在浓度低的时候,OH基团呈明显非结合状态,当浓度高并且位于纯液体状态时,二醇结构就由分子间的氢键决定。Chunli Mo等用二维相关近红外光谱分析了不同水分含量对桑蚕丝素蛋白的影响。结果发现采用近红外光谱结合二维相关光谱技术跟踪分析水丝蛋白结构的动态变化可行。二维相关光谱将谱图信息由一维扩展到了二维,其关注的是困扰引起的细微特征的光谱变化,因此可以解释一维光谱中很难解释的现象,如谱峰重叠或外界干扰下理化指标变化等现象。若能将二维光谱与一维光谱协同分析将会更有助于对被测物质特性的检测和定量分析。

[align=center][b]二维/多维相关光谱方法对热重-红外联用双线性数据的解析[/b][/align][align=center]郭然,徐怡庄[sup]*[/sup][/align][align=center]北京分子科学国家实验室,稀土材料化学及应用国家重点实验室,北京大学化学与分子[/align][align=center]工程学院,北京 100871[/align][b]摘要:[/b]本工作中,使用基于异步正交的二维/多维相关光谱方法对多类热重-红外联用双线性数据进行分析。结果表明,本方法可以有效地处理包含二组分甚至多组分气体逸出物的热重-红外数据,并得到体系中各纯物质光谱。该方法可以有效识别大量体系中某物质的特征吸收峰,且不需预先得知待差减物质谱图,相比于传统的差减法有较明显的优势。[b]关键字:[/b]二维/多维相关光谱 热重-红外联用[b]背景介绍[/b]热重-红外联用方法被广泛地应用于物质成分鉴定、热分解过程考察等相关研究。在常规的热重-红外联用分析中,不同气体逸出物随加热过程逐渐逸出,并通过红外气体池进行检测。然而,气体逸出物的逸出曲线经常会有重合,在某些情况下,逸出曲线甚至会有严重重叠。例如,两气体组分A及B由同一物质分解产生或是具有接近的沸点,则该两物质的逸出曲线会非常接近。气体逸出物逸出曲线的严重重叠,使得在红外检测过程中,只能得到混合物的红外光谱而非各纯物质光谱,这给气体逸出物的鉴定及后续分析造成了很大困难。一般来说,在对红外光谱进行处理,以期得到各纯物质光谱时,可以通过差减法,将光谱中存在的干扰项去除,从而得到目标物质的光谱。该方法的应用一般需要满足以下条件,即需要扣除的物质及其光谱已知。例如,光谱处理中常见的水汽及二氧化碳背景扣除方法,即是基于水汽和二氧化碳光谱已知的前提下,通过选择合适的峰位,找出差减的比例系数,从而将水汽及二氧化碳光谱从总光谱中移除。然而,随着总光谱复杂程度的加剧,干扰光谱鉴定的物质不仅是水和二氧化碳,而可能包含各类未知且具有不同光谱形状的气体逸出物,单纯进行水和二氧化碳的扣除,对很多体系的分析而言是远远不够的。即使是二氧化碳的扣除,差减法也存在一定问题。在中红外区,二氧化碳的谱峰主要存在于2350cm[sup]-1[/sup]-2200cm[sup]-1[/sup]的光谱区段。由于很少有气体产物在该光谱区段存在吸收峰,目前的二氧化碳扣除算法可以将该区段谱峰全部扣去。然而,实际体系中存在一些物质,在该光谱区段具有具红外活性的振动模式(如乙腈的C≡N三键伸缩振动)。当这些物质对总光谱有贡献时,差减法很难恰好将二氧化碳的成分准确扣除,从而导致得到的谱峰变形,影响后续的数据分析。本工作中,使用本课题组开发的二维/多维相关光谱方法对多类物质的热重-红外数据进行处理,以期得到各纯物质光谱。[b]算法简要介绍[/b]二维及多维异步谱的构建基于以下算法:[align=center] [img=,492,106]https://ng1.17img.cn/bbsfiles/images/2018/09/201809051625044178_4191_3237657_3.jpg!w492x106.jpg[/img][/align]式中,为物质k在[i]t[/i][sub]i[/sub]时刻的逸出浓度,为物质k在[i]v[/i][sub]j[/sub]处的红外吸收,N为Hilbert-Noda变换矩阵。通过基于Hilbert-Noda变换矩阵的异步相关乘法,构建二维异步谱。在异步谱上通过寻找特征性的系统缺峰,得到一级特征峰的吸收信息,并由该处的异步谱截线,得到各纯物质的光谱形状。构建多维异步谱时,在构建二维异步谱方式的基础上,对原始一维光谱进行多级分组,在二维异步谱上取各组相同位置的截线,进行基于公式(2)的高维异步谱构建。可以证明,通过异步光谱的升维算法,可以将体系中各成分对于光谱的贡献逐一去除,进而不断简化光谱形式,最终得到纯物质光谱。通过选择不同的升维路径,可以通过选择不同的特定吸收峰,去除不同成分对总光谱的贡献,从而得到不同的物质光谱(证明略)。本方法已应用在多类体系中,并成功得到了体系中各纯物质红外光谱。下面给出一个应用实例。[b]实验条件[/b]仪器:TGA(TGA-8000)-FTIR (Frontier) 联用仪器 (Perkin Elmer);样品:去离子水、乙腈、乙酸乙酯。实验步骤:配制水/乙腈/乙酸乙酯混合溶液(v:v:v=1:4:1)上样于坩埚,以30℃为起始温度,10℃/min速度升温至90℃,30℃/min升温至150℃。红外光谱采集:分辨率8cm[sup]-1[/sup],每张光谱采集时间约2.7s。[b]结果讨论[/b]水、乙腈、乙酸乙酯三组分的沸点相差不大,通过上述算法,可以将体系中各成分逐级去除,最终得到三组分各自的纯物质光谱。[align=center][b] [img=,690,626]https://ng1.17img.cn/bbsfiles/images/2018/09/201809051625227884_5273_3237657_3.jpg!w690x626.jpg[/img][/b][/align][align=center]图1 基于三维异步相关方法的水/乙腈/乙酸乙酯混合物热重-红外联用数据分析 (A) 二维异步相关谱 (B) 三维异步谱在x=3746cm[sup]-1[/sup]处的二维截面 (C) 三维异步谱在x=2620cm[sup]-1[/sup]处的二维截面 (D) Trace 1-图(B)在y=2620cm[sup]-1[/sup]处的截线,对应乙酸乙酯光谱(Trace 4);(Trace 2)图(B)在y=1768cm[sup]-1[/sup]处的截线,对应乙腈光谱(Trace 5);(Trace 3)图(C)在y=2982cm[sup]-1[/sup]处的截线,对应水光谱(Trace 6)[/align][b]致谢[/b]本工作由国家自然科学基金(No.51373003)赞助。
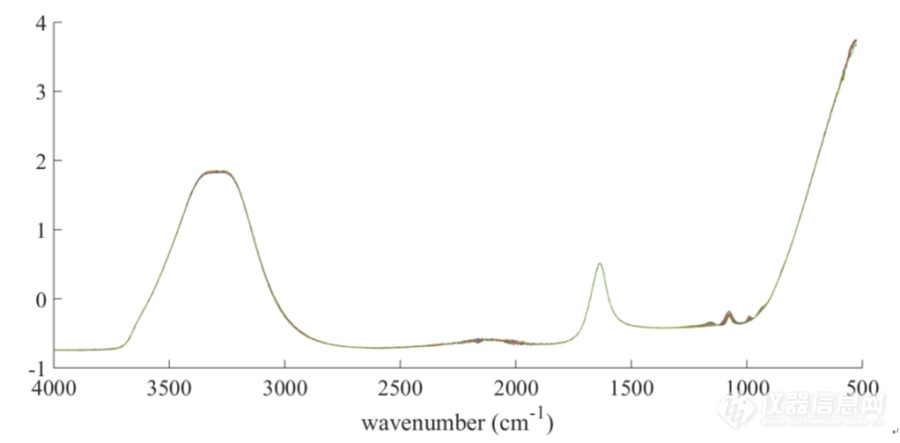
[align=center][b][/b][/align][align=center][b]二维相关分析用于pH引起的人血清白蛋白二级结构变化的研究[/b][/align]采用二维/衰减全发射红外光谱的分析技术对HSA在不同pH的缓冲体系下二级结构变化的研究,根据吸收峰发生变化的顺序的不同,解释蛋白质的变化过程。通过配制不同pH的缓冲溶液,与HSA混合得HSA-缓冲溶液的体系,利用中红外光谱分析技术对以缓冲溶液为背景,HSA-缓冲溶液体系为样品进行光谱的采集,并对HSA的结构的动态变化进行分析处理。[b][color=windowtext]4.1[/color][color=windowtext]实验仪器与试剂[/color][color=windowtext]4.[/color][color=windowtext]1.[/color][color=windowtext]1[/color][color=windowtext]实验[/color][color=windowtext]仪器[/color][color=windowtext]与软件[/color][/b][align=center][color=windowtext]表[/color][color=windowtext]4-1 [/color][color=windowtext]实验仪器与软件[/color][/align] [table=568][tr][td] [align=center][color=windowtext]仪器[/color][color=windowtext]/[/color][color=windowtext]软件[/color][/align] [/td][td] [align=center][color=windowtext]规格与型号[/color][/align] [/td][td] [align=center][color=windowtext]生产厂家[/color][/align] [/td][/tr][tr][td] [align=center][color=windowtext]电子分析天平[/color][/align] [/td][td] [align=center][color=windowtext]ME54E[/color][/align] [/td][td] [align=center][color=windowtext]梅特勒[/color][color=windowtext]-[/color][color=windowtext]托利多仪器股份有限公司[/color][/align] [/td][/tr][tr][td] [align=center][color=windowtext]磁力搅拌器[/color][/align] [/td][td] [align=center][color=windowtext]温控型[/color][/align] [/td][td] [align=center][color=windowtext]巩义市予华仪器有限责任公司[/color][/align] [/td][/tr][tr][td] [align=center][color=windowtext]pH[/color][color=windowtext]计[/color][/align] [/td][td] [align=center][color=windowtext]FE20[/color][color=windowtext]型[/color][/align] [/td][td] [align=center][color=windowtext]梅特勒[/color][color=windowtext]-[/color][color=windowtext]托利多仪器(上海)有限公司[/color][/align] [/td][/tr][tr][td] [align=center][color=windowtext][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url][/color][/align] [/td][td] [align=center][color=windowtext]1000μL[/color][color=windowtext]、[/color][color=windowtext]100μL[/color][/align] [/td][td] [align=center][color=windowtext]美国[/color][color=windowtext]Thermo Fisher[/color][color=windowtext]公司[/color][/align] [/td][/tr][tr][td] [align=center][color=windowtext]容量瓶[/color][/align] [/td][td] [align=center][color=windowtext]500mL[/color][/align] [/td][td] [align=center][color=windowtext]四川蜀牛玻璃仪器厂[/color][/align] [/td][/tr][tr][td] [align=center][color=windowtext]烧杯[/color][/align] [/td][td] [align=center][color=windowtext]500mL[/color][color=windowtext]、[/color][color=windowtext]50mL[/color][/align] [/td][td] [align=center][color=windowtext]四川蜀牛玻璃仪器厂[/color][/align] [/td][/tr][tr][td] [align=center][color=windowtext]傅里叶变换红外[/color][color=windowtext]/[/color][color=windowtext]拉曼联用光谱仪[/color][/align] [/td][td] [align=center][color=windowtext]NXR FT-RAMAN[/color][color=windowtext]型[/color][color=windowtext]6700FT-TR[/color][/align] [/td][td] [align=center][color=windowtext]美国[/color][color=windowtext]Nicolet[/color][color=windowtext]公司[/color][/align] [/td][/tr][tr][td] [align=center][color=windowtext]MATLAB[/color][color=windowtext]数据处理软件[/color][/align] [/td][td] [align=center][color=windowtext]2015a[/color][/align] [/td][td] [align=center][color=windowtext]美国[/color][color=windowtext]Mathworks[/color][color=windowtext]公司[/color][/align] [/td][/tr][/table][b][color=windowtext]4.[/color][color=windowtext]1.[/color][color=windowtext]2[/color][color=windowtext]实验材料与[/color][color=windowtext]试剂[/color][/b][align=center][color=windowtext]表[/color][color=windowtext]4-2 [/color][color=windowtext]实验材料与试剂[/color][/align] [table=568][tr][td][color=windowtext]试剂[/color][color=windowtext]/[/color][color=windowtext]材料[/color][/td][td][color=windowtext]规格[/color][color=windowtext]/[/color][color=windowtext]批号[/color][/td][td][color=windowtext]生产厂家[/color][/td][/tr][tr][td][color=windowtext]人血[/color][color=windowtext]清[/color][color=windowtext]白蛋白[/color][color=windowtext]([/color][color=windowtext]Albumin human[/color][color=windowtext])[/color][/td][td][color=windowtext]A9731-5G[/color][/td][td][color=windowtext]S[/color][color=windowtext]igma[/color][color=windowtext]-A[/color][color=windowtext]ldrich[/color][color=windowtext]公司[/color][/td][/tr][tr][td][color=windowtext]二水合[/color][color=windowtext]磷酸二氢钠[/color][/td][td][color=windowtext]分析纯[/color][/td][td][color=windowtext]国药集团化学试剂有限公司[/color][/td][/tr][tr][td][color=windowtext]十二水合[/color][color=windowtext]磷酸氢二钠[/color][/td][td][color=windowtext]分析纯[/color][/td][td][color=windowtext]国药集团化学试剂有限公司[/color][/td][/tr][tr][td][color=windowtext]磷酸[/color][/td][td][color=windowtext]分析纯[/color][/td][td][color=windowtext]国药集团化学试剂有限公司[/color][/td][/tr][/table][b][color=windowtext]4.2 [/color][color=windowtext]实验[/color][color=windowtext]内容[/color][color=windowtext]4.[/color][color=windowtext]2[/color][color=windowtext].[/color][color=windowtext]1 [/color][color=windowtext]样品的[/color][color=windowtext]配制[/color][/b](1)不同pH缓冲液的配制用磷酸配制0.2mol/L磷酸溶液作为A液,用十二水合磷酸氢二钠配制0.2mol/L磷酸氢二钠溶液作为B液。pH计测得A液pH为1.34,B液pH为9.07。利用上述的A液和 B液配制不同pH的缓冲液,配制pH为3.0、3.2、3.4、3.6、3.8、4.0、4.2、4.4、4.6、4.8、5.0、5.2、 5.4、5.6、 5.8、6.0、6.2、6.4、6.6、6.8、7.0、7.2的22个不同pH的缓冲溶液,放入到EP管中备用。(2)样品的配制磷酸盐溶液二元体系:取以上22个不同pH的缓冲液中800μL于EP管中,再加入200μL的双蒸水,充分混匀。HSA的磷酸盐溶液三元体系:依次用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]吸取上述22个混合样品800 μL分别加入到不同的EP管中,称取HSA 0.450 g充分溶解后,再分别向各管加入200μL的HSA溶液,充分混匀,所得三元体系HSA的浓度为30mg/mL。[b]4.2.2光谱的采集与处理[/b](1)中红外光谱谱图采集利用仪器傅里叶变换红外/拉曼联用光谱仪(NXRFT-RAMAN型,6700FT-TR,美国Nicolet公司)、金刚石ATR采样附件(Golden Gate ATR),采集中红外光谱,4000-500cm[sup]-1[/sup],2cm[sup]-1[/sup]分辨率,64次扫描,温度为室温(26℃),以空气为背景进行扫描,作为背景光谱,采集不同pH条件下HSA溶液的中红外光谱。(2)二维相关分析利用傅里叶变换红外/拉曼联用光谱仪测得的中红外光谱用MATLAB 2015a软件进行处理得到与pH相关的动态图谱—二维等高图,对所得的二维等高图进行二维相关的处理,计算出二维同步与异步矩阵,并得到二维同步谱图与二维异步谱图。分析二维同步谱图,谱图为主对角线对称图,相关峰出现在对角线上,为正值;交叉峰则出现在非对角线区域,可正可负。[b][color=windowtext]4.3 [/color][color=windowtext]实验结果与讨论[/color][/b][color=windowtext]([/color][color=windowtext]1[/color][color=windowtext])[/color][color=windowtext]H[/color][color=windowtext]SA [/color][color=windowtext]磷酸盐[/color][color=windowtext]溶液[/color][color=windowtext]中红外光谱图预处理结果与分析[/color][color=windowtext]图[/color][color=windowtext]4-1[/color][color=windowtext]为[/color][color=windowtext]pH 3.0[/color][color=windowtext]-[/color][color=windowtext]7.2[/color][color=windowtext]的[/color][color=windowtext]HSA [/color][color=windowtext]磷酸盐[/color][color=windowtext]溶液的经过[/color][color=windowtext]SNV[/color][color=windowtext]处理之后的光谱图[/color][color=windowtext],[/color][color=windowtext]SNV[/color][color=windowtext]与标准化算法计算公式相同,但不同之处是标准化算法是对一组光谱进行处理,而[/color][color=windowtext]SNV[/color][color=windowtext]是对一条光谱进行处理[/color][color=windowtext]。[/color][color=windowtext]进行[/color][color=windowtext]SNV[/color][color=windowtext]处理的主要目的是消除光谱的基线漂移的影响。[/color][align=center][img=,690,339]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131726099980_5308_3237657_3.png!w690x339.jpg[/img][/align][align=center][color=windowtext]图[/color][color=windowtext]4-1pH 3.0[/color][color=windowtext]-[/color][color=windowtext]7.2[/color][color=windowtext]的[/color][color=windowtext]HSA [/color][color=windowtext]磷酸盐[/color][color=windowtext]溶液的经过[/color][color=windowtext]SNV[/color][color=windowtext]处理之后的光谱图[/color][/align]在本章的研究中,主要考察HSA酰胺I区和酰胺II区结构的光谱变化,即1750-1580cm[sup]-1[/sup],图4-2所示从上到下依次为pH7.0、pH4.8、pH4.0和pH3.0的HSA的原始光谱减去对应pH缓冲液的光谱后得到的差谱图,进行差谱的主要目的是扣除水与缓冲盐对光谱的影响。从图中可以看到在酰胺I段在1653cm[sup]-1[/sup]具有明显的吸收峰,这个吸收峰可以归属为α-螺旋的吸收峰,并且在pH下降到3.0时,α-螺旋的特征峰变化较为明显,与pH7.0、pH4.8、pH4.0的光谱图在1653cm[sup]-1[/sup]不一样,吸收峰有所下降,形状也有一定程度的变化。推测在较低的pH条件下,HSA的α-螺旋结构遭到了破坏,因此发生了一定的结构变化。[align=center][img=,690,334]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131726229783_6130_3237657_3.png!w690x334.jpg[/img][/align][align=center]图4-2 HSA 磷酸盐溶液在波长为1750-1580cm[sup]-1[/sup]段的差谱图[/align]图4-3所示为 pH7.0-3.0范围的的HSA的连续小波变换(CWT)光谱,连续小波变化的目的是提高光谱分辨率。CWT应用的关键是选择合适的小波基与小波尺度,参数设置合理时,CWT在扣除无用信息的同时,可以提取出光谱中的有效信息。本章中使用了“Sym2”小波基和20小波尺度获得平滑效果以得到更高的分辨率。可以看出经过小波变换之后,光谱信息得到进一步的分辨,pH7.0下HSA可以保持天然结构,随着pH的降低,可以明显看大部分结构都发生了变化,某些吸收峰甚至消失。[align=center][img=,690,404]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131726350596_917_3237657_3.png!w690x404.jpg[/img][/align][align=center]图4-3 pH7.0-3.0范围的的HSA的连续小波变换光谱[/align]如表4-3所示,是在中红外光谱中,对蛋白质HSA分辨出的一些主要吸收峰进行了结构归属,可以辅助研究不同pH对蛋白质HSA的结构变化的影响。[align=center]表4-3 HSA的分辨出主要吸收峰[/align] [table=568][tr][td] [align=center]峰的波数(cm-1)[/align] [/td][td] [align=center]归属情况[/align] [/td][/tr][tr][td] [align=center] 1745[/align] [/td][td] [align=center]自由COOH基团[/align] [/td][/tr][tr][td] [align=center]1732/1722[/align] [/td][td] [align=center]半氢键结合的COOH基团[/align] [/td][/tr][tr][td] [align=center]1711[/align] [/td][td] [align=center]弱氢键结合的COOH基团[/align] [/td][/tr][tr][td] [align=center]1702[/align] [/td][td] [align=center]中等强度氢键结合的COOH基团[/align] [/td][/tr][tr][td] [align=center]1695[/align] [/td][td] [align=center]强氢键结合的COOH基团[/align] [/td][/tr][tr][td] [align=center]1680[/align] [/td][td] [align=center]β-转角[/align] [/td][/tr][tr][td] [align=center]1667[/align] [/td][td] [align=center]β-转角[/align] [/td][/tr][tr][td] [align=center]1653[/align] [/td][td] [align=center]α-螺旋[/align] [/td][/tr][tr][td] [align=center]1625[/align] [/td][td] [align=center]β-折叠链[/align] [/td][/tr][tr][td] [align=center]1613[/align] [/td][td] [align=center]Side chains[/align] [/td][/tr][tr][td] [align=center]1598[/align] [/td][td] [align=center]COO[sup]-[/sup][/align] [/td][/tr][/table][color=windowtext]([/color][color=windowtext]2[/color][color=windowtext])[/color][color=windowtext]pH 7[/color][color=windowtext].[/color][color=windowtext]2-5[/color][color=windowtext].[/color][color=windowtext]0[/color][color=windowtext]范围内[/color][color=windowtext]HSA[/color][color=windowtext]磷酸盐溶液[/color][color=windowtext]中红外[/color][color=windowtext]光谱的二维相关[/color][color=windowtext]分析[/color]由于在酰胺I区和酰胺II区能代表蛋白质HSA二级结构的吸收峰有重叠,在图4-1、图4-2、图4-3中能表示HSA的二级结构的信息不够详细,又因为二维红外光谱分析能提高图谱的分辨率,所以对不同pH下HSA磷酸盐溶液与磷酸盐溶液的差谱进行二维红外光谱分析。图4-4为pH 7.2-5.0范围内HSA磷酸盐溶液对应的二维相关同步谱(左)和异步谱(右),其中虚线部分为负相关,实线现部分为正相关。从图中可以看出,各吸收峰之间在HSA的质子化过程中具有高度的协同性。[align=center][img=,690,327]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131726485419_7489_3237657_3.png!w690x327.jpg[/img][/align][align=center]图4-4 pH 7.2-5.0范围内HSA磷酸盐溶液的二维相关同步谱(左)和异步谱(右),横、纵坐标均为波数Wavenumber(cm[sup]-1[/sup])[/align]在图4-4的同步谱中,除以上表4-4中得到的特征吸收峰外,另外可以辨识出的峰还包括1637cm[sup]-1[/sup],可以归属为β-strand。HSA中包括98个酸性侧链,包括36个天冬氨酸残基和62个谷氨酸残基和100个含有24个精氨酸、59个赖氨酸和17个组氨酸的侧链结构。在pH= 4.3的溶液中,大约有一半的天冬氨酸和谷氨酸酸性侧链基团发生质子化,因此推测,在pH从7.0到5.0过程中,羧基基团逐渐经历质子活化过程,将1732cm[sup]-1[/sup]和1722cm[sup]-1[/sup]归属为介于自由羧基和弱氢键结合的羧基之间的的半氢键结合状态的羧基基团。Noda规则为一段波长范围内出现异步相关光谱,说明该区域有重叠峰,但在同步谱中该位置没有明显的同步交叉峰,此时同步谱图中同步交叉相关的强度变化是越靠近峰位置中心其相关强度越小,表明峰强度变化方向是反向,而强度一个是增加的情况,另一个则是减小的情况。表4-2为根据Noda规则,已分辨出的吸收峰的变化顺序。[align=center]表4-4 根据同步谱/异步谱得到的交叉峰信息及根据Noda原则得出的pH7.2-5.0的范围内可以分辨的吸收峰的变化顺序[/align] [table=568][tr][td] [align=center]峰(cm[sup]-1[/sup])[/align] [/td][td] [align=center]Ф[/align] [/td][td] [align=center]ψ[/align] [/td][td] [align=center]变化顺序[/align] [/td][/tr][tr][td] [align=center]1739,1628[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1628>1739[/align] [/td][/tr][tr][td] [align=center]1716,1628[/align] [/td][td] [align=center]0[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]—[/align] [/td][/tr][tr][td] [align=center]1739, 1682[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1739>1682[/align] [/td][/tr][tr][td] [align=center]1682,1671[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1682>1671[/align] [/td][/tr][tr][td] [align=center]1671,1653[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1653>1671[/align] [/td][/tr][tr][td] [align=center]1682,1653[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1653>1682[/align] [/td][/tr][tr][td] [align=center]1739,1653[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1739>1653[/align] [/td][/tr][tr][td] [align=center]1716,1653[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1716>1653[/align] [/td][/tr][tr][td] [align=center]1727,1653[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1727>1653[/align] [/td][/tr][tr][td] [align=center]1700,1653[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1700>1653[/align] [/td][/tr][tr][td] [align=center]1671,1609[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1609>1671[/align] [/td][/tr][tr][td] [align=center]1637,1609[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1609>1637[/align] [/td][/tr][tr][td] [align=center]1682,1609[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1682>1609[/align] [/td][/tr][tr][td] [align=center]1671,1624[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1624>1671[/align] [/td][/tr][tr][td] [align=center]1624,1609[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1609>1624[/align] [/td][/tr][tr][td] [align=center]1671,1594[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1594>1671[/align] [/td][/tr][tr][td] [align=center]1682,1594[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1682>1594[/align] [/td][/tr][tr][td] [align=center]1609,1594[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1609>1594[/align] [/td][/tr][tr][td] [align=center]1624,1594[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1594>1624[/align] [/td][/tr][tr][td] [align=center]1653,1594[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1653>1594[/align] [/td][/tr][tr][td] [align=center]1653,1637[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1653>1637[/align] [/td][/tr][tr][td] [align=center]1637,1609[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1609>1637[/align] [/td][/tr][tr][td] [align=center]1637,1594[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1594>1637[/align] [/td][/tr][tr][td] [align=center]1637,1624[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1624>1637[/align] [/td][/tr][tr][td] [align=center]1671,1637[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1637>1671[/align] [/td][/tr][/table]由表4-4可得: 1739cm[sup]-1[/sup](自由COOH基团)、1727cm[sup]-1[/sup](半氢键结合的COOH基团)、1716cm[sup]-1[/sup](弱氢键结合的COOH基团)>1653cm[sup]-1[/sup](α-螺旋)>1682cm[sup]-1[/sup](β-转角)>1609cm[sup]-1[/sup](Side chains)>1594cm[sup]-1[/sup](COO[sup]-[/sup])>1624cm[sup]-1[/sup](β-折叠链)>1637cm[sup]-1[/sup](β-strand)>1671cm[sup]-1[/sup](β-转角)。因此除1653cm[sup]-1[/sup]目前在文献中其余的均无归属,此处因峰强度较小可以忽略;异步谱交叉峰峰强度很弱,因此,HSA的异步光谱表明羧基组的氢键的变化先于二级结构变化,二级结构的变化顺序为;先是α-螺旋,其次是高波长β-转角、酪氨酸侧链、β-折叠链、β-股、低波长β-转角。所以,pH(7.2-5.0)在较高情况下,COOH对pH的敏感性要高于α-螺旋结构的敏感性。(3)pH 5.2-4.4范围内HSA磷酸盐溶液中红外光谱的二维相关分析图4-7为pH5.2-4.4范围内的二维相关同步谱(左)和异步谱(右),其中虚线部分为负相关,实线部分为正相关。从图中可以看出,各吸收峰之间在HSA的质子化过程中具有高度的协同性。[align=center][img=,690,321]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131727525262_7281_3237657_3.png!w690x321.jpg[/img][/align][align=center]图4-5 pH5.2-4.4范围内的二维相关同步谱(左)和异步谱(右),横、纵坐标均为波数Wavenumber(cm[sup]-1[/sup])[/align][align=center]表4-5 根据同步谱/异步谱得到的交叉峰信息及根据Noda原则得出的pH5.2-4.4的范围内可以分辨的吸收峰的变化顺序[/align] [table=568][tr][td] [align=center]峰的波数(cm[sup]-1[/sup])[/align] [/td][td] [align=center]Ф[/align] [/td][td] [align=center]ψ[/align] [/td][td] [align=center]变化顺序[/align] [/td][/tr][tr][td] [align=center]1733,1720[/align] [/td][td] [align=center]0[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]—[/align] [/td][/tr][tr][td] [align=center]1720,1653[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1720>1653[/align] [/td][/tr][tr][td] [align=center]1697,1653[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1697>1653[/align] [/td][/tr][tr][td] [align=center]1653,1607[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1653>1607[/align] [/td][/tr][tr][td] [align=center]1607,1591[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1591>1607[/align] [/td][/tr][tr][td] [align=center]1653,1591[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1591>1653[/align] [/td][/tr][tr][td] [align=center]1697,1591[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1697>1591[/align] [/td][/tr][tr][td] [align=center]1626,1607[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1607>1626[/align] [/td][/tr][tr][td] [align=center]1636,1626[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1636>1626[/align] [/td][/tr][tr][td] [align=center]1607,1636[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1636>1607[/align] [/td][/tr][tr][td] [align=center]1636,1626[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1636>1626[/align] [/td][/tr][tr][td] [align=center]1653,1636[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1653>1636[/align] [/td][/tr][tr][td] [align=center]1671,1626[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1671>1626[/align] [/td][/tr][tr][td] [align=center]1671,1653[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1671>1653[/align] [/td][/tr][tr][td] [align=center]1671,1591[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1591>1671[/align] [/td][/tr][/table]由表4-5得:1733cm[sup]-1[/sup](半氢键结合的COOH基团)、1720cm[sup]-1[/sup](半氢键结合的COOH基团)、1715cm[sup]-1[/sup](弱氢键结合的COOH基团)>1697cm[sup]-1[/sup](强氢键结合的COOH基团)>1591cm[sup]-1[/sup](COO[sup]-[/sup])>1671cm[sup]-1[/sup](β-转角)>1653cm[sup]-1[/sup](α-螺旋)>1636cm[sup]-1[/sup](β-折叠链)>1626cm[sup]-1[/sup](β-折叠链)>1607cm[sup]-1[/sup](Side chains)>1626cm[sup]-1[/sup]、1671cm[sup]-1[/sup](β-转角)。因此pH 为5.2-4.4时,HSA的异步光谱表明羧基组的氢键的变化先于二级结构变化,即在该pH范围内,羧基对pH 变化的敏感性要高于α-螺旋的敏感性。(4)pH4.6-3.8范围内HSA磷酸盐溶液中红外光谱的二维相关分析图4-6为pH4.6-3.8范围内的二维相关同步谱(左)和异步谱(右)其中虚线部分为负相关,实线部分为正相关。从图中可以看出,各吸收峰之间在HSA的质子化过程中具有高度的协同性。[align=center][img=,690,315]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131728232083_9380_3237657_3.png!w690x315.jpg[/img][/align][align=center]图4-6pH4.6-3.8范围内的二维相关同步谱(左)和异步谱(右),横、纵坐标均为波数Wavenumber(cm[sup]-1[/sup])[/align][align=center]表4-6 根据同步谱/异步谱得到的交叉峰信息及根据Noda原则得出的pH4.6-3.8的范围内可以分辨的吸收峰的变化顺序[/align] [table=568][tr][td] [align=center]峰的波数(cm[sup]-1[/sup])[/align] [/td][td] [align=center]Ф[/align] [/td][td] [align=center]ψ[/align] [/td][td] [align=center]变化顺序[/align] [/td][/tr][tr][td] [align=center]1697,1677[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1697>1677[/align] [/td][/tr][tr][td] [align=center]1677,1668[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1677>1668[/align] [/td][/tr][tr][td] [align=center]1668,1648[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1648>1668[/align] [/td][/tr][tr][td] [align=center]1677,1648[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1677>1648[/align] [/td][/tr][tr][td] [align=center]1668,1636[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1636>1668[/align] [/td][/tr][tr][td] [align=center]1648,1636[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1648>1636[/align] [/td][/tr][tr][td] [align=center]1668,1636[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1636>1668[/align] [/td][/tr][tr][td] [align=center]1668,1682[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1668>1682[/align] [/td][/tr][tr][td] [align=center]1682,1611[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1611>1682[/align] [/td][/tr][tr][td] [align=center]1668,1611[/align] [/td][td] [align=center]0[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]—[/align] [/td][/tr][tr][td] [align=center]1636,1611[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1636>1611[/align] [/td][/tr][tr][td] [align=center]1611,1682[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1682>1611[/align] [/td][/tr][tr][td] [align=center]1682,1636[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1636>1682[/align] [/td][/tr][tr][td] [align=center]1611,1604[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]0[/align] [/td][td] [align=center]可能来自于同一基团[/align] [/td][/tr][/table]由表4-6得:1738cm[sup]-1[/sup](半氢键结合的COOH基团)、1729cm[sup]-1[/sup](半氢键结合的COOH基团)、1718cm[sup]-1[/sup](弱氢键结合的COOH基团)、1697cm[sup]-1[/sup](强氢键结合的COOH基团]>1677cm[sup]-1[/sup](β-转角)>1648cm[sup]-1[/sup](random coil)>1636cm[sup]-1[/sup](β-strand)>1682cm[sup]-1[/sup](β-转角)>1668cm[sup]-1[/sup](β-转角)、1611cm[sup]-1[/sup](Side chains)、1604cm[sup]-1 [/sup](COO[sup]-[/sup])。由上顺序得,HSA的异步光谱表明羧基组的氢键的变化先于二级结构变化,二级结构的变化顺序为:中波长β-转角、无卷曲构象、β-strand、高波长β-转角、低波长β-转角、酪氨酸残基。因此,pH在4.6-3.8范围内羧基组的氢键对pH的敏感性要高于无卷曲构象、β-strand,但羧基对pH的敏感性要低于无卷曲构象、β-strand。又因异步谱交叉峰峰强度很弱,所以1738cm[sup]-1[/sup]、1729cm[sup]-1[/sup]、1718cm[sup]-1[/sup]、1697cm[sup]-1[/sup]的顺序相当,1668cm[sup]-1[/sup]、1611cm[sup]-1[/sup]、1604cm[sup]-1[/sup]的顺序相当。(5)pH3.8-3.0范围内HSA磷酸盐溶液中红外光谱的二维相关分析[align=center][img=,690,308]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131729083359_5528_3237657_3.png!w690x308.jpg[/img][/align][align=center]图4-7 pH3.8-3.0范围内的二维相关同步谱(左)和异步谱(右),横、纵坐标均为波数Wavenumber(cm[sup]-1[/sup])[/align]图4-7为pH3.8-3.0范围内的二维相关同步谱(左)和异步谱(谱),其中虚线部分为负相关,实现部分为正相关,在异步谱中,仍可分辨出部分的吸收峰,包括1743cm[sup]-1[/sup],1730cm[sup]-1[/sup],1706cm[sup]-1[/sup],1699cm[sup]-1[/sup].与整个的酰胺I和酰胺II区分别形成强的正相关和负相关和正相关和负相关,说明在强酸环境中,羧基组的氢键形成要比其他pH条件范围快得多。[align=center][img=,690,365]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131729231532_818_3237657_3.png!w690x365.jpg[/img][/align][align=center]图4-8 pH3.8-3.0范围内的同步谱的透射图,x、y轴均为波数Wavenumber(cm[sup]-1[/sup]),z轴为相对强度)[/align][align=center][img=,690,322]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131729358095_7590_3237657_3.png!w690x322.jpg[/img][/align][align=center]图4-9pH3.8-3.0范围内的异步谱的透射图,x、y轴均为波数Wavenumber(cm[sup]-1[/sup]),z轴为相对强度[/align]在图4-8pH3.8-3.0范围内的同步谱的透射图、图4-9pH3.8-3.0范围内的异步谱的透射图中可以看到,1618cm[sup]-1[/sup]出现强的自动峰,而其他峰因为1618cm[sup]-1[/sup]信号较强而被掩盖掉。1618cm[sup]-1[/sup]可归属为蛋白侧链基团。可以得知,占HSA67%的α-螺旋结构在强酸环境中遭到破坏,吸收峰基本消失。[align=center]表4-7 根据同步谱/异步谱得到的交叉峰信息及根据Noda原则得出的pH3.8-3.0的范围内可以分辨的吸收峰的变化顺序[/align] [table=568][tr][td] [align=center]峰的波数(cm-1)[/align] [/td][td] [align=center]Ф[/align] [/td][td] [align=center]ψ[/align] [/td][td] [align=center]变化顺序[/align] [/td][/tr][tr][td] [align=center]1656,1648[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1656>1648[/align] [/td][/tr][tr][td] [align=center]1648,1640[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1640>1648[/align] [/td][/tr][tr][td] [align=center]1656,1640[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]0[/align] [/td][td] [align=center]—[/align] [/td][/tr][tr][td] [align=center]1648,1633[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1633>1648[/align] [/td][/tr][tr][td] [align=center]1656,1633[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1656>1633[/align] [/td][/tr][tr][td] [align=center]1648,1614[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1614>1648[/align] [/td][/tr][tr][td] [align=center]1633,1614[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1614>1633[/align] [/td][/tr][tr][td] [align=center]1656,1614[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1614>1656[/align] [/td][/tr][tr][td] [align=center]1648,1602[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1602>1648[/align] [/td][/tr][tr][td] [align=center]1656,1602[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1656>1602[/align] [/td][/tr][tr][td] [align=center]1633,1602[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]1602>1633[/align] [/td][/tr][tr][td] [align=center]1656,1589[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1589>1656[/align] [/td][/tr][tr][td] [align=center]1614,1589[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1589>1614[/align] [/td][/tr][tr][td] [align=center]1656,1648[/align] [/td][td] [align=center]+[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]1633>1648[/align] [/td][/tr][/table]由表4-7可知1691cm[sup]-1[/sup]、1648cm[sup]-1[/sup]、1669cm[sup]-1[/sup]、1656cm[sup]-1[/sup]、1648cm[sup]-1[/sup]、1640cm[sup]-1[/sup]、1633cm[sup]-1[/sup]、1614cm[sup]-1[/sup]、1602cm[sup]-1[/sup]、1589cm[sup]-1[/sup]、1743cm[sup]-1[/sup](自由COOH基团)、1730cm[sup]-1[/sup](半氢键结合的COOH基团)、1706cm[sup]-1[/sup](中等强度氢键结合的COOH基团)、1699cm[sup]-1[/sup](中等强度氢键结合的COOH基团)>1589cm[sup]-1[/sup](COO[sup]-[/sup])>1614cm[sup]-1[/sup](Side chains)> 1656cm[sup]-1[/sup](α-螺旋)、1640cm[sup]-1[/sup](α-螺旋)>1602cm[sup]-1[/sup](Side chains)>1633cm[sup]-1[/sup](β-折叠链)>1648cm[sup]-1[/sup](random coil)。pH为3.8-3.0时,HSA的异步光谱表明羧基组的氢键的变化先于二级结构的变化,首先是α-螺旋,其次是酪氨酸残基,β-折叠链等。因此,在pH 3.8-3.0的范围内,羧基对pH的敏感性要高于α-螺旋的敏感性。[align=center][img=,690,335]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131729514171_7621_3237657_3.png!w690x335.jpg[/img][/align][align=center]图4-10不同pH段的二维相关同步谱的能量谱,a、b、c、d四个谱图依次为pH7.2-5.0,5.2-4.4,4.6-3.8,3.8-3.0范围二维相关同步能量谱图[/align]从图4-10中可以看出在这四个pH段的光谱特征具有明显的区别,这些差异意味着在不同的pH条件下HSA的结构发生了明显不同的改变。从图4-11中可以明显看出在不同的pH中蛋白结构发生明显的变化。[align=center][img=,690,492]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131730224583_14_3237657_3.png!w690x492.jpg[/img][/align][align=center]图4-11对异步谱中的1653cm[sup]-1[/sup]的异步谱进行提取的图谱,从上到下依次为pH7.2-5.0、5.2-4.4、4.6-3.8、3.8-3.0范围对异步谱中的1653cm[sup]-1[/sup]的异步谱进行提取图谱[/align][b]4.4结论[/b]本章内容通过广义二维相关红外光谱探究了HSA在酸性条件下解折叠的过程,同步谱和异步相关谱提供了详细的光谱变化。二维相关光谱不仅提供了二级结构的变化信息,并且也能表征羧基基团和侧链结构的变化。在分析中可以看出有至少四种不同氢键结合程度的羧基基团参与了结构变化过程中,在不同的pH范围,均是由羧基结构先发生变化,因此推测在酸性环境中羧基基团的质子化可能是诱发蛋白结构发生变化的重要原因。且在不同pH范围内HSA的二级结构发生变化的过程中,吸收峰发生变化的顺序有所不同。二维相关技术的应用有助于解释蛋白质的变化过程,具有独特的优势。此外,异步谱的应用,可以提供更多的蛋白结构变化信息。虽然分析中得到了谱图相关强度,但是因为有些信号较弱,且差谱之后噪音的存在,这些峰变化的先后的准确性仍需要进一步的确定。此外,应用[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]分析技术结合中红外光谱分析技术对pH引起的体系变化仍需要进一步探索,以相互补充和印证。
求助Noda小组在Internet上提供的进行二维相关性计算的MatlbaM语言源程序,或是其它的进行二维相关性分析的MATLAB程序也行。在一篇论文上看到过说是Noda小组在网上提供了二维相关性计算的matlab源代码,但找不着,哪位大侠可以指点一下?pocha软件画图能力太差了。
二维液相和质谱分析都是分析复杂体系的有力工具,我以前应用二维液相和质谱联用做过一些植物萜类化合物的分析,现在正在做多酚类化合物和糖苷类化合物的研究。在工作中,发现在阀切换时,总有系统峰出现,虽然不影响分析,但有点难看,如果大家有消除系统峰的好办法请告诉我。大家应用二维液相和质谱联用做的东东交流一下,看看有那些问题。下面是一份二维液相质谱分析在蛋白质组学分析中应用的专题报告,244页,内容丰富,与大家分享一下。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=129341]二维液相质谱分析在蛋白质组学分析中应用[/url]
请教各位老师,我用的是PE公司的仪器及软件,请问怎样做红外二维相关谱与二阶导数谱?
请问二维核磁分析什么样结构的样品是最好的?也就是说什么样的样品有必要做个二维核磁?谢谢了
[font=Encryption][color=#898989]摘要:[/color][/font][font=Encryption][color=#666666] 原油中烃类[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析的传统方法是先对原油进行族分离得到饱和烃和芳烃,然后分别进行[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析,因此不能反映原油的原始特性和烃类组分的全貌.全二维[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析方法能直接对原油样品进行分析,同时获得饱和烃和芳烃的地球化学参数,避免原油样品经族分离带来的分析误差,缩短分析时间.通过一维、二维色谱柱及升温速率、柱流量、初始柱温等条件实验,优选出原油中烃类全二维[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析的最佳实验条件 应用原油的全二维[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]/飞行时间质谱分析结果,建立了饱和烃、芳烃、萘系列、菲系列及二苯并噻吩化合物的相对位置定性图版,再利用图版对原油中组分进行定性分析 采用面积归一化法进行定量分析,并计算出了石油天然气行业标准所规定的饱和烃与芳烃地球化学参数 精确度实验结果表明,质量分数大于1%的样品多次重复分析的相对偏差小于5%,符合原油实验测定要求.[/color][/font]
为什么在全二维色谱分析下计算C5到C7轻烃间各化合物相对浓度,环烷烃,异构烷烃浓度均高于一维色谱分析下计算的浓度,但正构烷烃浓度低于一维色谱?
书名:中药二维相关红外光谱鉴定图集作者:孙素琴 周群 秦竹出版社:化学工业出版社出版年:2003页数:451页装帧:精装ISBN: 7-5025-4423-2
上海哪里可以做红外光谱-质谱-同步热分析联用,测试一个样大概多少钱?
通过二维相关红外光谱,研究了再生蚕丝蛋白膜的构象及其转变与温度之间的关系。
实验室要过17025了,现使用标准见附件。求助关于同步热分析仪 傅里叶红外光谱仪 测试所涉及的测试标准由哪些,谢谢大家可以分享啊。最好是国标~~
有没有比较详细的二维色谱资料啊
二维材料是当前材料学的研究热点,尺寸为数十微米的二维材料通常用XPS表面分析设备自带的光学显微镜无法直接观察到。本作品介绍了一种图案点阵法,利用XPS自带的最大12倍的光学显微镜,能很好的定位数十微米的二维材
各位同仁,那位比较了解同步辐射光源这方面的知识,给大家讲解一下。我只是知道采用这种光源的红外显微镜的空间分辨率比现在的硅碳棒光源要高很多,可以分析细胞。
公司新收购了一台STA同步热分析仪,可以串联红外和质谱,我们是食品药品环境器械工业品检测的第三方检测,请问大家在哪些项目可以应用?

【网络会议】:全二维色谱在复杂样品分析中的应用【讲座时间】:2015年08月18日 10:00【主讲人】:张艳海赛默飞世尔公司色谱质谱部应用研究中心液相色谱应用工程师,在赛默飞一直致力于液相色谱方面的应用方法开发,主要应用方向为多维色谱分离、online-SPE技术在药物、食品和环境中的应用,积累有丰富的分析经验。【会议介绍】 随着科学研究的不断深入,复杂样品的分析已成为热点。一维色谱很难满足要求。多维色谱分离技术可提供更大的峰容量,有效减少色谱峰重叠,从而提供更多更准确的信息,已获得越来越多研究人员的关注和应用。 赛默飞特色的双三元液相色谱在多维色谱分离方面具有较高的自动化和灵活性,易于使用,可轻松实现二维或多维色谱分离应用。本次讲座将给大家介绍赛默飞双三元液相色谱在中药和蛋白分析中全二维液相色谱分离技术的应用。 -------------------------------------------------------------------------------1、报名条件:只要您是仪器网注册用户均可报名,通过审核后即可参会。2、报名并参会用户有机会获得100元手机充值卡一张哦~3、报名截止时间:2015年08月18日 9:304、报名参会:http://www.instrument.com.cn/webinar/meeting/meetingInsidePage/16085、报名及参会咨询:QQ群—379196738http://ng1.17img.cn/bbsfiles/images/2017/10/2015042911235201_01_2507958_3.jpg
我单位(高校测试中心)的DSC-TG同步热分析、红外、荧光光谱目前都对外开放,均为进口仪器。有需要者欢迎联系测试,量大价格优惠!可选择是否开发票。地点在福州,QQ 2285532917

二维付立叶变换光学系统的空间带宽积与颗粒大小分析任中京(山东建材学院 250022)提要用付立叶光学原理,从理论与实践讨论了二维付立叶变换光学系统的空间带宽积的物理意义。首次提出了具有重要实用价值的敏感空间带宽积概念并介绍了它的主要应用。关健词光学付立叶变换,空间带宽积,粒度分析二维付立叶变换光学系统最成功的应用领域之一就是颗粒粒度分析。依据付立叶光学原理,通过检测群的付立叶谱,无需颗粒按大小在空间分离,便可实现粒度实时与动态测试与分析,从而开辟了粒度在线分析的广阔前景现在已被广泛应用于建材、冶金、能源、化工等许多领域。此类粒度分析仪与经典的成象光学仪器不同,不能用放大率、景深、清晰度等参数来描述,概括仪器本质特征的参数是空间带宽积,空间带宽积制约着激光粒度仪的测量范围、分辩率、粒度的分级。正确理解空间带宽积,是改进与提高激光粒度分析仪的基础。本文着重探讨空间带宽积的物理意义,及其与颗粒大小分析之间的密切关系。空间带宽积在二维付立叶变换光路中,直径为d的圆孔屏置于前焦面,在平行激光照射下,在后焦面可得到此孔的衍射图样,中心O级衍射谱称为爱里斑,爱里斑半径由下式表示:http://ng1.17img.cn/bbsfiles/images/2013/05/201305281052_441887_388_3.jpg从(2)式可见,衍射物的空间尺度d与衍射空间频谱宽度ρ/λf的乘积为一常数,我们称d*ρ/λf为空间带宽积。为了不失一般性,我们讨论二维付立叶变换系统对任一空域函数的抽样,在空域频域均采用直角座标系。由抽样定理可知,在空域对于带限函数g(x,y)使用间隔为△x△y的寻距抽样,得样本函数:http://ng1.17img.cn/bbsfiles/images/2013/05/201305281052_441888_388_3.jpghttp://ng1.17img.cn/bbsfiles/images/2013/05/201305281052_441889_388_3.jpghttp://ng1.17img.cn/bbsfiles/images/2013/05/201305281052_441890_388_3.jpg我们称满足(5)式的抽样间隔为尼奎斯特间隔。(5)式表明尼奎斯特间隔与原函数的带宽之积等于1。此乘积即为直角座标系中的空间带宽积。以上分析表明:小的空间尺寸必然对应着一个宽的频带,换句话说,要测量小颗粒必须要用较宽的频带。如果尼奎斯特间隔大子所测的颗粒,则此颗粒在抽样中将被漏掉,频率将失真。尼奎斯特间隔对激光粒度仪来讲就是该仪器最小可分辩尺寸。激光粒度仪的空间带宽积在激光粒度仪中,由于颗粒群的空间频谱具有中心对称性,因此通常采用同心环状的阵列探测器对功率谱进行抽样。现考察一个半径为r0的颗粒,其透过率函数为http://ng1.17img.cn/bbsfiles/images/2013/05/201305281052_441891_388_3.jpg(11)式给出了颗粒与其付立叶径向功率谱的敏感空间带宽积。其物理意义是颗粒直径d发生变化时,满足上式的ρm处的功率谱变化最大。敏感空间带宽积在激光粒度分析仪的设计中具有重要作用。敏感空间带宽积的应用敏感空间带宽积在激光粒度分析仪的设计中可用来确定测量的上下限粒径,与颗粒的分级。http://ng1.17img.cn/bbsfiles/images/2013/05/201305281052_441892_388_3.jpg从(11)式还可看出,使用长波长的激光光源或者增大付立叶透镜的焦距有利于扩大测量范围;反之,则有利于提高仪器的分辩率。[s

刚刚在上海同步辐射实现了二维掠入射X射线衍射测量,与大家分享一下结果。清晰的图片上传到谱图库中了。[img]http://ng1.17img.cn/bbsfiles/images/2010/06/201006181014_225484_1988793_3.jpg[/img]
最近,研究二维液相色谱系统,发现岛津和湖南德米特的二维液相色谱系统,几乎独家垄断,价格比两套lc20还高。
【作者】:刘朝霞1周亚楠1何兰1丁丽霞2【题名】:二维[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]技术在药物分析中的应用【期刊】:中国药学杂志.【年、卷、期、起止页码】:2019,54(12)【全文链接】:https://kns.cnki.net/kcms2/article/abstract?v=3uoqIhG8C44YLTlOAiTRKibYlV5Vjs7iLik5jEcCI09uHa3oBxtWoIlSwQgyG1CGZCsLXh3sTIdR9m0mpRcAFsefpdV-z7rJ&uniplatform=NZKPT
二维液相色谱(2D—LC)是将分离机理不同而又相互独立的两支色谱柱串联起来构成的分离系统。样品经过第一维的色谱柱进入接口中,通过浓缩、捕集或切割后被切换进入第二维色谱柱及检测器中。二维液相色谱通常采用两种不同的分离机理分析样品,即利用样品的不同特性把复杂混合物(如肽)分成单一组分,这些特性包括分子尺寸、等电点、亲水性、电荷、特殊分子间作用(亲和)等,在一维分离系统中不能完全分离的组分,可能在二维系统中得到更好的分离,分离能力、分辨率得到极大的提高。完全正交的二维液相色谱,峰容量是两种一维分离模式单独运行时峰容量的乘积。假如两种分离系统都有100的峰容量,那么良好的二维系统理论上可产生10000的峰容量。二维液相色谱大多使用两支或多支色谱柱,并通过柱结合技术实现样品的柱间切换。柱切换通常可分为部分和整体切换两种模式。按切割组分是否直接进人二维中,二维分离又可分为离线和在线两种方式。早期的中心切割技术,大都先在容器中收集一维洗脱产物,再进样到第二维中。随着现代仪器的发展和适应自动化分离的需要,目前二维色谱大多采用在线方式,使一维洗脱产物(部分或全部)直接进入到第二维柱系统中进行分离分析。部分模式即采用中心切割技术,只使第一维分离的部分感兴趣的组分进入第二维中进一步分析。为了将样品有效地转移到下一维柱系统中,必须先在第一维分离模式中用标准物进行实验,根据得到的分离信息设计切换程序。部分模式不能得到样品所有组分的信息,此外,还有操作繁琐、样品易损失与污染及可能降低分辨率等缺点。整体模式即全多维液相色谱模式(comprehensive HPLC)。基于Giddings 的理论,一般认为全多维分离应满足3个条件:(1)样品的每一部分都受到不同模式的分离;(2)所有样品组分以相等的比例(100%或稍低一些,即并不要求100%分析物,只要分流的部分能代表所有样品组分信息即可)转移到二维及检测器中;(3)在一维中已得到的分辨率基本上维持不变。“基本”指通过测量全二维中第一维轴上的某个特殊峰所对应的第一维的分辩率与一维情况相比减少不超过10%。其中,第一条和第三条说明了传统的中心切割技术与全二维的区别。Schoenmakem等 认为在二维分离之前进行分流也可称为全二维分离,进一步拓宽了全二维分离的概念。

求购二手美国TA SDT Q600同步热分析仪,见图片,微信:xu573537859,或站短。[img=,500,335]https://ng1.17img.cn/bbsfiles/images/2019/11/201911190956091468_6465_3905896_3.jpg!w500x335.jpg[/img]
中国科技网讯 以往的研究表明,二维碳薄片石墨烯拥有一个通用的光吸收系数。而据物理学家组织网近日报道,现在,美国能源部劳伦斯伯克利国家实验室的科学家首次证实,所有的二维半导体也同样普遍适用于一个类似的简单吸光规律。他们利用超薄半导体砷化铟薄膜进行的实验发现,所有的二维半导体,包括受太阳能薄膜和光电器件行业青睐的Ⅲ-Ⅴ族化合物半导体,都有一个通用的吸收光子的量子单位,他们称之为“AQ”。相关研究论文发表在美国《国家科学院学报》上。 从太阳能电池到光电传感器再到激光器和各类成像设备,许多当今的半导体技术都是基于光的吸收发展起来的。吸光性对于量子阱中的纳米尺度结构来说尤为关键。量子阱是由带隙宽度不同的两种薄层材料交替生长在一起形成的具有量子限制效应的微结构,其中的电荷载流子的运动被限制在一个二维平面上,能带结构呈阶梯状分布。 “我们使用无需支撑的厚度可减至3纳米的砷化铟薄膜作为模型材料系统,来准确地探测二维半导体薄膜的厚度和电子能带结构对光吸收性能的影响。”论文的通信作者、劳伦斯伯克利国家实验室材料科学部的科学家兼加州大学伯克利分校电气工程和计算机科学教授阿里·贾维说,“我们发现,这些材料的阶梯式光吸收比与材料的厚度和能带结构无关。” 他们将超薄的砷化铟膜印在由氟化钙制作的光学透明衬底上,砷化铟膜吸收光,氟化钙衬底不吸光。贾维说:“这样我们就能够根据材料的能带结构和厚度来研究厚度范围在3纳米到19纳米之间的薄膜的吸光性能。” 借助伯克利实验室先进光源的傅立叶变换红外分光镜,贾维团队在室温下测出了从一个能带跃迁到下一个能带时的光吸收率。他们观察到,随着砷化铟薄膜能带的阶梯式跃迁,AQ值也以大约1.7%的系数相应地逐级递增或者递减。 “这种吸光规律对于所有的二维半导体来说似乎是普遍适用的。”论文另一个通信作者、电气工程师伊莱·雅布洛诺维奇说,“我们的研究结果加深了对于强量子限制效应下的电子—光子相互作用的基本认识,也为了解如何使二维半导体拓展出新奇的光子和光电应用提供了独特视角。”(陈丹) 《科技日报》(2013-8-5 二版)
【序号】:3【作者】: 施靖 陈艳【题名】:经阴道二维联合三维超声成像诊断宫腔黏连的临床价值分析【期刊】:现代实用医学. 【年、卷、期、起止页码】:2021,33(10)【全文链接】:https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CJFD&dbname=CJFDLAST2021&filename=NBYX202110063&uniplatform=NZKPT&v=QRTf4TGZNo-QHML4b5Vc72POsEBVSKOSPqaaMfOOZcc8jFZIOSIaSdEKBuTkwthU