推荐厂家
暂无
暂无
 留言咨询
留言咨询
 留言咨询
留言咨询
 留言咨询
留言咨询

 留言咨询
留言咨询

 留言咨询
留言咨询

 400-860-5168转3452
400-860-5168转3452
 留言咨询
留言咨询




[size=16px]动物疫病诊断仪主要检测什么动物疫病诊断仪主要检测以下几种:猪弓形体IgG抗体检测:用于检测弓形虫抗体。猪蓝耳病ELISA诊断试剂盒:用于检测猪蓝耳病病毒抗体。猪伪狂犬病ELISA抗体检测诊断试剂盒:用于伪狂犬病毒抗体检测。猪瘟ELISA诊断试剂盒:用于检测猪瘟抗体。猪细小病毒ELISA诊断试剂盒:用于检测细小病毒抗体。此外,动物疫病诊断仪还可以检测黄曲霉毒素B1、猪伪狂犬病毒、猪口蹄疫3ABC蛋白、猪口蹄疫病毒IgG、猪布鲁氏杆菌病、猪传染性胃肠炎等。[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2023/11/202311290939024874_272_6098850_3.jpg!w690x690.jpg[/img][/size]
GB/T 18089-2008 蓝舌病病毒分离、鉴定及血清中和抗体检测技术
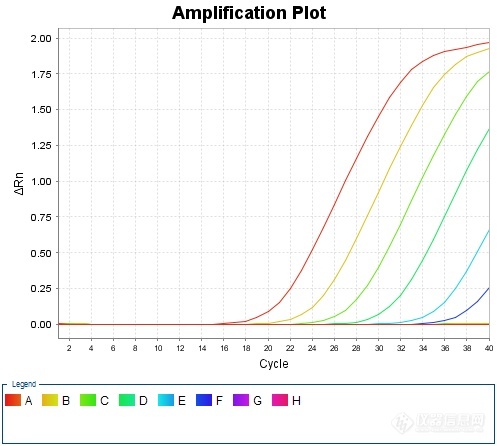
[color=black]猪伪狂犬病毒荧光定量[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测方法的模块化构建及实践[/color][color=black]1 前言[/color][color=black]猪伪狂犬病是由猪伪狂犬病病毒(Pseudo rabies virus,PRV)引起的猪的急性传染病。该病在猪呈暴发性流行。可引起妊娠母猪流产、死胎,公猪不育,新生仔猪大量死亡,育肥猪呼吸困难、生长停滞等,是危害全球养猪业的重大传染病之一。[/color][color=black]伪狂犬病毒属于疱疹病毒科(Herpesviridae)、猪疱疹病毒属,病毒粒子为圆形,直径150~180nm,核衣壳直径为105~110nm。病毒粒子的最外层是病毒囊膜,它是由宿主细胞衍生而来的脂质双层结构。囊膜表面有长约8~10nm呈放射状排列的纤突。[/color][color=black]伪狂犬病毒是疱疹病毒科中抵抗力较强的一种。在37℃下可存活7h,8℃可存活46天,而在25℃干草、树枝、食物上可存活10~30天,但短期保存病毒时,4℃较-20℃冻结保存更好。病毒在pH4~pH9之间保持稳定。5%石炭酸经2min灭活,但0.5%石炭酸处理32天后仍具有感染性。0.5%~1%氢氧化钠迅速使其灭活。对乙醚、氯仿等脂溶剂以及福尔马林和紫外线照射敏感。[/color][color=black]伪狂犬病毒在全世界广泛分布。伪狂犬病自然发生于猪、牛、绵羊、犬和猫,另外,多种野生动物、肉食动物也易感。水貂、雪貂因饲喂含伪狂犬病毒的猪下脚料也可引起[/color][url=https://baike.baidu.com/item/%E4%BC%AA%E7%8B%82%E7%8A%AC%E7%97%85%22 \t %22_blank][color=black]伪狂犬病[/color][/url][color=black]的暴发。[/color][color=black]猪是伪狂犬病毒的贮存宿主,病猪、带毒猪以及带毒鼠类为本病重要传染源。不少学者认为,其他动物感染本病与接触猪、鼠有关。[/color][color=black]在猪场,伪狂犬病毒主要通过已感染猪排毒而传给健康猪,另外,被伪狂犬病毒污染的工作人员和器具在传播中起着重要的作用。而空气传播则是伪狂犬病毒扩散的最主要途径,但到底能传播多远还不清楚。人们还发现在邻近有伪狂犬病发生的猪场周围放牧的[/color][url=https://baike.baidu.com/item/%E7%89%9B%E7%BE%A4%22 \t %22_blank][color=black]牛群[/color][/url][color=black]也能发病,在这种情况下,空气传播是惟一可能的途径。在猪群中,病毒主要通过鼻分泌物传播,另外,乳汁和精液也是可能的传播方式。[/color][color=black]除猪以外的其他动物感染伪狂犬病毒后,其结果都是死亡。猪发生伪狂犬病后,其临诊症状因日龄而异,成年猪一般呈隐性感染,怀孕母猪可导致流产、死胎、木乃伊胎和种猪不育等综合症候群。15日龄以内的仔猪发病死亡率可达100%,断奶仔猪发病率可达40%,死亡率20%左右;对成年肥猪可引起生长停滞、增重缓慢等。[/color][color=black]伪狂犬病的发生具有一定的季节性,多发生在寒冷的季节,但其他季节也有发生。[/color][color=black]新生仔猪感染伪狂犬病毒会引起大量死亡,临诊上新生仔猪第1天表现正常,从第2天开始发病,3~5天内是死亡高峰期,有的整窝死光。同时,发病仔猪表现出明显的神经症状、昏睡、呜叫、呕吐、拉稀,一旦发病,1~2日内死亡。剖检主要是肾脏布满针尖样出血点,有时见到肺水肿、脑膜表面充血、出血。15日龄以内的仔猪感染本病者,病情极严重,发病死亡率可达100%。仔猪突然发病,体温上升达41℃以上,精神极度委顿,发抖,运动不协调,痉挛,呕吐,腹泻,极少康复。断奶仔猪感染伪狂犬病毒,发病率在20%~40%左右,死亡率在10%~20%左右,主要表现为神经症状、拉稀、呕吐等。成年猪一般为隐性感染,若有症状也很轻微,易于恢复。主要表现为发热、精神沉郁,有些病猪呕吐、咳嗽,一般于4~8天内完全恢复。怀孕母猪可发生流产、产木乃伊胎儿或死胎,其中以死胎为主无论是头胎母猪还是经产母猪都发病,而且没有严格的季节性,但以寒冷季节即冬末春初多发。[/color][color=black]伪狂犬病的另一发病特点是表现为种猪不育症。近几年发现有的猪场春季暴发伪狂犬病,出现死胎或断奶仔猪患伪狂犬病后,紧接着下半年母猪配不上种,返情率高达90%,有反复配种数次都屡配不上的。此外,公猪感染伪狂犬病毒后,表现出睾丸肿胀、萎缩,丧失种用能力。[/color][color=black]由于猪伪狂犬病毒可以通过精液传播,一旦公猪感染伪狂犬,则在短时间内可快速导致整个猪场母猪群感染该病。而猪伪狂犬病又可通过乳汁传播,故感染伪狂犬病的母猪又可快速导致整个猪场的仔猪感染该病。因此,非常有必要对种猪(公猪、母猪)进行猪伪狂犬病进行病毒核酸监测,并实施猪伪狂犬病实施净化措施。[/color][color=black]2 模块化检测方法思路[/color][color=black]总体思路是:将动物疫病荧光定量[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测分为三个模块,核酸提取采用DNA/RNA共提试剂,核酸扩增采用预混液+引物探针方式,质控品利用抗原或商品化疫苗自制。具体思路如下:[/color][color=black]——核酸提取采用DNA/RNA共提试剂;[/color][color=black]——引物探针严格按照标准方法,委托生物工程公司合成;[/color][color=black]——反应体系中其他成分,采购商品化q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]预混液;[/color][color=black]——质控品:阳性对照采用商品化疫苗,测定结果后按一定比例稀释,保存备用。[/color][color=black]——反应体系:设为20μL,其中包含:预混液(2×)10μL、ROX 0.4μL为固定量,引物探针加入量根据检测标准中的终浓度予以换算,加灭菌水补足18μL,RNA模板为2μL;[/color][color=black]——反应条件首先按照标准中的条件开展摸索,如达到预期效果则予以固定;如效果不佳则参照预混液及引物探针推荐条件进行适当调整。[/color][color=black]3 材料和方法[/color][color=black]3.1 病毒[/color][color=black]猪伪狂犬病毒疫苗。[/color][color=black]3.2 试剂[/color][color=black]DNA/RNA共提试剂盒:FastPure Viral DNA/RNA Mini Kit试剂盒,南京诺维赞生产;[/color][color=black]q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]预混液:AceQ Universal U+ Probe Master Mix V2,南京诺维赞生产。[/color][color=black]3.3 引物探针[/color][color=black]按照GB/T 35911-2018 《伪狂犬病病毒荧光[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测方法》提供的序列,委托上海生工合成,引物稀释成10μmol/L、探针稀释成5μmol/L,分装成小包装冷冻保存备用。具体序列如下:[/color][color=black]检测gH基因引物探针序列:[/color][color=black]正向引物:5’-ACGCTCGGCTTCCTCTCC-3’[/color][color=black]反向引物:5’-GGTAGTCGTCGCTCTCGTG-3’[/color][color=black]探 针:5’-FAM-TCGCGCATCGTCTGGTGCAT-BHQ1 -3’[/color][color=black]检测gE基因引物探针序列:[/color][color=black]正向引物:5’-GCTGTACGTGCTCGTGAT-3’[/color][color=black]反向引物:5’-TCAGCTCCTTGATGACCGTGA-3’[/color][color=black]探 针:5’-VIC-CACAACGGCCACGTCGCCACCTG-BHQ1 -3’[/color][color=black]3.4 反应体系[/color][color=black]根据GB/T 35911-2018 《伪狂犬病病毒荧光[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测方法》所载反应体系,按照终浓度一致原则予以转化。具体转换方法:[/color][color=black]——反应体系总体积设定为20μL;[/color][color=black]——将标准中反应体系的10×[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url] Buffer、MgCl2、dNTPs、Taq酶等成分转换为q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]预混液10μL(推荐量);[/color][color=black]——因使用ABI7500荧光[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]仪,故在体系中加入ROX 0.4μL;[/color][color=black]——标准中gH基因正向引物、反向引物、探针的终浓度分别为0.2μmol/L、0.2μmol/L和0.2μmol/L,gE基因正向引物、反向引物、探针的终浓度分别为0.2μmol/L、0.2μmol/L和0.12μmol/L,故在修改后的体系中加入量为0.4μL、0.4μL、0.8μL和0.4μL、0.4μL、0.48μL;[/color][color=black]——总DNA加入量修改为2μL(根据经验该加入量已经足够);[/color][color=black]——根据上述各成分用量,补充体积的无核酸酶水修改为4.72μL。[/color][table][tr][td][color=black]标准方法[/color][/td][td][/td][td][/td][td][color=black]修改方法[/color][/td][td][/td][/tr][tr][td][color=black]10Χ [url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url] Buffer[/color][/td][td][align=center][color=black]5.0[/color][/align][/td][td][/td][td][color=black]2Χ q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]预混液[/color][/td][td][align=center][color=black]10[/color][/align][/td][/tr][tr][td][color=black]Taq酶(5U/μL)[/color][/td][td][align=center][color=black]2.0[/color][/align][/td][td][/td][td][color=black]ROX[/color][/td][td][align=center][color=black]0.4[/color][/align][/td][/tr][tr][td][color=black]dNTPs(100mmol/L)[/color][/td][td][align=center][color=black]1.5[/color][/align][/td][td][/td][td][color=black]gH基因正向引物(10μmol/L)[/color][/td][td][align=center][color=black]0.4[/color][/align][/td][/tr][tr][td][color=black]MgCl2[/color][/td][td][align=center][color=black]0.25[/color][/align][/td][td][/td][td][color=black]gH基因反向引物(10μmol/L)[/color][/td][td][align=center][color=black]0.4[/color][/align][/td][/tr][tr][td][color=black]gH基因正向引物(10μmol/L)[/color][/td][td][align=center][color=black]1.0[/color][/align][/td][td][/td][td][color=black]gH基因探针(5μmol/L)[/color][/td][td][align=center][color=black]0.8[/color][/align][/td][/tr][tr][td][color=black]gH基因反向引物(10μmol/L)[/color][/td][td][align=center][color=black]1.0[/color][/align][/td][td][/td][td][color=black]gE基因正向引物(10μmol/L)[/color][/td][td][align=center][color=black]0.4[/color][/align][/td][/tr][tr][td][color=black]gH基因探针(10μmol/L)[/color][/td][td][align=center][color=black]1.0[/color][/align][/td][td][/td][td][color=black]gE基因反向引物(10μmol/L)[/color][/td][td][align=center][color=black]0.4[/color][/align][/td][/tr][tr][td][color=black]gE基因正向引物(10μmol/L)[/color][/td][td][align=center][color=black]1.0[/color][/align][/td][td][/td][td][color=black]gE基因探针(5μmol/L)[/color][/td][td][align=center][color=black]0.48[/color][/align][/td][/tr][tr][td][color=black]gE基因反向引物(10μmol/L)[/color][/td][td][align=center][color=black]1.0[/color][/align][/td][td][/td][td][color=black]无核酸酶水[/color][/td][td][align=center][color=black]4.72[/color][/align][/td][/tr][tr][td][color=black]gE基因探针(10μmol/L)[/color][/td][td][align=center][color=black]0.6[/color][/align][/td][td][/td][td][color=black]总DNA[/color][/td][td][align=center][color=black]2.0[/color][/align][/td][/tr][tr][td][color=black]无核酸酶水[/color][/td][td][align=center][color=black]23.95[/color][/align][/td][td][/td][td][color=black]总体积[/color][/td][td][align=center][color=black]20[/color][/align][/td][/tr][tr][td][color=black]内参质粒[/color][/td][td][align=center][color=black]0.2[/color][/align][/td][td][/td][td][/td][td][/td][/tr][tr][td][color=black]总DNA[/color][/td][td][align=center][color=black]10[/color][/align][/td][td][/td][td][/td][td][/td][/tr][tr][td][color=black]总体积[/color][/td][td][align=center][color=black]50[/color][/align][/td][td][/td][td][/td][td][/td][/tr][/table][color=black]3.5 反应条件[/color][color=black]参照GB/T 35911-2018 《伪狂犬病病毒荧光[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测方法》推荐的扩增程序,结合ABI7500荧光采集时间不能少于34s的要求,进行预试验。扩增程序如下:[/color][color=black]50℃2min →95℃2min →(95℃15s → 60℃34s)*40[/color][color=black]如扩增结果理想,则不做修改直接采纳,否则进行适当调整。[/color][color=black]4 试验结果[/color][color=black]对猪伪狂犬病毒疫苗(BK61株)进行核酸检测,结果较理想。扩增曲线如下:[/color][align=center][img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009251442207825_7042_1627156_3.jpg[/img][/align][color=black]注:因猪伪狂犬疫苗BK61株属于gE基因缺失苗,故gE基因未能检出。[/color][color=black]5 阳性质控的制备[/color][color=black]根据GB/T 35911-2018 《伪狂犬病病毒荧光[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测方法》规定,阳性对照应Ct≤30。对猪伪狂犬病毒疫苗(BK61株)适当稀释后进行再次检测,结果如下:[/color][table][tr][td][align=center][color=black]稀释倍数[/color][/align][/td][td][align=center][color=black]1:10^0[/color][/align][/td][td][align=center][color=black]1:10^1[/color][/align][/td][td][align=center][color=black]1:10^2[/color][/align][/td][td][align=center][color=black]1:10^3[/color][/align][/td][/tr][tr][td][align=center][color=black]PRV疫苗(BK61株)[/color][/align][/td][td][align=center][color=black]19.12[/color][/align][/td][td][align=center][color=black]22.58[/color][/align][/td][td][align=center][color=black]25.90[/color][/align][/td][td][align=center][color=black]29.58[/color][/align][/td][/tr][/table][color=black]经综合判定,最后采用猪伪狂犬病毒疫苗(BK61株)作1: 10^2稀释,分装为200μL/管作为阳性质控,Ct值约26,-70℃冻存备用。[/color][color=black]6 讨论[/color][color=black]6.1 检测工作更加方便高效[/color][color=black]一是在核酸提取环节采用了DNA/RNA共提试剂,待检样品经一次提取核酸,除可应用于伪狂犬病毒、圆环病毒、非洲猪瘟等DNA病毒项目检测外,还可应用于口蹄疫、蓝耳病等RNA病毒项目检测;[/color][color=black]二是由于实验室储备了足够量的q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]预混液,在开展检测时,不必担心部分检测量较少的项目由于试剂组分不足而罢工事件的发生;[/color][color=black]三是由于q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]预混液适用于多数DNA病毒项目的检测,在检测任务发生重大变化时,可以方便地调整检测项目,不必担心试剂不足或浪费情况的发生。[/color][color=black]6.2 阳性质控品制备方便[/color][color=black]猪伪狂犬病毒疫苗是较常用的动物免疫用疫苗,只需对疫苗进行含量测定,进行一定比例的稀释即可作为实验室内部的阳性质控品。[/color][color=black]6.3 适用性有待进一步验证[/color][color=black]尽管在构建新方法时,对适用性进行了验证,但由于缺少伪狂犬全基因疫苗,因此对于gE基因的适用性未对进行验证。对于其他毒株,尤其是较新型的变异株是否有效,尚有待进一步观察和验证。[/color][color=black]6.4 严格依法依规操作[/color][color=black]如果有关法律法规或上级有关部门出台政策,要求采用获批准的成品试剂盒用于检测,则实验室必须及时停止自建方法的使用。[/color]