内毒素系存在于革兰阴性菌细胞壁外膜中的一种相对不溶性物质,它的主要成分是脂多糖( LPS ),能够引起发热、休克、器官损害、甚至死亡等病理反应。但是,几十年来人们对于内毒素的定量检测一直束手无策。如今,天津大学、中国生物制品检定所经过十多年的研究,终于寻找到了一种可靠有效的临床内毒素定量检测方法,研制出了第一台细菌内毒素定量分析仪(BET-24A)。该仪器采用先进的光密度反应时间法测定原理,配有目前最先进的专利技术鲎试剂安瓿直接检测,操作简便,检测时间短,能准确检测出人体内毒素的含量,从而为临床内毒素血症的早期诊断,及指导临床及时合理用药具有重要价值。 意义: 快速鉴别诊断细菌性和非细菌性感染和炎症。 早期判断革兰氏阴性细菌感染情况。 相关疾病的早期诊断与病情监控。 帮助临床医生筛选适当的药物。 评价临床治疗及预后情况,提高临床治愈率,降低死亡率。
谁做过内毒素定量检测啊,最好是终点显色法
细菌内毒素检测新手指南 鲎试剂 鲎试剂是从栖生于海洋的节肢动物“鲎”的蓝色血液中提取变形细胞溶解物,经低温冷冻干燥而成的生物试剂,专用于细菌内毒素与β-葡聚糖检测。 鲎试剂按原料来源分:全世界目前有4个种属的鲎,其中仅有东方鲎(Tachypleus tridentatus Leach) 和美洲鲎(Limulus polyphemus Linnaeus)可制造鲎试剂,对应生产出来的鲎试剂分别为东方鲎鲎试剂(Tachypleus Amebocyte Lysate, TAL)和美洲鲎鲎试剂(Limulus Amebocyte Lysate,LAL),TAL与LAL具有相同的功效。 鲎试剂按方法分: 凝胶法鲎试剂动态浊度法鲎试剂终点浊度法鲎试剂动态显色法鲎试剂终点显色法鲎试剂 凝胶法系通过鲎试剂与内毒素产生凝集反应的原理来定性检测或半定量内毒素的方法。凝胶法鲎试剂常见规格为0.1ml/支或0.5ml/支或者更大装量,使用时应加除热原水(细菌内毒素检查用水)复溶后使用。凝胶法是通过观察有无凝胶形成作为反应的终点。此法操作比较简单,经济,不需要专用测定设备,可以进行定性或半定量测定。 特异性鲎试剂,即弃G因子鲎试剂,是国内首创的产品, 它专一对内毒素起反应,避免了G因子旁路的干扰,使检测结果更加可靠,在药检和临床检验方面是不可或缺的理想检测试剂。 动态浊度法鲎试剂、终点浊度法鲎试剂、动态显色法鲎试剂、终点显色法鲎试剂,这四种方法都是定量检测内毒素的。 根据检测原理,终点浊度法和动态浊度法都属于浊度法。浊度法系利用检测鲎试剂与内毒素反应过程中的浊度变化而测定内毒素含量的方法。终点浊度法未见商品化产品。动态浊度法(又称动态比浊法)是检测反应混合物的浊度上升某一预先设定的吸光度所需要的反应时间,或是检测浊度增加速度的方法。 终点显色法和动态显色法都是属于显色基质法。显色基质法系利用鲎试剂与内毒素反应过程中产生的凝固酶使特定底物显色释放出的呈色团的多少而测定内毒素含量的方法,根据产物颜色判断内毒素浓度,又称为比色法。厦门鲎试剂厂于2005年推出以鲎四肽为显色底物的鲎试剂盒,抗干扰能力强, 灵敏度高达0.005EU/ml, 质量达到国际领先水平。目前已有500多家单位使用该试剂盒,并有部分单位发表相应文献。国内有少量国外产品,但价格远高于国产试剂,到货周期长。 如果您仅需要检测样品的内毒素限量,可以选择凝胶法鲎试剂,通过确定内毒素限值及最大有效稀释倍数,做样品的干扰试验从而确定使用的鲎试剂的灵敏度。如果您需要定量测定样品中内毒素含量则应选择显色基质鲎试剂盒或动态浊度法鲎试剂。 动态浊度法与动态显色法需要带温育系统的动态光度测定仪器及配套软件,例如,微板鲎试仪ELx808及软件TALgent 或Gen5。动态浊度法与动态显色法简单方便、一步即成,线性范围宽。 终点显色法需要配套酶标仪或可见分光光度计进行检测。配套带有温育系统的酶标仪,如微板鲎试仪ELx808,可减少试剂用量。 相关链接:厦门市鲎试剂实验厂有限公司于1983年成立,于2000年加资改组,是国内最大最早生产鲎试剂的厂家,本厂于1987年研制成功鼓浪屿牌鲎试剂(荣获1978-1979年度福建省重大科技成果二等奖,1983年卫生部甲级成果奖,1988年获卫生部科学技术进步三等奖),1988年获卫生部新试剂生产批件((88)卫药SJ-02号),1995年全国首家推出特异性鲎试剂,2005年又推出显色基质鲎试剂,2007年推出高效、自动、微量的鲎试仪ELX808(内毒素测定仪)及配套软件,2009年重磅推出透析专用鲎试剂盒。目前已有透析专用鲎试剂盒、显色基质鲎试剂、凝胶法鲎试剂、动态浊度法鲎试剂、特异性鲎试剂、内毒素、辅剂及鲎试仪ELX808、除热源耗材等一系列产品。
鲎试剂分类及选购-内毒素检测新手必看显色基质鲎试剂、凝胶法鲎试剂、特异性鲎试剂、动态浊度法鲎试剂、比色法鲎试剂、显色法鲎试剂、动态显色法鲎试剂、浊度法鲎试剂 、动态比浊法鲎试剂、弃G因子鲎试剂、终点显色法鲎试剂...。如果你是一位刚准备做细菌内毒素检测的实验人员,看到有这么多种鲎试剂,是不是有个疑问:“这么多种鲎试剂,我该怎么选择呢?”别急,不要被这么多名字吓到了,以下为您详细分类介绍;首先,知道什么是鲎试剂。鲎试剂是从栖生于海洋的节肢动物“鲎”的兰色血液中提取变形细胞溶解物,经低温冷冻干燥而成的生物试剂,专用于细菌内毒素检测。按原料来源分:全世界有5个种属的鲎,其中仅有中国鲎(又名三刺鲎)Tachypleus tridentatus Leach和美洲鲎Limulus polyphemus Linnaeus可制造鲎试剂,对应生产出来的鲎试剂分别为中国鲎鲎试剂(Tachypleus Amebocyte Lysate),缩写为TAL;美洲鲎鲎试剂(Limulus Amebocyte Lysate),缩写为LAL。TAL与LAL有相同的功效。按方法分:中国药典2005年版中收录了2种细菌内毒素检查法,即凝胶法和光度测定法,后者包括浊度法和显色基质法。供试品检测时,可使用其中任何一种方法进行试验。当测定结果有争议时,除另有规定外,以凝胶法结果为准。05年中国药典附录细菌内毒素检查法详见http://www.houshiji.com/newslist.asp?newsid=135&sort=2凝胶法系通过鲎试剂与内毒素产生凝集反应的原理来定性检测或半定量内毒素的方法。凝胶法鲎试剂常见规格为0.1ml/支或0.5ml/支或者更大装量,使用时应加无热原水(细菌内毒素检查用水)复溶后使用。2005年版药典中凝胶法鲎试剂结果的判断:保温60分钟±2分钟后观察结果。部分商家所说的半小时出结果的快速凝胶法鲎试剂是没有依据的,没到时间就观察结果可能导致假阴性。特异性鲎试剂(又叫弃G因子鲎试剂)是凝胶法鲎试剂的一种,细菌内毒素及β-葡聚糖均能与鲎试剂发生凝聚反应。特异性鲎试剂就是屏蔽β-葡聚糖引起的鲎试剂凝聚反应,使鲎试剂仅与内毒素起反应。一般中草药注射液成份复杂,干扰因素较多,常含有β-葡聚糖或内毒素类似物。用特异性鲎试剂能减少或消除假阳性反应。(应做对比及干扰试验)。光度测定法分为浊度法和显色基质法,这2种方法都是定量检测内毒素的。浊度法系利用检测鲎试剂与内毒素反应过程过程中的浊度变化而测定内毒素含量的方法。根据检测原理,可分为终点浊度法和动态浊度法。终点浊度法未见与商品化产品,不再赘述。动态浊度(比浊)法是检测反应混合物的浊度到达某一预先设定的吸光度所需要的反应时间,或是检测浊度增加速度的方法。显色基质法系利用鲎试剂与内毒素反应过程中产生的凝固酶使特定底物显色释放出的呈色团的多少而测定内毒素含量的方法,因使用分光光度计或酶标仪器,又称为比色法。根据检测原理,分为终点显色法和动态显色法。国内已有显色基质鲎试剂盒(终点法),早期有上海伊华以鲎三肽为原料做成的鲎试剂盒,厦门鲎试剂厂于2005推出以鲎四肽为原料的鲎试剂盒,也有少量国外产品,但到货周期长,价格远高于国产试剂。动态比色法与终点比色基本原理差不多。国产暂无动态比色法,相信很快就会面市。如果您是药厂、医院、医疗器械厂商等单位的实验人员,仅需要检测样品的内毒素限量,则应选择凝胶法鲎试剂,通过确定内毒素限值及最大有效稀释倍数,做样品的干扰试验从而确定使用的鲎试剂的灵敏度。如果您需要定量测定样品中内毒素含量则应选择显色基质鲎试剂或动态浊度法鲎试剂。动态浊度法鲎试剂一般需要配备专用的动态浊度仪或带有特定软件的酶标仪,比较适合样品量较多的用户(。显色基质鲎试剂用酶标仪或分光光度计检测。是样品数较少(少于200-300个),设备比较简陋的用户。如果已有内毒素检测专用酶标仪,则可选择显色基质鲎试剂盒或动态浊度法鲎试剂。简单的说,鲎试剂就2种:定性和定量,定性就选凝胶法(特殊产品用特异性鲎试剂)。定量就是显色法鲎试剂盒或动态浊度法鲎试剂(根据已有仪器定)。如果有动态比色法鲎试剂那就多一种选择(当然要看成本)。相信通过以上介绍您对鲎试剂已经有一定了解,聪明的你一定知道如何去选择鲎试剂了吧!特别说明:由于环境污染等原因,鲎的数量在不断减少。台湾澎湖海洋生物研究中心黄丁士副研究员正在做养殖鲎的研究,他培育出12000尾刚孵化的“一龄鲎”, 60天后有250尾脱壳成“二龄鲎”,仅有少部分“二龄鲎”再经历2周成为“三龄鲎”。“二龄鲎”到“三龄鲎”的阶段存活率只有5%,人工繁殖技术上一直未能突破“三龄鲎”的瓶頸而停滯。日本也曾经划出鲎保护区,专门用来进行人工养殖鲎,但经过多年实验以失败告终。鲎的产卵量很大,但是能活到成年的比例很小。一只鲎必需脱壳15到16次,需要15年达到成年,只有成年鲎才可以采血,因此人工养殖鲎基本上不太可能。部分酒家所谓的人工养殖大多是将成年鲎圈养起来。部分保护动物是可以经营利用的,前提是,被经营利用的必须是这些野生动物经人工养殖繁殖的后代。 因此所有酒家经营的鲎都是非法的。目前日本等国由于鲎的数量减少不得不进口美洲鲎及中国鲎原料来生产鲎试剂。因此,请看到此文的朋友不要吃鲎,也请转告您身边的亲朋好友保护它。
请问我干开始做内毒素的检测,我不知道其中的内毒素限值的确定公式中的K,M,的数值是多少,药典中我说的没有合适我的产品,我的产品是三类医疗器械。还有确定最大有效稀释倍数的。我也不知道里面的浓度是怎么确定,谢谢了。
作为冻干类的注射剂产品原辅料得增加细菌内毒素项目检测,国家要求的接着问题来了,一些不能溶于水的原辅料,用什么溶液溶解?可以用氢氧化钠溶液或者其他溶液溶解,但是怎么保证溶液中无细菌内毒素,或者用计量先确定有多少细菌内毒素,然后再标定?希望大神们给个解决方法,可行的。
1、抗生素在杀菌或抑菌的同时促进了内毒素的释放,临床已见有抗生素使用后,出现脓毒性休克的先例。2、经研究发现,不同抗生素中诱发内毒素释放的作用存在差异,即头孢他啶培福新依米配能阿米卡星;在拮抗革兰阴性菌的抗生素中,碳青霉烯类优于头孢菌素类。3、避免应用亚治疗量的抗生素,不但最终未能达到杀菌目的,反而会促进耐药菌的形成,更有促进内毒素释放的负面作用。资料来源于《中华烧伤杂志》肖光夏教授快速鉴别诊断细菌性和非细菌性感染和炎症。早期判断革兰氏阴性细菌感染情况。相关疾病的早期诊断与病情监控。帮助临床医生筛选适当的药物。 评价临床治疗及预后情况,提高临床治愈率,降低死亡率。
BET-24A细菌内毒素分析仪器怎样做到定量检测的呢????
BET-24A细菌内毒素分析仪器怎样做到定量检测的呢????[em57] [em20]
[font=&][size=16px][color=#333333]点击链接查看更多:[url]https://www.woyaoce.cn/service/info-39860.html[/url]检测内容[/color][/size][/font][font=&][color=#333333][/color][/font][font=微软雅黑] [/font][font=宋体]最近“猫粮细菌内毒素”的话题热度很高,中广测带您了解细菌内毒素,并针对宠物食品中疑似隐患项目推出检测方案。[/font][font=宋体][size=16px]一、什么是细菌内毒素[/size][/font][font=宋体][size=16px]?[/size][/font][font=宋体][size=16px]细菌内毒素(Endotoxin)是革兰氏阴性菌细胞壁的主要成分,其化学成分为脂多糖(LPS)。细菌在正常状态时不释放出来,只有当细菌死亡裂解或自溶时,才表现其毒性。[/size][/font][font=宋体][size=16px]二、细菌内毒素有什么危害[/size][/font][font=宋体][size=16px]?[/size][/font][font=宋体][size=16px]相关研究表明,细菌内毒素广泛存在环境中,环境中低浓度细菌内毒素经口进入人体消化道并不产生明显危害,肝脏可以将细菌内毒素分解去除,并使细菌内毒素保持在相对较低的含量。当突然遇到或摄入大剂量细菌内毒素时,超出机体的免疫承受力时可引起发热,严重的会导致内毒素血症、休克甚至死亡。[/size][/font][font=宋体][size=16px]目前,我国已对注射剂和疫苗类产品中细菌内毒素有限量要求,但对人类食品和宠物食品中细菌内毒素含量未做规定。[/size][/font][font=宋体][size=16px] 中广测是华南地区唯一的国家级分析测试中心,是广东省饲料和饲料添加剂行政审批检测机构,2021年宠物饲料加工产品企业标准“领跑者”评估机构。拥有专业的宠物食品检测技术团队,针对当前宠物食品热点问题,参考《中国药典》“细菌内毒素检查法”,研究建立了适用于宠物食品中细菌内毒素含量的检测方法,可为从事宠物食品生产经营的广大企事业单位、爱宠人士提供全面专业的科研和检测技术服务。[/size][/font][font=&][size=16px][color=#333333]检测标准[/color][/size][/font][font=&][color=#333333][/color][/font][table][tr][td]产品名称[/td][td]检测项目[/td][td]检测标准[/td][/tr][tr][td]细菌内毒素[/td][td]细菌内毒素检查法[/td][td]中国药典[/td][/tr][/table]
BET-24A细菌内毒素分析仪器怎样做到定量检测的呢????[em20] [em20] [em20]
在浊度法检测内毒素含量时,经常有鲎试剂、稀释水等影响因素,想知道一些这方面的知识。另:浊度法检测用的测定仪是否也会影响检测结果
cavalry119在来信中提到:在内毒素的正式干扰试验中,其结果判定为 供试品溶液及检查用水应呈阴性,含内毒素的样品及用检查用水稀释的内毒素标准品应为阳性,试验为有效,其他的都能懂,但是正式干扰试验就是为了确定供试品的最大的不干扰测定浓度,供试品溶液呈阴性的话,那后面的内毒素的半定量检测中,还需要对供试品进行稀释,这样供试品不也一样应该呈现阴性嘛?
最近我用小白鼠做试验,需先给每只小白鼠注射1.5×105 EU(是10的5次方)大肠杆菌内毒素,实验完后要检测小白鼠血液中内毒素含量,血液再检测前应该怎样处理呢?用内毒素试剂盒能直接测出含量吗?试剂盒得多少钱,相配套的耗材我应该准备那些,希望那位大侠能不吝赐教,在此先谢谢了!!! 我的邮箱是norton626@126.com
大家知不知道,目前内毒素检测用的鲎试剂都暂停供货了,能买到的都是未经标定的,据说是中检所那边的问题,恢复供应要一个月之久,哪位版友知道具体情况啊?
随着血液净化技术的迅猛发展,越来越多的医院拥有透析中心,由反渗水和透析液的污染所引发的一些临床问题也渐渐引起血液净化工作者的重视。污染透析液中的细菌内毒素通过透析膜进入透析患者体内,引起致热原反应。反复出现致热原反应,不仅影响透析患者的透析效果,还和透析患者发生低蛋白血症、恶[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]、发热、炎症、弥漫性血管内凝血、多器官功能障碍综合征、内毒素休克等并发症密切相关,增加患者的住院率和病死率。我国卫生部要求各级卫生行政部门加强对血液透析质量的监管,其中就包括对透析用水及透析液内毒素污染的监测。厦门市鲎试剂实验厂有限公司研发部门已研制成功抗干扰能力强、稳定性强、重现性好的透析专用内毒素检测鲎试剂盒。 (来源:www.houshiji.com)
我是新手,我想请问一下做内毒素的洁净台可以和无菌室的洁净台公用一个吗?也就说内毒素和无菌室是可以在一起还是要分开。内毒素是测含量的话,应该用药典里的哪种方法? 谢谢了!
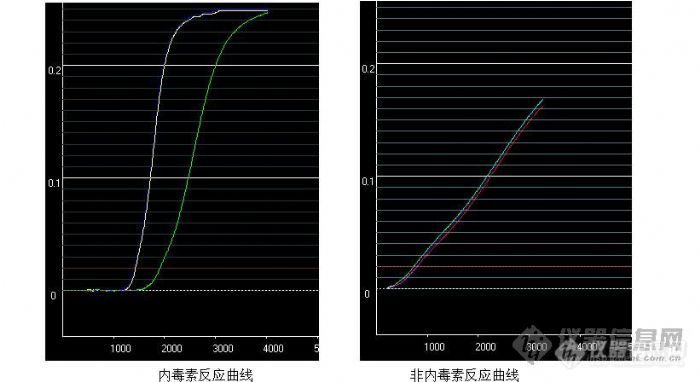
[center]非细菌内毒素反应曲线的发现[/center]鲎试剂的特异性系指在药品、生物制品和血液制品中鲎试剂能准确测出被测物质内毒素的能力,既不能造成样品内毒素的漏检,也不能将其它物质错判为内毒素。目前我公司研究证明,已知能与鲎试剂发生反应的物质有细菌内毒素和β-葡聚糖。中国药品生物制品检定所夏振民报道除(1-3)-β-葡聚糖外,(1-4)、(1-6)-β-葡聚糖同样使鲎试验产生阳性结果,这些物质的总称为真菌多糖,普遍存在于真菌细胞壁。如果这类物质具有像内毒素一样的致热活性,细菌内毒素检查和热原检查结果的符合率会接近一致,但是真菌多糖不是一种致热物质。这将导致在使用普通鲎试剂检测这些样品时,出现细菌内毒素检查不合格,热原检查合格的现象,造成对这些物质热原检查的错判(假阳性),将其它物质错判为内毒素,造成企业直接经济损失。判断假阳性的方法: 1、特异性鲎试剂法。特异性鲎试剂经特殊的工艺改造,只与细菌内毒素发生凝胶反应,阻断了β-葡聚糖生成凝胶的反应,避免假阳性的形成。本公司的鲎试剂特异性好,对药品中超量的细菌内毒素分辨率为100%,只与细菌内毒素发生凝胶反应,不与β-葡聚糖生成凝胶反应,避免假阳性的形成,避免将合格药品判为不合格而造成企业的经济损失;同时可避免因样品内毒素的漏检,造成临床用药的不良反应,保证患者用药安全。 2、定量反应曲线分析法。细菌内毒素、β-葡聚糖样物质与定量鲎试剂反应的区别:定量鲎试剂与细菌内毒素反应曲线为规则S型特征曲线,β-葡聚糖样物质与定量鲎试剂反应曲线为经过0点的斜线或不规则曲线;定量鲎试剂与细菌内毒素为变速反应,反应速度先慢然后变快最后又变慢,β-葡聚糖样物质与定量鲎试剂反应基本是恒速。通过观察定量反应的反应曲线及反应速度可以区分细菌内毒素和β-葡聚糖样物质。[img]http://ng1.17img.cn/bbsfiles/images/2009/06/200906011408_153048_1626679_3.jpg[/img]该反应曲线能直观的判断内毒素反应类型
本法系利用鲎试剂来检测或量化由革兰氏阴性菌产生的细菌内毒素,以判断供试品中细菌内毒素的限量是否符合规定的一种方法。 细菌内毒素检查包括两种方法,即凝胶法和光度测定法,后者包括浊度法和显色基质法。供试品检测时,可使用其中任何一种方法进行试验。当测定结果有争议时,除另有规定外,以凝胶法结果为准。 本试验操作过程应防止微生物和内毒素的污染。 细菌内毒素的量用内毒素单位(EU )表示,1EU 与1 个内毒素国际单位(IU )相当。 细菌内毒素国家标准品系自大肠埃希菌提取精制而成,用于标定、复核、仲裁鲎试剂灵敏度和标定细菌内毒素工作标准品的效价。 细菌内毒素工作标准品系以细菌内毒素国家标准品为基准标定其效价,用于试验中的赏试剂灵敏度复核、干扰试验及各种阳性对照。 细菌内毒素检查用水系指内毒素含量小于0.O15EU/ml(用于凝胶法)或0.005EU / ml (用于光度侧定法)且对内毒素试验无干扰作用的灭菌注射用水。 试验所用的器皿需经处理,以去除可能存在的外源性内毒素。耐热器皿常用干热灭菌法(250℃ 、30 分钟以上 ) 去除,也可采用其他确证不干扰细菌内毒素检查的适宜方法。若使用塑料器械,如微孔板和与微量加样器配套的吸头等,应选用标明无内毒素并且对试验无干扰的器械。
注射用水中有一项细菌内毒素的检测,从来没有做过,不知道要购买哪些仪器和试剂,望有经验的老师指点。
2016年6月1日,法国生物梅里埃宣布收购德国Hyglos公司,这家位于德国贝尔恩里德专业从事细菌内毒素检测的公司成立于2009年。Hyglos公司在药物制剂细菌内毒素检测用重组蛋白的研发及生产领域具有独特及公认的专业经验。 细菌内毒素是某些革兰氏阴性菌细胞壁中的一种成分,是一种热原性物质,会导致高热。药典标准规定在与血液系统及中枢神经系统有关的药物制剂中不得检出此类物质,例如注射剂及一些医疗器械。而且在生产用水等原材料和中间体中需定量检查细菌内毒素。 目前,细菌内毒素的检查依赖于鲎试剂,鲎在亚洲已濒临灭绝,在美国已受到保护,即使仅有微量细菌内毒素的存在,鲎的血液也会凝固。 Hyglos公司开发出一种利用重组蛋白的创新方法,减少了对鲎血液的需求,因此可以采用一系列完全标准化的反应来检测细菌内毒素。另外,当使用某些处方来生产生物技术药物时,这些处方可能会隐藏或“掩盖”细菌内毒素;Hyglos公司研发出一种独特的原创技术,用来防止细菌内毒素的“掩盖”,使得细菌内毒素可以被检测。 生物梅里埃工业部Nicolas Cartier 强调道:“Hyglos在重组蛋白领域的专业技术为细菌内毒素检测开辟了新领域。忠于我们的创新精神,我们对它的全新技术充满信心。其现有的产品组合丰富了我们在制药工业及医疗器械领域的微生物控制解决方案。” Hyglos公司市场部经理Wolfgang Mutter博士补充说:“我们非常高兴加入生物梅里埃。它在全球工业微生物控制领域的领导地位以及其商业网络覆盖范围为我们带来可靠前景,能够使制药生产商受益于我们所开发的用于细菌内毒素检测的可靠、有效的科学技术成果。” 目前,细菌内毒素市场约有2.5亿欧元规模,每年增长12%左右,这些大多得益于生物药物、医疗器械以及疫苗市场容量的增长。 为收购Hyglos公司全部股票,生物梅里埃需支付达2400万欧元,将在接下来3年分阶段完成。
求购一台进口的内毒素检测恒温培养箱,欢迎大家推荐!
1968年美国科学家Dr. Levin和Bang建立了鲎试验法。此后世界各国对鲎试剂的生产和应用得以迅速发展。1980年美国药典20版首先收载了细菌内毒素检 查法。随后,英国药典、日本药局方、中国药典等也相继收载了该方法。本文主要对中国药典1995年版与英国药典1995年增补本、美国药典23版和日本药局方13版等的细菌内毒素检查法进行了比较。1 检验品种的比较中国药典1995年版二部共收载细菌内毒素检查品种12个,2000年版二部增至47个,而美国药典23版收载了471个品种进行细菌内毒素检查。因此,我们需加紧对更多的品种进行细菌内毒素检查方法的研究,加快该法对药品检验的普及和推广工作,提高我国药品标准和检验水平。2 检验方法的比较细菌内毒素试验的方法有凝胶法、浊度法、显色基质法、免疫学法等。其中凝胶法多为限量 检查法,浊度法和显色基质法为定量检查法,且后两种方法都属于分光光度法。浊度法还可 分为终点浊度法和动态浊度法;显色基质法也可分为终点显色基质法和动态显色基质法。凝胶法是较为经典的方法,各国药典都有收载,而收载了细菌内毒素定量测定法的有美国药典、英国药典、欧洲药典和日本药局方等。中国药典1995年版只收载了凝胶法,2000年版才涉及到定量测定法。因此,我们还需要对细菌内毒素定量测定进行研究,需要有供定量测定 用的标准品、仪器和试剂,以后逐步建立起我国的细菌内毒素定量测定方法。3 细菌内毒素标准品各国药典均设置了细菌内毒素的标准品,其中中国药典、英国药典和美国药典还可采用根据标准品为基准进行标定的工作标准品或对照标准品。除英国药典采用U为内毒素的单位外,其余各国药典都用EU为内毒素的单位。美国药典和中国药典对内毒素标准品每一步稀释时的混匀时间作出了明确规定。除中国药典外,其余各国药典规定了内毒素标准贮备液在冰箱里保存不得超过14d,且用前应在旋涡混 合器上充分混合至少3min。
求购一台进口的内毒素检测恒温培养箱,欢迎大家推荐!
本文是USP24细菌内毒素检查法(BACTERLAL ENDOTOXINS TEST)的译文,但目前执行的标准是USP24版第二增补本(USP—NF19 Second Supplement)的细菌内毒素检查法,读者可对照学习,从中可看出USP24细菌内毒素检查的不足之处。本文将介绍用鲎试剂检测样品内或样品上存在的细菌内毒素浓度的方法。鲎试剂(Limulus Amebocyte,LAL)来自鲎的循环细胞,经水提取而行,制备和检验后,用于凝固法。反应的终点是将供检样品稀释后,与平行稀释的参考内毒素标准进行直接比较得到的。测得的内毒素含量用规定的内毒素单位表示。鲎试剂也是用浊度法或显色法来读取数据的,这些试齐只要能满足这些选择方法的要求,就可以使用。在做试验时,需要先做出一条标准曲线,并用该曲线计算供检样品的内毒素含量,包括样品和对照液加鲎试剂后的培育时间和在分光光度计上读取光密度时使用的波长等操作,都应该事先规定好。如果是终点浊度法,则到达培育期后,应立刻读取读数。而动力学检测(凶手浊度法和显色法),光密度的测定是贯穿于整个反应期间,而用于计算结果的百分数就是从这些读数中计算出来的。在用终点法的显色法检测时,在到达事先规定的反应时间后,添加停止酶反应的试剂使反应停止后,再读取数据。1、参考内毒素标准与对照内毒素标准参考内毒素标准(Reference standard endotoxin,RSE)是美国药典(USP)的内毒素参考标准,其效价为每瓶10 000个USP内毒素单位(EU)。每瓶参考内毒素标准加5ml鲎试剂用水(LAL Reagent Watet),用旋转搅拌器间歇搅拌30min使其溶解,制成原液,用这一原液制作合适的系列稀释。原液应保存于冰箱中,用于以后的稀释,但保存时间不得超过14d。用前,用旋转搅拌器强力搅拌至少3min,每一步稀释,至少搅拌30s,然后才能用它稀释下一步。经稀释的参考内毒素不得贮存待以后使用,因为吸附作用会使其失去活性。对照内毒素标准(Contuol standard endotoxin,CSE)是以参考内毒素标准为标准另行制备的。一批新的对照内毒素标准在使用前应进行检定。检定时使用的鲎试剂应为试验中使用的同批鲎试剂。参考内毒素标准对照内毒素标准进行检定时,可使用鲎试剂的凝固法,按“试验操作”进行。每批对照内毒素标准,至少取1瓶与1瓶参考内毒素标准进行对比。参考内毒素标准的每个稀释度作4管。每瓶或每个样品的对照内毒素标准的每个稀释度也都要4管。参考内毒素标准终点的对数Log10的平均值和对照内毒素标准终点的对数Log10平均值之间的差值的反对数等于对照内毒素标准效价的标定值。可根据情况,将其变换成每ng干燥制剂的单位数或每瓶所含的单位数。适宜的对照内毒素标准的效价应不小于2EU/ng也不大于50EU/ng。2、试验的准备鲎试剂的灵敏度应经过确证。试验中使用的所有容器和用具,都必须在≥250℃的烤箱中,用足够的时间进行加热处理、破坏这些用具表面上可能存在的外源性内毒素。内毒素试验的结果是否可靠,还必须从试验使用的各种用具、溶液、洗涤用品中取样或提取样品,并用适当的方法证明它们对反应没有抑制或拉强或其它干扰作用。可按下述方法进行抑制试验或增强试验。试验中应设置阴性对照。如果鲎试剂的原材料、生产方法或处方发生改变时都要重新进行试验。3、鲎试剂灵敏度的确认试验为了确认鲎试剂标签上的灵敏度,每批至少取1瓶样品进行检定。参考内毒素标准(或对照内毒素标准)作2倍系列稀释,稀释成2.0λ,1.0λ,0.5λ和0.25λ。其中λ是鲎试剂标签上的灵敏度EU/ml。上述4个稀释度和阴性对照都要重复做4管。所得结果的几何平均值的对数应大于或等于0.5λ,小于或等于2.0λ。每一批新的鲎试剂,使用前都必须作标签灵敏度的确认试验。4、抑制试验和增强试验用不超过地大有效稀释而检测不出内毒素的样品,不加或内毒素,使最后浓度等于2.0λ,1.0λ,0.5λ和0.25λ。按照试验操作(Test Procedure)项的规定用标准内毒素进行检定。不加和加内毒素的样品管至少做4管。同时,用水稀释上述相同浓度的内毒素和阴性对照各两管,做平行两管试验。按照计算和判定项的方法,计算样品终点内毒素浓度的几何平均值。如果所得结果大于或等于0.5λ,小于或等于2.0λ,则该样品适合作细菌内毒素检查。用中和、灭活或除去干扰物质方法或用不超过最大有效稀释度稀释检品后,可重做抑制试验和增强试验。如果用不超过最大有效稀释法,对已知加量的内毒素可以克服抑制和增强作用。则样品可以经过稀释后,再作内毒素检查。如果在试验条件下,对未处理的样品检查出有内源性内毒素。则该样品不适合用于作抑制或拉强试验。不过,这种样品可用超过滤法将存在的内毒素去掉或做适当稀释、使之适合于作抑制或增强试验。稀释未处理样品(像开瓶溶解或在使用前注射前稀释那样),稀释到检验不到内毒素但不超过最大有效稀释倍数。再用这些已稀释的样品重作抑制试验或增强试验。5、最大有效稀释度(MVD) 最大有效稀释度是指在使用时将药物溶解或稀释成恰好用于注射或其它非经口途径使用的浓度。有时为了避免给药量的体积(EU/ml)计算。用试剂标签上的灵敏度(EU/ml)λ除限定浓度,就可以得到MVD因子。如果某一试剂的限量浓度是按重量或按药品的活性单位
中国药典2005年版二部附录细菌内毒素检查法中的干扰试验,说:"使用的供试品溶液应为未检查出内毒素且不超过最大有效稀释倍数(MVD)的溶液."请问如果做注射用水的细菌内毒素,那么供试品溶液是什么样的注射用水?怎样处理不含内毒素?后面的"凝胶半定量试验"A "从通过干扰试验的稀释倍数开始"这个稀释倍数是定值吗?怎样求?"系列溶液A中每一系列平行管的终点稀释倍数乘以λ,"什么是终点稀释倍数?
细菌内毒素检查法应用与论坛[R].2005,4(1):9,做细菌内毒素检测,想参考一下,谁有这篇文章啊?
内毒素,它具体是什么物质?蛋白质还是多糖,或者...。不知能用HPCE 进行检测吗?安培检测器还是紫外检测器,哪个更好呢?
请问药物的内毒素检查是不是非要在无菌条件下检查??这问题可能很白痴,但请各位大侠赐教[em07]
请教一下各位:内毒素检查使用的工作标准品(中国药品生物制品检定所生产)的保质期一般是多长时间,盒子上写的是批号效期,比如说我现在所用的批号是150601-200964,不知道有哪位知道标准品的保质期呢?谢谢!