
[align=center][size=18px]鲜玉米青贮干样淀粉的测定[/size][/align][align=center][img]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311046569861_3622_5310370_3.png[/img][/align][align=center][size=12px]图1[/size][/align][align=left][size=16px]测定淀粉的主要方法有酶水解法、酸水解法、旋光法,但在牧场中,最常用酶水解法来测定鲜玉米青贮干样(见图1)中的淀粉。[/size][/align][align=left]1、 [size=16px]原理[/size][/align][align=left][size=16px]样品经除去脂肪及可溶性糖类后,其中淀粉用淀粉酶水解成小分子糖,再用盐酸将小分子糖水解成单糖,最后按还原糖测定。[/size][/align][align=left]2、 [size=16px]测定步骤[/size][/align][align=left][size=16px]2.1称取粉碎好的鲜玉米青贮2-5g,置于放有折叠滤纸的漏斗内。先用50mL 60-90℃的石油醚分5次洗去脂肪,再用150mL 85%无水乙醇洗去可溶性糖类,滤干乙醇,将残留物移入250mL烧杯内,并用50mL水冲洗滤纸,洗液一并倒入烧杯内(见图2),将烧杯置沸水浴上加热15min,使淀粉糊化,放冷到60℃以下,加20mL淀粉酶溶液,在55-60℃水浴1h,并不断搅拌。然后取1滴此液加1滴碘化钾溶液,若不显蓝色可进行下一步;若显蓝色,再加热糊化并加入20mL淀粉酶溶液,继续保温,直至加碘不显蓝色为止。加热至沸,冷却后移入200mL容量瓶中,并加水至刻度(见图3),混匀、过滤、弃去初滤液。取50mL滤液,置于200mL锥形瓶中,如5mL盐酸5ml盐酸(1+1),装上回流冷凝器,在沸水浴中回流1h,冷后用pH计,用氢氧化钠溶液(200g/L)、盐酸溶液调至中性,溶液转入100mL容量瓶中,洗涤锥形瓶,洗液并入100mL容量瓶中,加水至刻度,混匀备用。[/size][/align][align=center][img]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311046572565_7470_5310370_3.png[/img][size=16px] [/size][/align][align=center][size=12px]图2[/size][size=16px] [/size][/align][align=center][img]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311046577319_3570_5310370_3.png[/img][/align][align=center][size=12px]图3[/size][size=16px] [/size][/align][align=left][size=16px]2.2吸取5.0ml碱性酒石酸铜甲液及5.0ml碱性酒石酸铜乙液置于150ml锥形瓶中,加水10ml,加入玻璃珠2粒,从滴定管中滴加比预测体积少1ml的样品溶液至锥形瓶中,使在2min内加热至沸,趁沸以每2s1滴的速度滴定,直至蓝色刚好退去为终点,记录消耗样液体积。同法平行操作三份,得出平均消耗体积。[/size][/align][align=left][size=16px]同时,量取50ml水及与样品处理时相同量的淀粉酶溶液。[/size][/align][align=left]3、 [size=16px]计算结果[/size][/align][align=left][/align][align=left][size=16px]式中:[/size][img]" style="max-width: 100% max-height: 100% [/img]——试样中淀粉的含量,g/100g[/align][align=left] [img]" style="max-width: 100% max-height: 100% [/img]——测定用试样中葡萄糖的质量,mg[/align][align=left] [img]" style="max-width: 100% max-height: 100% [/img]——空白中葡萄糖的质量,mg[/align][align=left] [img]" style="max-width: 100% max-height: 100% [/img]——以葡萄糖计换算成淀粉的换算系数[/align][align=left] [img]" style="max-width: 100% max-height: 100% [/img]——称取试样的质量,g[/align][align=left] [img]" style="max-width: 100% max-height: 100% [/img]——测定用试样处理的体积,mL[/align]

[size=16px] 粮食水分测定仪通常可以用来测定各种类型的粮食的水分含量。这些粮食包括但不限于以下几种: 稻谷:如大米、小麦、稻米等。 谷物:如玉米、燕麦、大麦、小麦、大豆等。 油籽:如花生、大豆、棉籽、葵花籽等。 饲料:用于家禽、牲畜和宠物的饲料。 干果:如坚果、葡萄干、杏仁等。 豆类:如绿豆、红豆、黑豆等。 粉类产品:如面粉、淀粉、糯米粉等。 其他谷物和种子:如糙米、荞麦、草籽等。 粮食水分测定仪通常用于农业、食品加工、饲料生产等领域,以确保粮食和谷物的质量,并帮助控制储存条件,以防止霉变和腐败。不同类型的粮食可能有不同的水分标准,因此需要使用适当的水分测定仪来进行测试和监测。这些仪器通常使用不同的测量方法,如烘干法、微波法、红外法等,以确定粮食的水分含量。[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2023/09/202309071135162164_2545_6098850_3.png!w690x690.jpg[/img][/size]
所测定水分的范围大约在5-20%之间,如饲料及其添加剂,含量有高淀粉类物质等。要求:1、如果需要温度补偿的,最好有2、误差在0.2%以内3、测定速度较快且稳定4、价格适中由于是饲料及其添加剂,所以卡氏水分测定仪应该就不能用了,因为没有能使用样品都溶解的溶剂。快速水分测定仪 概述: 快速水分测定仪是迅速准确的测定物质水分的化验仪器,目前仪器原理有电阻法,电容法,高频法,近红外等。目前最成熟的就是电阻法,电容法,高频法,该仪器以稳定的性能,快速的检出结果赢得广大用户的好评。 以上是百度上获得,不知道有没有哪一种适合的。
所测定水分的范围大约在5-20%之间,如饲料及其添加剂,含量有高淀粉类物质等,最终产品是过20目的颗粒。要求:1、如果需要温度补偿的,最好有2、误差在0.2%以内3、测定速度较快且稳定4、价格适中由于是饲料及其添加剂,所以卡氏水分测定仪应该就不能用了,因为没有能使用样品都溶解的溶剂。快速水分测定仪 概述: 快速水分测定仪是迅速准确的测定物质水分的化验仪器,目前仪器原理有电阻法,电容法,高频法,近红外等。目前最成熟的就是电阻法,电容法,高频法,该仪器以稳定的性能,快速的检出结果赢得广大用户的好评。 以上是百度上获得,不知道有没有哪一种适合的。
我想请教一下淀粉方面的专家,国标里边说测定淀粉灰分要在900度,可我们一直在550渡测定(根据食品中灰分测定方法 ),是不是不太对?为什么淀粉要那么高温度灰化?
各位老大们:按GB测定淀粉“斑点”时,斑点究竟长什么样子,看异色斑还是什么啊?测定的目的和影响因素有哪些啊?我在做的时候称取完10g后淀粉要怎么样才算均匀分布在白色板上了,样本厚度大概有多少?以前以为挺简单的,结果现在才发现一团糟啊。
[align=center][font=DengXian]淀粉的测定[/font][/align][font=DengXian]淀粉是一种多糖。它广泛存在于植物的根、茎、叶、种子等组织中,是人类食物的重要组成部分,也是供给人体热能的主要来源。[/font][font=DengXian]淀粉是由葡萄糖单位构成的聚合体,按聚合形式不同,可形成两种不同的淀粉分子——直链淀粉和支链淀粉。[/font][font=DengXian]淀粉的主要性质如下:[/font][font=DengXian]①[/font][font=DengXian]水溶性:直链淀粉不溶于冷水,可溶于热水,支链淀粉常压下不溶于水。只有在加热并加压时才能溶解于水。[/font][font=DengXian]②[/font][font=DengXian]醇溶性:不溶于浓度在[/font]30[font=DengXian]%以上的乙醇溶液。[/font][font=DengXian]③[/font][font=DengXian]水解性:在酸或酶的作用下可以水解,最终产物是葡萄糖。[/font][font=DengXian]④[/font][font=DengXian]旋光性:淀粉水溶液具有右旋性[/font][[font=DengXian]α[/font]]20 [font=DengXian]为[/font](+)201.5-205[font=DengXian]。[/font][font=DengXian]⑤[/font][font=DengXian]与碘有呈色反应(是碘量法的专属指示剂)[/font][font=DengXian]淀粉的作用:[/font][font=DengXian]稳定剂——雪糕、冷饮食品[/font][font=DengXian]增稠剂——肉罐头[/font][font=DengXian]胶体生成剂[/font][font=DengXian]保湿剂[/font][font=DengXian]乳化剂[/font][font=DengXian]粘合剂[/font][font=DengXian]填充料——糖果[/font][font=DengXian]淀粉的测定方法有多种,根据淀粉的理化性质而建立的。常用的方法有:[/font] [font=DengXian]酸水解法[/font] [font=DengXian]酶水解法[/font] [font=DengXian]旋光法[/font] [font=DengXian]酸化酒精沉淀法:淀粉不溶于[/font]30%[font=DengXian]以上的乙醇[/font]
求助大米中直链淀粉和支链淀粉含量测定方法由于需要,需要测定大米中直链淀粉和支链淀粉的比例,方法越简单越好,结果可以不要求太精确有知道方法的,能不能提供一下,在此先谢谢了
[align=center][font=DengXian]淀粉的测定[/font]--[font=DengXian]旋光法[/font][/align][font=DengXian](一)[/font] [font=DengXian]原理[/font][font=DengXian]淀粉具有旋光性,在一定条件下旋光度的大小与淀粉的浓度成正比。用氯化钙溶液提取淀粉,使之与其他成分分离,用氯化锡沉淀提取液中的蛋白质后,测定旋光度,即可计算出淀粉含量。[/font]2[font=DengXian].适用范围及待点[/font] [font=DengXian]本法适用于淀粉含量较高,而可溶性糖类含量很少的谷类样品,如面粉、米粉等。操作简便、快速。[/font]GB/T 5009.9[font=DengXian]—[/font]2003[font=DengXian]《食品中淀粉的测定》[/font] 1. [font=DengXian]酶解[/font] [font=DengXian]酸解[/font] [font=DengXian]测定还原糖[/font] 2. [font=DengXian]酸水解[/font] [font=DengXian]测定还原糖[/font]
测定食品中的淀粉含量对于决定其用途具有重要意义,淀粉是供给人体热量的主要来源。淀粉在食品中的作用是作为增稠剂、凝胶剂、保湿剂、乳化剂、黏合剂等。直链淀粉不溶于冷水,但可溶于热水,支链淀粉常压下不溶于水。只有在加热并加压时才能溶解于水。淀粉不溶于浓度在30%以上的乙醇溶液。在酸或酶的作用下,淀粉可以发生水解,其水解最终产物是葡萄糖。淀粉水溶液具有右旋性20为(+)201.5一205。与碘发生呈色反应,这也是碘量法的专属指示剂。淀粉的测定方法有多种,可根据淀粉的理化性质而建立。淀粉因其品种不同,淀粉的大小和形状也不同,故淀粉的物理检验法常用显微镜分析法,可鉴别不同品种的淀粉。淀粉含量的常用化学测定方法包括酸水解法、酶水解法、旋光法和酸化酒精沉淀法等。一、酶水解法淀粉用麦芽淀粉酶水解成二糖,再用酸将二糖水解为单糖,然后测定由水解所得到的单糖,即还原糖。常用于液化的淀粉酶是麦芽淀粉酶。它是a一淀粉酶和β一淀粉酶的混合物。酶水解法的优点在于:在一定条件下,用a一淀粉酶处理样品,则能使淀粉与半纤维素等某些多糖分开来。因为a一淀粉酶具有严格的选择性,只能使淀粉液化变成低分子糊精和可溶性糖分,而对半纤维素不起作用。在用a一淀粉酶液化淀粉除去半纤维素等不溶性残留物后,再用酸水解使些成葡萄糖,所得结果比较准确。这种酶水解作用被称之为选择性水解。酶水解法测定淀粉的具体步骤如下。样品的处理。将磨碎样品置于漏斗中,用50mL乙醚分数次洗涤,除去脂肪,再用10%乙醇洗去可溶性糖分,共5次。酶水解开始要使淀粉糊化,将烧杯置沸水浴上加热15min,使放冷至60℃以下,然后再加入20mL淀粉酶溶液,在55一60℃保温1h,并不断搅拌。取1滴此液于白色点滴板上,加1滴碘液应不呈蓝色,若呈蓝色,再加热糊化,冷却至60℃以下,再加20mL淀粉酶溶液,继续保温,直至酶解液加碘液后不呈蓝色为止,加热至沸使酶失活,冷却后移入250mL容量瓶中,加水定容。混匀后过滤,弃去初滤液,收集滤液备用。用菲林试剂测定葡萄糖含量,同时做空白试验。淀粉=/式中:A—样品中淀粉相当于还原糖的重量,mg;B—空白相当于还原糖的重量;0.9—还原糖换算为淀粉因数;V/100—样液酶解后稀释至100mL,取VmL;W一样品重量,g。注意:淀粉酶水解时,发生了下述反应:(C6H10O5)n+nH20O→nC6Hl2O6故0.9份淀粉,水解后可得1份葡萄糖。所以,根据定量所得葡萄糖量乘以0.9,即得相应的淀粉含量。二、酸水解法样品经乙醚除去脂肪,乙醇除去可溶性糖类后,用盐酸水解淀粉为葡萄糖,按还原糖测定方法测定还原糖含量,再折算为淀粉含量。此法适用于淀粉含量较高,而半纤维素等其他多糖含量较少的样品。该法操作简单、应用广泛,但选择性和准确性不及酶法。于250mL锥形瓶中加入30mL6mol/L盐酸,装上冷凝管,置沸水浴中回流2h,速冷,定容,过滤,弃去初滤液,收集滤液备用。用菲林试剂测定葡萄糖含量,同时做空白试验。三、旋光法淀粉具有旋光性,在一定条件下旋光度的大小与淀粉的浓度成正比。用氯化钙溶液提取淀粉,使之与其他成分分离,用氯化锡沉淀提取液中的蛋白质后,测定旋光度,即可计算出淀粉含量。本法适用于淀粉含量较高,而可溶性糖类含量很少的谷类样品,如面粉、米粉等。操作简便、快速。将样品研细并通过40目以上的标准筛,称取2g样品,置于250mL烧杯中,加水10mL,搅拌使样品湿润,加入70mL氯化钙溶液,盖上表面皿,在5min内加热至沸并继续加热15min,加热时随时搅拌以防样品附在烧杯壁上。如泡沫过多可加1一2滴辛醇消泡。迅速冷却后,移入100mL容量瓶中,用氯化钙溶液洗净烧杯中附着的样品,洗液并入容量瓶中。加5mL氯化锡溶液,用氯化钙溶液定容到刻度,混匀,过滤,弃去除滤液,收集滤液装入旋光管中,测定旋光度。根据下式计算淀粉含量:淀粉=×100%式中:a—旋光度读数,度;L—旋光管长度,dm;m—样品质量,g;203—淀粉的比旋光度,度。
[align=center]【我们不一YOUNG】淀粉的测定--酶水解法[/align](一) 原理[img]https://ng1.17img.cn/bbsfiles/images/2024/07/202407261509074564_753_1615838_3.png[/img](二)适用范围及特点 因为淀粉酶有严格的选择性、只水解淀粉而不会水解其他多糖,水解后通过过滤可除去其他多糖。所以该法不受半纤维素、多缩戊糖、果胶质等多糖的干扰,适合于这类多糖含量高的样品,分析结果准确可靠,但操作复杂费时。(三)说明与讨论酶水解开始要使淀粉糊化 将烧杯置沸水浴上加热15分钟,冷至60℃以下,然后再加入20mL淀粉酶溶液,在55—60℃保温1小时,并不时搅拌。 取1滴此液于白色点滴板上,加1滴碘液应不呈蓝色,若呈蓝色,再加热糊化,冷却至60℃以下,再加20mL淀粉酶溶液,继续保温,直至酶解液加碘液后不呈蓝色为止,加热至沸使酶失活,冷却后移入250mL容量瓶中,加水定容。混匀后过滤,弃去初滤液,收集滤液备用。淀粉糊化——淀粉吸水溶胀,破坏晶格结构,变成粘度很大的淀粉糊,使其易被淀粉酶作用。糊化 = α-化糊化度又称α-化度酶水解未糊化淀粉速度:酶水解糊化淀粉速度= 1:20000 方便快餐食品经α-化后,复水性强,好消化。 方便面检测项目中有α-化度的测定。淀粉α化度的测定原理:已糊化的淀粉,在淀粉糖化酶的作用下,可水解为还原糖, α化度越高,即糊化的的淀粉越多,水解后生成的糖越多。先将样品充分糊化,经淀粉糖化酶水解后,用碘量法测糖含量。以此作为标准,糊化程度为100%。然后另取样品,不糊化,用淀粉糖化酶直接水解,用同样方法测定糖含量,通过计算可求出被测样品的相对糊化程度,即样品的α化度。
标准GB/T 15683-1995 稻米直链淀粉含量的测定中,淀粉标准溶液的制备挺麻烦的,要分别用马铃薯制备直链淀粉,用大米制备支链淀粉,再做成混合标准液。请问做过这个实验的高手,制备过程繁杂否?我看标准附录的步骤已经要吐血了。顺便问问,直链、支链淀粉标样有直接贩卖的没?
标准GB/T 15683-1995 稻米直链淀粉含量的测定中,淀粉标准溶液的制备挺麻烦的,要分别用马铃薯制备直链淀粉,用大米制备支链淀粉,再做成混合标准液。请问做过这个实验的高手,制备过程繁杂否?我看标准附录的步骤已经要吐血了。顺便问问,直链、支链淀粉标样有直接贩卖的没?
查了一些淀粉的测定方法,其中有用到耐高温淀粉酶,想知道怎么判断耐高温淀粉酶?该酶的商业名称?厂家?价格?还有浓度或者规格?大家还有什么好的测定淀粉的方法吗?
那位兄弟姐妹有比较快的方法来测定荞麦总淀粉的含量.. 因为样品太多了,用一样的方法真的慢死了.. 谢谢!
国标GBT20378-2006,想知道这个国标是针对什么东西的,是只对纯淀粉,还是可以用来测定像谷物里面的淀粉?如果只是针对纯淀粉,那谷物里面的淀粉要如何测定?
山东云唐智能科技有限公司生产的还原糖测定仪为集成化食品安全快速检测分析设备,采用台式一体化设计,主要用于各类蜂蜜品质的快速定量检测,应用于现场检测蜂蜜蔗糖、还原糖(葡萄糖和果糖)、羟甲基糠醛、酸度、农药残留、淀粉酶、脯氨酸、水分、糖分、灰分含量等项目。 该蜂蜜检测仪为集成化食品安全快速检测分析设备,目前已于食药监局、卫生部门、高教院校、科研院所、农业部门、蜜蜂养殖场、蜂蜜加工厂及检验检疫部门等单位广泛使用。
1 关于成品淀粉的酸度 成品淀粉的酸度是淀粉的重要质量指标之一,一般的表示方法以100g绝干淀粉消耗0.1mol/lNaOH溶液的ml数表示,淀粉的酸度是指淀粉中无机及有机酸的总量,按N1V1=N2V2,如果淀粉的酸度为10,即100g绝干淀粉消耗0.1mol/lNaOH10ml,折算成HCL量为0.1×10×0.036/100=0.00036,即相当于0.036%,指100g绝干淀粉中相当于含HCL0.036g。相当于氢0.1×10×0.001/100=0.00001可写成1×10-5。 2 关于淀粉的pH值 pH值的概念是指水溶液中氢离子浓度的负对数,即溶液中氢离子浓度倒数的对数值,pH值与氢离子浓度的关系式为: pH=log1/[H+] 例:若溶液的氢离子浓度为0.00001,可写成1×10-5 。则 pH=log1/1×10-5 =5 淀粉的pH值测定一般以20%淀粉溶液,用酸度计测定。有的淀粉指标规定淀粉的pH值为5~7,则氢离子浓度为0.00001~0.0000001。 3 关于淀粉酸度与pH的关系 淀粉的酸度高,肯定其pH低,但二者很难准确换算,因基准不同,酸度是以淀粉干物为基准,pH是指溶液状态,还涉及酸的解离度问题,淀粉中酸性物质主要是有机酸,化验的只是总酸度,而且是绝干状态为基准,不是溶液,不存在解离的氢离子浓度,故不能以简单的公式换算。若按以上公式换算,则酸度10ml相当于pH5。[em0815]
1 关于成品淀粉的酸度 成品淀粉的酸度是淀粉的重要质量指标之一,一般的表示方法以100g绝干淀粉消耗0.1mol/lNaOH溶液的ml数表示,淀粉的酸度是指淀粉中无机及有机酸的总量,按N1V1=N2V2,如果淀粉的酸度为10,即100g绝干淀粉消耗0.1mol/lNaOH10ml,折算成HCL量为0.1×10×0.036/100=0.00036,即相当于0.036%,指100g绝干淀粉中相当于含HCL0.036g。相当于氢0.1×10×0.001/100=0.00001可写成1×10-5 。 2 关于淀粉的pH值 pH值的概念是指水溶液中氢离子浓度的负对数,即溶液中氢离子浓度倒数的对数值,pH值与氢离子浓度的关系式为: pH=log1/[H+] 例:若溶液的氢离子浓度为0.00001,可写成1×10-5 。则 pH=log1/1×10-5 =5 淀粉的pH值测定一般以20%淀粉溶液,用酸度计测定。有的淀粉指标规定淀粉的pH值为5~7,则氢离子浓度为0.00001~0.0000001。 3 关于淀粉酸度与pH的关系 淀粉的酸度高,肯定其pH低,但二者很难准确换算,因基准不同,酸度是以淀粉干物为基准,pH是指溶液状态,还涉及酸的解离度问题,淀粉中酸性物质主要是有机酸,化验的只是总酸度,而且是绝干状态为基准,不是溶液,不存在解离的氢离子浓度,故不能以简单的公式换算。若按以上公式换算,则酸度10ml相当于pH5。
常温下淀粉不溶于水,GB5009.8里是对样品进行预处理后过滤,留下淀粉来水解进行测定的。如果是经过高温溶解形成稳定体系的淀粉含量应该如何测定呢?
gb/t15683-2008大米 直链淀粉含量的测定方法中的支链淀粉标液和马铃薯直链淀粉标液(1mg/ml)哪里有卖?这个标准有啥注意事项吗?曲线好做吗?有做过的大侠请赐教!没做过此项目,心里没底,不知好不好做
[align=center][font=DengXian]淀粉的测定[/font]--[font=DengXian]酸水解法[/font][/align][font=DengXian](一)[/font] [font=DengXian]原理[/font] [font=DengXian]样品经乙醚除去脂肪,乙醇除去可溶性糖类后,用盐酸水解淀粉为葡萄糖,按还原糖测定方法测定葡萄糖含量,再折算为淀粉含量。[/font][font=DengXian](二)方法[/font][font=DengXian]淀粉水解[/font] [font=DengXian]准确称取[/font]0.5g[font=DengXian]样品置入[/font]250mL[font=DengXian]三角瓶中,加[/font]50mL 1[font=DengXian]+[/font]4[font=DengXian]盐酸溶液,瓶口接上回流冷凝管或长玻璃管,于沸水浴中回流水解半小时,取出,迅速冷却,并用[/font]20[font=DengXian]%氢氧化钠溶液中和至中性或微酸性。脱脂棉过滤,滤液用[/font]250ml[font=DengXian]容量瓶接收。用水充分洗涤残渣,然后用水定容至刻度,摇匀,为供试糖液。[/font][font=DengXian](三)适用范围及特点[/font][font=DengXian]此法适用于淀粉含量较高,而半纤维素等其他多糖含量较少的样品。该法操作简单、应用广泛,但选择性和准确性不及酶法。[/font]
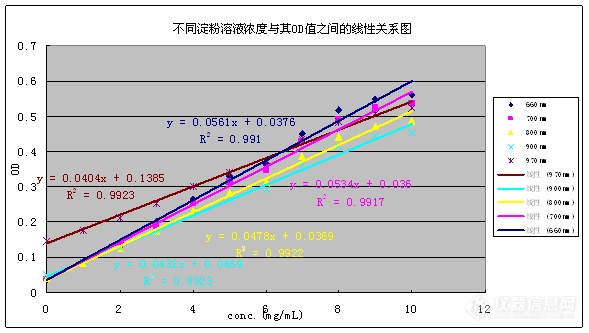
[align=center][b]使用酶标仪测定α-淀粉酶抑制率方法的研究[/b][/align][align=left][b]1.实验原理[/b][/align][align=left] 淀粉的消化主要有α-淀粉酶与α-葡萄糖苷酶的参与,α-淀粉酶水解α-1,4-连接键,消化的产物主要有麦芽糖、麦芽三糖、α-糊精,这些物质的进一步消化要在小肠上靠α-葡萄糖苷酶进行,α-葡萄糖苷酶主要包含麦芽-葡糖淀粉酶与蔗糖-异麦芽糖酶,α-葡萄糖苷酶水解的产物是葡萄糖。因此,通过抑制淀粉酶或葡萄糖苷酶的活性,阻碍食物中碳水化合物的水解与消化,减少糖分的吸收,以达到控制体内血糖浓度水平。[/align][align=left] 本实验是针对淀粉酶水解淀粉溶液而导致溶液中浑浊度的变化,测定溶液吸光度值的变化,以抑制剂阿卡波糖作为参照标准,抑制淀粉酶的能力以阿卡波糖当量来表达。[/align][align=left][b]2.实验方法与数据处理[/b] 将空白、样品或标准抑制剂Acarbose(阿卡波糖)与α-淀粉酶溶液混合均匀,37℃保温孵育15min,然后再加入淀粉溶液,快速振荡后在660nm迅速开始测定,利用酶标仪配备软件记录吸光度OD,初始吸光度值记为f1,以后每隔一段时间测定一个点,吸光度分别记为f1, f2 …,抑制剂作用下衰减曲线下的积分面积,扣除无抑制剂的空白曲线下面积,得出抑制剂的曲线下净面积(Net AUC)。衰退曲线下面积AUC可以近似看作各梯形面积之和,可以表达为:AUC=0.5×(f[sub]1[/sub]+f[sub]2[/sub])×ΔT+0.5×(f[sub]2[/sub]+f[sub]3[/sub])×ΔT+...+0.5×(f[sub]x[/sub]+f[sub]x+1[/sub])×ΔT+...+0.5×(f[sub]n-1[/sub] +f[sub]n[/sub])×ΔT=0.5×[2×(f[sub]1[/sub] +f[sub]2[/sub] +...+ f[sub]n-1[/sub] +f[sub]n[/sub])-f[sub]1[/sub] -f[sub]n[/sub]]×ΔT其中f[sub]n[/sub]代表第n个测定点时的吸光度,ΔT为相邻两个测定点之间的时间间隔,因本实验测定方法中ΔT设定为2min,一共有61测定点,因此该公式可以简化为:AUC=2×(f[sub]2[/sub]+f[sub]3[/sub]+...+f[sub]60[/sub])+ f[sub]1[/sub] + f[sub]61[/sub]以Acarbose当量μmol Acarbose equivalent/g (μmol AE/g)表达。[/align][align=left][b]3.试剂溶液的制备3.1 磷酸盐缓冲溶液3.1.1 CaCl[sub]2[/sub]溶液[/b]准确称取CaCl[sub]2[/sub]2H[sub]2[/sub]O粉末0.25g溶于100 mL ddH[sub]2[/sub]O,即为CaCl[sub]2[/sub]溶液2500mg/L。[b]3.1.2缓冲溶液工作液[/b]分别称取8.9g Na[sub]2[/sub]HPO[sub]4[/sub]2H[sub]2[/sub]O与6.9g NaH[sub]2[/sub]PO[sub]4[/sub]H[sub]2[/sub]O于1000 mL容量瓶中,再量取CaCl[sub]2[/sub]溶液20 mL,混合后用ddH[sub]2[/sub]O定容至1000 mL,这样得到0.1M,pH 6.9的缓冲溶液,冰箱下贮存。[b]3.2 玉米淀粉溶液[/b]玉米淀粉储备液:准确称取约1.0000g大米淀粉,加入50mL缓冲液,磁力搅拌数分钟后置于78℃左右水浴10分钟,于磁力搅拌器中搅拌自然冷却至室温,即为2%的淀粉溶液(20mg/mL);玉米淀粉工作液:将储备液用缓冲溶液依次分别稀释至1.0-10mg/mL的工作液。[b]3.3 α-淀粉酶溶液[/b]准确称取α-淀粉酶固体粉末(23U/mg)40mg,用缓冲溶液定容至10 mL,即为4mg /mL的α-淀粉酶储备液,再依次稀释至0.2、0.1、0.05、0.04、0.025 mg /mL的α-淀粉酶工作液。[b]3.4 Acarbose标准溶液的配制[/b]0.1g acarbose定容到100 mL磷酸缓冲液中,得到1mg /mL贮备液,然后用磷酸缓冲溶液依次稀释成的工作液0.01、0.02、0.03、0.04、0.05 mg /mL。[b]4.研究步骤[/b][/align][align=left][b]4.1 淀粉溶液的线性范围[/b] 由于本实验是对样品中浑浊度的变化来进行,而对浑浊度的测量不像紫外-可见分光光度计那样有理想的波长以及会出现明显的特征峰,根据文献大多数浑浊度的测量波长在620-700nm之间。为了确定玉米淀粉溶液的线性,我们选择玉米淀粉溶液的浓度在0-10mg/mL,波长选择660、700、800、900、970nm进行比较。使用玉米淀粉工作液0-10mg/mL,分别在660nm、700nm、800nm、900nm、970nm波长下测定其吸光度,重复测定3次。不同波长下淀粉溶液浓度与其OD值之间的线性关系图如下:[/align][align=left][img=,589,333]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171420555396_7331_1613776_3.png!w589x333.jpg[/img][/align][align=left][table][tr][td][align=center]波长/nm[/align][/td][td][align=center]线性相关系数R[sup]2[/sup][/align][/td][td][align=center]线性斜率[/align][/td][td][align=center]空白OD值[/align][/td][td][align=center]LOD检测限[/align][/td][td][align=center]LOQ定量限[/align][/td][/tr][tr][td][align=center]660[/align][/td][td][align=center]0.9910[/align][/td][td][align=center]0.0561[/align][/td][td][align=center]0.038±0.001[/align][/td][td][align=center]0.048[/align][/td][td][align=center]0.159[/align][/td][/tr][tr][td][align=center]700[/align][/td][td][align=center]0.9917[/align][/td][td][align=center]0.0534[/align][/td][td][align=center]0.038±0.001[/align][/td][td][align=center]0.052[/align][/td][td][align=center]0.174[/align][/td][/tr][tr][td][align=center]800[/align][/td][td][align=center]0.9922[/align][/td][td][align=center]0.0478[/align][/td][td][align=center]0.041±0.002[/align][/td][td][align=center]0.093[/align][/td][td][align=center]0.310[/align][/td][/tr][tr][td][align=center]900[/align][/td][td][align=center]0.9923[/align][/td][td][align=center]0.0432[/align][/td][td][align=center]0.051±0.002[/align][/td][td][align=center]0.108[/align][/td][td][align=center]0.361[/align][/td][/tr][tr][td][align=center]970[/align][/td][td][align=center]0.9923[/align][/td][td][align=center]0.0404[/align][/td][td][align=center]0.145±0.002[/align][/td][td][align=center]0.138[/align][/td][td][align=center]0.458[/align][/td][/tr][/table]从上图及上表中可以知道,玉米淀粉浓度在0-10mg/mL时的线性关系均较好,相关系数均在0.99以上。虽然线性相关系数较低,但在波长660nm下的线性斜率高于其他波长下的线性斜率,且LOD检测限与LOQ定量限均是最小,因此选择波长660nm作为测定波长。[/align][align=left][b]4.2 淀粉酶的活力[/b] 将20μL的缓冲溶液与20μL的不同浓度α-淀粉酶溶液混合均匀,37℃保温孵育15min,然后再加入60μL的2%淀粉溶液,快速振荡后在660nm迅速开始测定其吸光度值。以不同浓度的淀粉酶浓度0.4、0.2、0.1、0.05、0.04、0.025 mg /mL,底物选择20mg/mL的淀粉溶液进行试验,在660nm下测定其吸光度值的变化曲线。660nm下其吸光度值的衰退曲线图:[/align][align=left][img=,672,359]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171423163167_2471_1613776_3.png!w672x359.jpg[/img][/align][align=left]从上图,在660nm波长下,不同淀粉酶浓度使淀粉溶液的吸光度下降,而且淀粉酶浓度越大,吸光度下降的越快。AUC与淀粉酶浓度成负相关关系,随着酶浓度的增大,曲线下面积AUC逐渐减小。[/align][align=left][b]4.3 抑制剂阿卡波糖活力[/b] 采用不同浓度的阿卡波糖浓度0.01、0.02、0.03、0.04、0.05 mg /mL分别进行试验(n=3),淀粉溶液的浓度选择20mg/mL,淀粉酶浓度选择0.2mg /mL。通过试验,各个不同浓度的阿卡波糖抑制曲线图如下:[/align][align=left][img=,687,390]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171426550249_8100_1613776_3.png!w687x390.jpg[/img][img=,668,320]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171426580379_7253_1613776_3.png!w668x320.jpg[/img][/align][align=left]从上图看出,阿卡波糖浓度 在0.01-0.05 mg /mL之间与其曲线下净面积Net AUC的线性较好,相关系数R[sup]2[/sup]=0.9972。[/align][align=left][b]4.4 线性研究[/b] 以不同浓度的阿卡波糖0.01、0.02、0.03、0.04、0.05、0.06、0.07mg /mL分别进行试验,淀粉溶液的浓度选择20mg/mL,淀粉酶浓度选择0.2mg /mL。通过试验,各个不同浓度的阿卡波糖抑制曲线图如下:[/align][align=left][img=,690,359]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171427557847_1976_1613776_3.png!w690x359.jpg[/img][/align][align=left]不同浓度的阿卡波糖与其曲线下净面积Net AUC的线性关系图如下(重复试验7次):[/align][align=left][img=,690,359]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171427580179_2403_1613776_3.png!w690x359.jpg[/img][/align][align=left][table][tr][td][align=center]n[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][td][align=center]6[/align][/td][td][align=center]7[/align][/td][td][align=center]av[/align][/td][td][align=center]SD[/align][/td][td][align=center]%RSD[/align][/td][/tr][tr][td][align=center]R[sup]2[/sup][/align][/td][td][align=center]0.9909[/align][/td][td][align=center]0.9806[/align][/td][td][align=center]0.9788[/align][/td][td][align=center]0.9942[/align][/td][td][align=center]0.9934[/align][/td][td][align=center]0.991[/align][/td][td][align=center]0.9932[/align][/td][td][align=center]0.9889[/align][/td][td][align=center]0.0064[/align][/td][td][align=center]0.6477[/align][/td][/tr][tr][td][align=center]SLOPE[/align][/td][td][align=center]4433.9[/align][/td][td][align=center]4850.1[/align][/td][td][align=center]4500[/align][/td][td][align=center]4219.3[/align][/td][td][align=center]5675.1[/align][/td][td][align=center]4468[/align][/td][td][align=center]5110.9[/align][/td][td][align=center]4751[/align][/td][td][align=center]503.27[/align][/td][td][align=center]10.593[/align][/td][/tr][/table]从上表看出,不同浓度的阿卡波糖与其曲线下净面积Net AUC之间的线性相关系数R[sup]2[/sup]在0.9889±0.0064之间,相对标准偏差0.65%;斜率在4751±503.3之间,相对标准偏差10.6%。[/align][align=left][b]4.5 提取溶剂的影响[/b]对提取溶剂(丙酮:乙醇:水的混合溶剂)进行研究,即以提取溶剂代替缓冲溶液进行试验,并与缓冲溶液进行比较。[/align][align=left][img=,609,340]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171437196510_7149_1613776_3.png!w609x340.jpg[/img][/align][align=left]其中:BLK——20μL缓冲溶液+20μL淀粉酶+60μL淀粉;BLK1——20μL提取溶剂+20μL淀粉酶+60μL淀粉;Emp——40μL缓冲溶液+60μL淀粉;Emp1——40μL提取溶剂+60μL淀粉。[/align][align=left]通过对提取溶剂稀释10、100、1000、10000倍后再进行同样试验(如下图):[/align][align=left][img=,657,362]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171438035079_1244_1613776_3.png!w657x362.jpg[/img][/align][align=left]从图上看出,通过对提取溶剂稀释10、100、1000、10000倍后试验,基本对测定无影响。[/align][align=left][b][b]4.6 样品检测[/b][/b][/align][align=left][b] 将[/b]样品提取液代替阿卡波糖加入到淀粉酶溶液中,37℃保温孵育15min,然后再加入淀粉溶液,快速振荡后在660nm迅速开始测定。通过计算得出样品中的AE(阿卡波糖当量)。也可以通过比较抑制率IC50,来判断样品中的淀粉酶抑制率强弱。[/align][align=left][b]5.小结[/b] 通过以上对α-淀粉酶抑制率试验方法进行研究,实验表明,该方法适用于样品中α-淀粉酶抑制率的筛选。[/align][align=left]注意事项:[/align][align=left]1. 标准溶液或者样品与淀粉酶溶液混合后需在37℃保温孵育15min,再加入淀粉溶液;[/align][align=left]2. 加入淀粉溶液让后需要快速振荡后在660nm迅速开始测定;[/align][align=left][b]6.参考文献[/b]1. LEE WAH KOH, LIN LING WONG, YING YAN LOO, STEFAN KASAPIS, AND DEJIAN HUANG. J. Agric. Food Chem. 2010, 58, 148-1542. ALVIN ENG KIAT LOO AND DEJIAN HUANG. J. Agric. Food Chem. 2007, 55, 9805-98103. Elena Lo Piparo, Holger Scheib,Nathalie Frei, Gary Williamson, Martin Grigorov, and Chieh Jason Chou. J. Med. Chem. 2008, 51, 3555-35614. TOSHIRO MATSUI, TAKASHI TANAKA, SATOMI TAMURA, ASAMI TOSHIMA,KEI TAMAYA,YUJI MIYATA,KAZUNARI TANAKA, AND KIYOSHI MATSUMOTO. J. Agric. Food Chem. 2007, 55, 99-105[/align]

[size=16px] 土壤盐分测定仪行业应用 土壤盐分测定仪在农业、环境科学、土地管理和土壤研究等行业中有广泛的应用,主要用于以下方面: 农业管理:农业领域使用土壤盐分测定仪来监测土壤中的盐分水平。高盐分土壤可能对作物生长产生负面影响,因此农民和农业专家使用这些仪器来评估土壤盐分,并相应地管理土地和灌溉系统,以确保作物的健康生长。 灌溉管理:土壤盐分测定仪可以帮助农民和灌溉系统管理者监测土壤盐分水平,以优化灌溉方案。正确的灌溉管理可以减少土壤盐分积累,提高土地的可持续性。 土地恢复:在受盐碱化影响的土地上,土壤盐分测定仪可以用来监测土壤的盐分状况,并评估土地恢复工程的效果。这对于将受损土地恢复为农业用地非常重要。 土地规划:土壤盐分测定仪可用于土地规划和土地使用决策。它可以帮助政府、土地管理机构和城市规划者确定哪些土地适合农业、建筑或其他用途,以及如何最好地管理和改善土壤质量。 环境监测:土壤盐分测定仪也用于环境科学领域,以监测盐分对生态系统的影响。这包括湿地和沿海生态系统,以及受盐分污染影响的土地。 总之,土壤盐分测定仪在不同行业中都具有广泛的应用,有助于有效管理土壤盐分,保护土地资源,提高农业生产力,实施可持续土地管理和环境保护。[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2023/10/202310241005038778_5755_6098850_3.jpg!w690x690.jpg[/img][/size]
淀粉体外消化请问淀粉体外消化率怎么测定?
我公司想要求购一批粉尘测定仪,主要对露天的煤场进行环境测定,能否推荐几款产品型号?多谢!!!主要的产品要求是:直读式,中等流量,连续采样时间在4h以上,最好能定时采样。
我主要做饲料及其原料中淀粉含量的测定,拟用旋光仪检测,GB/T 20194-2006中的前处理方法很繁琐,时间也很长,不知道有没有更为简便适用的方法。
pH值的测定方法求小麦淀粉、马铃薯淀粉、复合磷酸盐的pH值测定方法。待测溶液需要多少样品和水分配比啊?这个标准(GB8884-2007马铃薯淀粉)适用小麦淀粉吗 ?
有谁知道淀粉总酸度测定的方法有哪些种类有知道的就帮帮我谢谢
为何用酸水解法测定淀粉含量,在水解完后需要调节其PH值