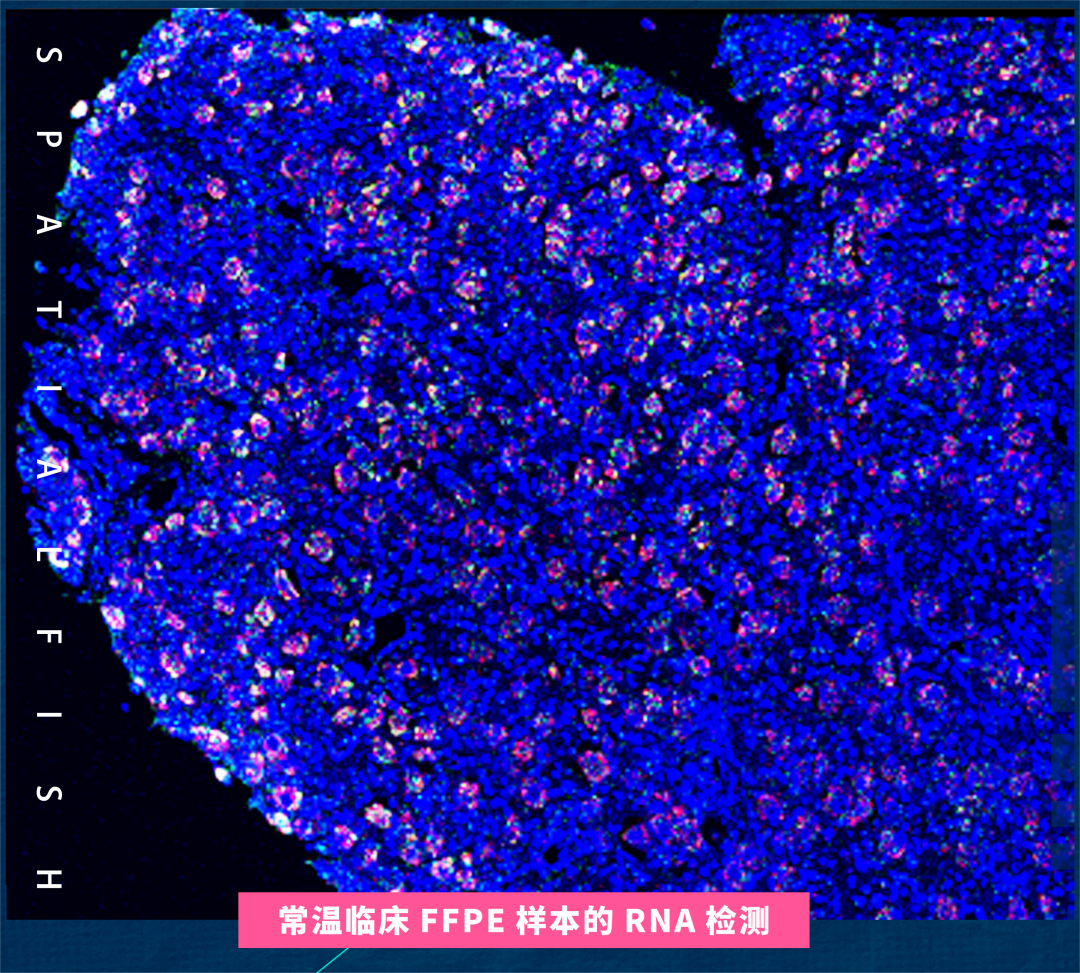
低温电镜解析蛋白结构十大进展
结构生物学领域有一条不成文的观点:结构决定功能。只有知道生物分子的原子排布,科学家们才能了解这个蛋白的功能。几十年来,分析蛋白结构有一个无冕之王——X射线晶体衍射。在X射线晶体衍射中,科学家们让蛋白结晶,然后利用X射线照射,随后根据X射线的衍射来重建蛋白的结构。在蛋白质数据银行(Protein Data Bank)的100000多条蛋白词目里,超过90%的蛋白结构是利用X射线晶体衍射技术解析得到的。 尽管X射线晶体衍射一直是结构生物学家的最佳工具,但是它存在较大的限制。科学家们将蛋白进行大块结晶通常需要多年的时间。而很多基础蛋白分子,例如嵌在细胞膜上的蛋白,或是形成复合体的蛋白却无法被结晶。 X射线晶体衍射技术(X-ray crystallography)即将成为历史,低温电子显微技术(cryo-electron microscopy, 也称作electron cryomicroscopy, cryo-EM)引发结构生物学变革。 低温电子显微镜适用于研究大的、稳定的分子,这些分子能够承受电子的轰击,而不发生变形——由多个蛋白组成的分子机器是最好的样本。因此由RNA紧紧围绕的核糖体是最佳的样本。三位化学家用X射线晶体衍射研究核糖体溶液的工作在2009年获得了诺贝尔化学奖,但这些工作花了几十年。近几年,低温电镜研究者们也陷入了“核糖体热”。多个团队研究了多种生物的核糖体,包括人类核糖体的首个高清模型。X射线晶体衍射的研究成果远远落后于LMB的Venki Ramakrishnan实验室,Venki获得了2009年的诺奖。Venki表示,对于大分子来说,低温电子显微镜远比X射线晶体衍射要实用。 这几年,低温电子显微镜的相关文章有很多:2015年一年,这个技术就用于100多个分子的结构研究。X-射线晶体衍射只能对单个、静态的蛋白晶体成像,但低温电子显微镜能够对蛋白的多种构象进行成像,帮助科学家们推断蛋白的功能。 现在低温电镜迅猛发展,专家们正在寻找更大的挑战作为下一个解析目标。对很多人来说,最想解析的是夹在细胞膜内的蛋白。这些蛋白是细胞信号通路中的关键分子,也是比较热门的药物靶标。这些蛋白很难结晶,而低温电子显微镜不大可能对单个蛋白进行成像,这是因为很难从背景噪音中提取这些信号。 这些困难都无法阻挡加利福利亚大学(University of California)的生物物理学家程亦凡。他计划解析一种细小的膜蛋白TRPV1。TRPV1是检测辣椒中引起灼烧感的物质的受体,并与其它痛感蛋白紧密相关。加利福利亚大学病理学家David Julius等人之前尝试结晶TRPV1,结果失败。用低温电子显微镜解析TRPV1项目,一开始进展缓慢。但2013年底,技术进步使得这一项目有了重大突破,他们获得了分辨率为0.34纳米的TRPV1蛋白的结构。该成果的发表对于领域来说,无异于惊雷。因为这证实了低温电子显微镜能够解析小的、重要的分子。 尽管低温电子显微镜发展迅速,很多研究者认为,它仍有巨大提升空间。他们希望能制造出更灵敏的电子探测器,以及更好地制备蛋白样本的方法。这样的话,就能够对更小的、更动态的分子进行成像,并且分辨率更高。5月,有研究者发表了一篇细菌蛋白的结构,分辨率达到了0.22纳米。这也显示了低温显微镜的潜力。 1997年时,英国医学研究委员会分子生物学实验室结构生物学家Richard Henderson非常坚定地宣称,低温电镜会成为解析蛋白结构的主流工具。在将近20年后的今天,他的预测比当年有了更多底气。Henderson表示,如果低温电镜保持这样的势头继续发展,技术问题也得以解决,那么低温电镜不仅会成为解析蛋白结构的第一选择,而是主流选择。这个目标已经离我们不远了。 1. 施一公小组在《Science》发两篇论文报道剪接体三维结构 U4/U6.U5 tri-snRNP电镜密度及三维结构示意图。 2015年8月21日,清华大学生命科学学院施一公教授研究组在国际顶级期刊《科学》(Science)同时在线发表了两篇背靠背研究长文,题目分别为“3.6埃的酵母剪接体结构”(Structure of a Yeast Spliceosome at 3.6 Angstrom Resolution)和“前体信使RNA剪接的结构基础”(Structural Basis of Pre-mRNA Splicing)。第一篇文章报道了通过单颗粒冷冻电子显微技术(冷冻电镜)解析的酵母剪接体近原子分辨率的三维结构,第二篇文章在此结构的基础上进行了详细分析,阐述了剪接体对前体信使RNA执行剪接的基本工作机理。清华大学生命学院博士后闫创业、医学院博士研究生杭婧和万蕊雪为两篇文章的共同第一作者。 这一研究成果具有极为重大的意义。自上世纪70年代后期RNA剪接的发现以来,科学家们一直在步履维艰地探索其中的分子奥秘,期待早日揭示这个复杂过程的分子机理。施一公院士研究组对剪接体近原子分辨率结构的解析,不仅初步解答了这一基础生命科学领域长期以来备受关注的核心问题,又为进一步揭示与剪接体相关疾病的发病机理提供了结构基础和理论指导。详细新闻报道参见:施一公研究组在《科学》发表论文报道剪接体组装过程重要复合物U4/U6.U5 tri-snRNP的三维结构。(Science, 20 Aug 2015, doi: 10.1126/science.aac7629 doi: 10.1126/science.aac8159) 2. Science:HIV重大突破!史上最详细HIV包膜三维结构出炉! 这项研究首次解析出HIV Env三聚体处于自然状态下的高分辨率结构图,其中HIV利用Env三聚体侵入宿主细胞。图片来自The Scripps Research Institute。 在一项新的研究中,TSRI的研究人员解析出负责识别和感染宿主细胞的HIV蛋白的高分辨率结构图片。相关研究结果发表在2016年3月4日那期Science期刊上,论文标题为“Cryo-EM structure of a native, fully glycosylated, cleaved HIV-1 envelope trimer”。 这项研究是首次解析出这种被称作包膜糖蛋白三聚体(envelope glycoprotein trimer,以下称Env三聚体)的HIV蛋白处于自然状态下的结构图。这些也包括详细地绘制这种蛋白底部的脆弱位点图,以及能够中和HIV的抗体结合位点图。(Science, 04 Mar 2016, doi: 10.1126/science.aad2450) 3. Nature:史上最详细转录因子TFIID三维结构出炉,力助揭示人类基因表达秘密 在一项新的研究中,来自美国加州大学伯克利分校、劳伦斯伯克利国家实验室和西班牙国家研究委员会(CSIC)罗卡索拉诺物理化学研究所的研究人员在理解我们体内被称作转录起始前复合物(pre-initiation complex, PIC)的分子机构(molecular machinery)如何发现合适的DNA片段进行转录方面取得重大进展。他们史无前例地详细呈现一种被称作TFIID的转录因子所发挥的作用。相关研究结果于2016年3月23日在线发表在Nature期刊上,论文标题为“Structure of promoter-bound TFIID and model of human pre-initiation complex assembly”。论文通信作者是劳伦斯伯克利国家实验室生物物理学家Eva Nogales,论文第一作者是Nogales实验室生物物理学研究生Robert Louder。其他作者是Yuan He、José Ramón López-Blanco、Jie Fang和Pablo Chacón。 这一发现是非常重要的,这是因为它为科学家们理解和治疗一系列恶性肿瘤铺平道路。Eva Nogales说,“理解细胞中的这种调节过程是操纵它或当它变坏时修复它的唯一方式。基因表达是包括从胚胎发育到癌症在内的很多重要生物学过程的关键。一旦我们能够操纵这些基本机制,那么我们就能够要么校正应当或不应当存在的基因表达,要么阻止这种过程[即基因表达]失去控制时的恶性状态。”(Nature, 31 March 2016, doi:10.1038/nature17394) 4. Science:科学家成功解析人类剪接体关键结构 在最近发表的一篇Science研究论文中,来自德国的科学家们利用冷冻电镜技术首次在分子级分辨率水平上重现了人类剪接体中一个关键复合体——U4/U6.U5 tri-snRNP的结构。剪接体是一种由RNA和蛋白质组成的用于切掉mRNA前体中内含子的分子机器。该研究解析的U4/U6.U5 tri-snRNP是构成剪接体的一个重要组成部分,研究人员利用单颗粒冷冻电镜获得了人类U4/U6.U5 tri-snRNP的三维结构,该复合体分子量达到180万道尔顿,解析分辨率达到7埃。该研究模型揭示了Brr2 RNA解螺旋酶如何在分离的人类tri-snRNP中通过空间结构阻止未成熟的U4/U6 RNA发生解链,还展现了泛素C端水解酶样蛋白Sad1如何将Brr2固定在预激活位置。 研究人员将他们获得的结构模型与酿酒酵母tri-snRNP以及裂殖酵母剪接体的结构进行了对比,结果表明Brr2在剪接体激活过程中发生了显著的构象变化,支架蛋白Prp8也发生了结构变化以容纳剪接体的催化RNA网络。(Science, 25 Mar 2016, doi: 10.1126/science.aad2085) 5. 北京大学毛有东、欧阳颀课题组与其合作者在Science发表炎症复合体冷冻电镜结构 炎症复合体三维结构 北京大学物理学院毛有东研究员、北京大学物理学院/定量生物学中心欧阳颀院士与哈佛医学院吴皓教授合作利用冷冻电子显微镜技术解析了近原子分辨率的炎症复合体的三维结构,首次阐释了其复合物在免疫信号转导过程中的单向多聚活化的分子结构机理。该研究工作以“Cryo-EM Structure of the Activated NAIP2/NLRC4 Inflammasome Reveals Nucleated Polymerization”为题于2015年10月8日在线发表在国际期刊Science。 先天免疫是人类免疫系统的重要组成部分,炎症复合体在触发先天免疫响应的过程中起到了关键信号转导的效应器作用,从而启动细胞凋亡等免疫应答和炎症反应。炎症复合体是胞浆内一组复杂的多蛋白复合体,是胱天蛋白酶活化所必需的反应平台,其复合物单体由多个结构域构成,并在上游蛋白的激活下诱导组装形成环状复合物。炎症复合体的结构对于认识先天免疫的信号转导过程、免疫调控和病原诱导活化等免疫响应机理具有关键的核心价值,因而成为国内外一流结构生物学和免疫学实验室追捧的研究对象。(Science, 23 Oct 2015, 10.1126/science.aac5789) 6. Nature:施一公团队揭示γ -分泌酶原子分辨率结构 人体γ -分泌酶3.4埃三维结构 日前,清华大学教授施一公团队与国外学者合作,构建了分辨率高达3.4埃的人体γ -分泌酶的电镜结构,并且基于结构分析了γ -分泌酶致病突变体的功能,为理解γ -分泌酶的工作机制以及阿尔茨海默氏症的发病机理提供了重要基础。相关成果8月18日在《自然》发表。 阿尔茨海默氏症是最为严峻的老年神经退行性疾病之一,但其发病机理尚待揭示。目前研究已知β -淀粉样沉淀是该病的标志性症状之一。而β -淀粉样沉淀的产生是APP蛋白经过一系列蛋白酶切割产生的短肽聚集而来。在此切割过程中,最关键的蛋白酶是γ -分泌酶。γ -分泌酶由四个跨膜蛋白亚基组成,其中,编码Presenilin(PS1)蛋白的基因中有200多个突变与阿尔茨海默氏症病人相关。γ -分泌酶在阿尔茨海默氏症的发病中扮演着重要角色。 研究人员通过收集更多的数据、大量的计算并升级分类方法,计算构建出3.4埃原子分辨率γ -分泌酶的三维结构,可以观察到绝大部分氨基酸的侧链以及胞外区部分糖基化修饰和结合的脂类分子。在高分辨结构的基础上,施一公研究组对PS1上的致病性突变体进行了研究,发现这些突变主要集中在两个较为集中的区域内。他们对于其中一些突变体进行了生化性质的研究,发现这些突变会影响γ -分泌酶对于底物APP的酶切活性,然而对切割活性的影响却有所不同。(Nature, 10 September 2015, doi:10.1038/nature14892) 7. Nature:人类核糖体结构终于被解析! 核糖体是进行蛋白质翻译的机器,能够催化蛋白质合成。目前,许多研究已经对多种生物的核糖体结构进行了原子水平的结构解析,但获得人核糖体结构一直存在很大挑战,这一问题的解决对于人类疾病的深入了解以及治疗手段和策略的开发都有重要意义。 近日,著名国际学术期刊nature在线发表了法国科学家关于人类核糖体结构解析的最新研究进展。 在该项研究中,研究人员利用高分辨率单颗粒低温电子显微镜以及原子模型构建的方法获得了人类核糖体接近原子水平的结构。该核糖体结构的平均分辨率为3.6A,接近最稳定区域的2.9A分辨率水平。这一研究成果对人类核糖体RNA,氨基酸侧链的实体结构,特别是转运RNA结合位点以及tRNA脱离位点处的特定分子相互作用提供了深入见解,揭示了核糖体大小亚基接触面的原子细节,发现在核糖体大小亚基的旋转运动过程中,其接触面发生了强烈的重构过程。(Nature, 30 April 2015, doi:10.1038/nature14427) 8. Nature:日本科学家成功解析代谢关键因子受体结构 近日,著名国际学术期刊nature在线发表了日本科学家的最新研究进展,他们利用结构生物学方法对脂联素(adiponectin)受体,AdipoR1和AdipoR2,进行了结构解析,发现脂联素受体具有与G蛋白偶联受体不同的七次跨膜螺旋,对于靶向脂联素受体的肥胖及其相关代谢疾病治疗方法开发具有重要意义。 在该项研究中,研究人员对人类AdipoR1和AdipoR2的晶体结构进行了解析,分辨率分别达到2.9 ?和2.4 ?,他们通过解析发现脂联素受体是具有不同结构的一类新受体。脂联素受体的这种七次跨膜螺旋在构象上与G蛋白偶联受体的七次跨膜螺旋不同,在这种新的 七次跨膜螺旋中,由三个保守组氨酸残基协同一个锌离子形成了一个大的腔体。这种锌结合结构可能在adiponectin刺激的AMPK磷酸化和UCP2表达上调方面具有一定作用。(Nature, 16 April 2015, doi:10.1038/nature14301 ) 9. Molecular Cell:中国科学家揭示A型流感病毒RNA聚合酶复合体的三维冷冻电镜结构 2015年1月22日,中科院生物物理所刘迎芳研究组与清华大学王宏伟研究组在著名期刊Molecular Cell杂志在线发表了题目为 “Cryo-EM Structure of Influenza Virus RNA Polymerase Complex at 4.3 ? Resolution”的论文,揭示了流感病毒RNA聚合酶复合体的结构和功能。 生物物理所刘迎芳和清华大学王宏伟课题组等中外多方参与的实验室通过使用最新的高分辨率单颗粒冷冻电镜三维重构技术,解析了含有A型流感病毒RNA聚合酶大部分成分的4.3埃分辨率的四聚体电镜结构。该复合体涵盖了流感病毒聚合酶催化活性的核心区域。从三维重构密度图中可以清晰识别出该空腔内PB1上的催化结构域以及结合的RNA复制起始链,据此,研究人员推测这是进行RNA合成反应的区域。这一活性中心结构与正链RNA聚合酶具有相似性,研究人员也因此提出了流感病毒合成新生RNA链的机制。(Molecular Cell, 5 March 2015, doi:10.1016/j.molcel.2014.12.031) 10. Cell:科学家获得首个中介体复合物精确结构图 中介体复合物(Mediator Complex)是细胞中最大也最为复杂的分子机器之一。现在,来自斯克利普斯研究所(TSRI)的科学家们在《细胞》杂志上报告称,他们利用用电镜获得了首个中介体复合物(Mediator)的精确结构图。 Mediator是所有动植物细胞中的关键分子机器,对于绝大多数基因的转录有着至关重要的调控作用。Mediator拥有二十多个蛋白亚基,解析它的结构是基础细胞生物学的一大进步。这一成果能够为许多疾病提供宝贵的线索(从癌症到遗传性的发育疾病)。论文资深作者,TSRI副教授Francisco Asturias表示:"明确这些大分子机器的结构和作用机制,可以帮助我们理解许多关键的细胞过程。" 在这项新研究中,研究人员获得了高纯度的酵母Mediator,并通过电镜成像得到了迄今为止最为清晰的Mediator3D模型,分辨率达到约18埃。随后他们又进行了多种生化分析,例如在逐个去除蛋白亚基的同时观察电镜图像发生的改变。他们由此确定了酵母Mediator25个蛋白亚基的精确定位。 项新研究获得的结构图谱,全面修正了之前的Mediator' 粗略模型。论文第一作者Kuang-LeiTsai表示:"定位了所有的蛋白亚基之后,我们发现头部模块应该位于Mediator的顶部而不是底部。"此外,研究人员还对人类Mediator进行了深入研究。Tsai说:"大体上看,人类和酵母的Mediator总体结构颇为类似。"最后研究人员在结构数据的基础上,为人们展示了Mediator调控转录时的构象变化。(Cell, 29 May 2014, doi: 10.1016/j.cell.2014.05.015)