作者:李寅;陈凤仪;张国添;杨辉;黄玉玲;谢清春;钟鸣; (广州市番禺区中心医院;广东药学院药物研究所;广州汉方现代中药研究开发有限公司;)摘要:目的:测定厄贝沙坦在人血浆中的蛋白结合率。方法:采用HPLC法测定厄贝沙坦的浓度。采用平衡透析法测定厄贝沙坦的人血浆蛋白结合率。结果:以Diamonsil C18(4.6 mm×250 mm,5μm)为色谱柱,以乙腈-0.02 mol/L磷酸二氢钾水溶液(磷酸调pH至2.6)(45∶55)为流动相,检测波长为245 nm,血浆样品中其他成分不干扰厄贝沙坦的测定,厄贝沙坦的线性范围为0.10~10.40μg/ml,定量下限为0.10μg/ml。厄贝沙坦的低、中、高浓度的蛋白结合率分别为93.0%、91.5%、92.3%。结论:厄贝沙坦具有较强的蛋白结合率。谱图:无
药物和蛋白的结合过程是可逆的还是不可逆的呢?
RIP技术(RNA Binding Protein Immunoprecipitation,RNA结合蛋白免疫沉淀),是研究细胞内RNA与蛋白结合情况的技术,是了解转录后调控网络动态过程的有力工具,能帮助我们发现miRNA的调节靶点。RIP这种新兴的技术运用针对目标蛋白的抗体把相应的RNA-蛋白复合物沉淀下来,然后经过分离纯化就可以对结合在复合物上的RNA进行分析。RIP可以看成是普遍使用的染色质免疫沉淀ChIP技术的类似应用,但由于研究对象是RNA-蛋白复合物而不是DNA-蛋白复合物,RIP实验的优化条件与ChIP实验不太相同(如复合物不需要固定,RIP反应体系中的试剂和抗体绝对不能含有RNA酶,抗体需经RIP实验验证等等)。RIP技术下游结合microarray技术被称为RIP-Chip,帮助我们更高通量地了解癌症以及其它疾病整体水平的RNA变化。Millipore基于磁珠的RIP实验流程RIP 实验基本原理:1. 用抗体或表位标记物捕获细胞核内或细胞质中内源性的RNA结合蛋白。2. 防止非特异性的RNA的结合。3. 免疫沉淀把RNA结合蛋白及其结合的RNA一起分离出来。4.结合的RNA序列通过microarray(RIP-Chip),定量RT-PCR或高通量测序(RIP-Seq)方法来鉴定。延伸阅读:95%的人类基因组并不编码基因,而是产生大量的非编码RNA,真正编码蛋白质的基因只占人类总基因组的约2%。这些非编码RNA在生命的生长发育的各个阶段都发挥着重要的调节作用,与艾滋病、白血病、糖尿病、畸形等多种病变密切相关,并且参与着干细胞和表观遗传学调控。而RNA-蛋白复合物驱动了几乎所有细胞过程的基因表达的转录后调控,包括剪接(splicing)、出核转运(nuclear export)、mRNA 稳定性以及蛋白转译过程,因此,对基因调控的了解就有赖于确定这些过程中RNA的结合的变化。因此,RNA研究也被越来越多的科学家重视起来,目前已经成为生命科学研究中一个炙手可热的领域,而RIP技术也逐渐成为RNA研究领域的一项常规方法,帮助我们了解越来越受关注的转录后调控网络。
请问大家,是否可以用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LCMS[/color][/url]来分析一个蛋白和小分子化合物的结合情况?可以知道结合方式么?如果可以,需要哪些已知信息,比如小分子的结构、分子量、大分子蛋白的分子量?谢谢!
纳米材料与结合蛋白的纳米材料,1.在荧光光度分析上会有什么不同[em01] ?2.蛋白的包覆会影响纳米材料的荧光峰吗?3.纳米材料的结合对蛋白的荧光峰会有影响吗?谢谢
我现在在做蛋白和核酸的结合.我的蛋白和核酸可以结合. 蛋白是400多KDa的 核酸很小, 是30bp的dsDNA. 我现在的检测条件下只跑蛋白是可以跑出来的, 当我蛋白和核酸一起跑的时候, 也会在跟只跑蛋白在差不多的位置出峰. (我用的双波长检测,蛋白和核酸分别标记,所以都能看到.)问题就是,一起跑的时候, 出的所有峰, 都是既有蛋白又有核酸, 不管我加的比例是多少.我就很困惑. 如果我加的核酸量很小的话,不是应该有很多游离的蛋白吗,就是说应该有的蛋白峰对应的地方是没有核酸出峰才对的啊, 为什么没有这样的峰呢, 我什么地方理解错了吗?~ 请大家帮忙.谢谢~~~~!BTW, 我用的是bare fused silica capillary, 是CZE, 不是凝胶的 谢谢~~~
美国北卡罗莱纳大学教堂山分校文理学院的首席化学教授约瑟夫—德西蒙博士领导的研究小组发现,人体中的一种正常的良性蛋白质,如果和纳米粒子相结合,就能瞄准并杀死癌细胞,而无须负载那些携带化疗药物的粒子。此前,研究人员曾认为,纳米粒子只有携带了有毒的化学载体才能达到这样的效果。转铁蛋白是人体血液中数量第四多的蛋白质,近20年来一直被作为肿瘤靶向载体用以递送治癌药物。纳米粒子通常也是无毒的,需要通过负载标准化疗药物来治疗癌症。然而,结合转铁蛋白的“打印”纳米粒子,不仅能识别它们,还能诱导癌细胞死亡。而不与任何纳米粒子结合的自由转铁蛋白,能从拉莫斯癌细胞中获得养料生长,即使在很高浓度下也不会杀死任何拉莫斯癌细胞。然而令人吃惊的是,转铁蛋白附着在纳米粒子表面后,其能有效地筛选标靶,攻击并杀死B细胞淋巴瘤。在许多迅速生长的癌细胞表面,蛋白质受体被过度表达,于是和转铁蛋白配体结合的治疗就能找到并瞄准它们,而结合转铁蛋白的纳米粒子被认为是安全且无毒的。德西蒙实验室发明了一种“打印”技术,能人为造出尺寸精确且形状符合预期的纳米颗粒。他们采用这种技术制作出一种可与人类转铁蛋白相结合的生物相容性纳米粒子,其能安全且精确地识别广谱癌症,除了B细胞淋巴瘤外,还能有效地指向非小型细胞,如肺、卵巢、肝脏和前列腺的癌细胞。研究人员目前正在进一步研究,携带转铁蛋白的纳米粒子如何及为何对于拉莫斯癌细胞是有毒的,而对其他细胞却无毒。化学治疗和放射治疗曾被认为是癌症的最有效疗法,但这些疗法通常会损害健康组织和器官。这一发现将可能发展出一种全新的策略来治疗某种类型的淋巴瘤,而副作用更小。不过,德西蒙承认,该研究也会引起一些人对不可预期后果的担忧,即一个设计好的针对某类癌症的靶向化疗载体是否会偏离目标。
转铁蛋白与纳米粒子结合就可瞄准并杀死拉莫斯癌细胞,而无需负载其他化疗药物,此项发现将有望发展出癌症靶向治疗的新策略。 相关研究成果发表在本周的《美国化学协会杂志》上。 美国北卡罗莱纳大学教堂山分校文理学院的首席化学教授约瑟夫德西蒙博士领导的研究小组发现,人体中的一种正常的良性蛋白质,如果和纳米粒子相结合,就能瞄准并杀死癌细胞,而无须负载那些携带化疗药物的粒子。此前,研究人员曾认为,纳米粒子只有携带了有毒的化学载体才能达到这样的效果。 转铁蛋白是人体血液中数量第四多的蛋白质,近20年来一直被作为肿瘤靶向载体用以递送治癌药物。纳米粒子通常也是无毒的,需要通过负载标准化疗药物来治疗癌症。然而,结合转铁蛋白的“打印”纳米粒子,不仅能识别它们,还能诱导癌细胞死亡。而不与任何纳米粒子结合的自由转铁蛋白,能从拉莫斯癌细胞中获得养料生长,即使在很高浓度下也不会杀死任何拉莫斯癌细胞。 然而令人吃惊的是,转铁蛋白附着在纳米粒子表面后,其能有效地筛选标靶,攻击并杀死B细胞淋巴瘤。在许多迅速生长的癌细胞表面,蛋白质受体被过度表达,于是和转铁蛋白配体结合的治疗就能找到并瞄准它们,而结合转铁蛋白的纳米粒子被认为是安全且无毒的。 德西蒙实验室发明了一种“打印”技术,能人为造出尺寸精确且形状符合预期的纳米颗粒。他们采用这种技术制作出一种可与人类转铁蛋白相结合的生物相容性纳米粒子,其能安全且精确地识别广谱癌症,除了B细胞淋巴瘤外,还能有效地指向非小型细胞,如肺、卵巢、肝脏和前列腺的癌细胞。 研究人员目前正在进一步研究,携带转铁蛋白的纳米粒子如何及为何对于拉莫斯癌细胞是有毒的,而对其他细胞却无毒。 化学治疗和放射治疗曾被认为是癌症的最有效疗法,但这些疗法通常会损害健康组织和器官。这一发现将可能发展出一种全新的策略来治疗某种类型的淋巴瘤,而副作用更小。 不过,德西蒙承认,该研究也会引起一些人对不可预期后果的担忧,即一个设计好的针对某类癌症的靶向化疗载体是否会偏离目标。(科技日报)
最近做血浆样品遇到了这样的情况:做方法学的时候,空白血浆添加药物出的峰形很好,与杂质峰的分离度等都很好,所有方法学考察的数据都很好。到做实际样品的时候问题出现了,在进样后1min的时候以及目标峰刚结束的时候出了两个很大的杂峰(不成峰形,就是一大坨),后面那个杂峰干扰目标峰。刚开始以为是进样时间长了导致柱子脏(实际上柱压没变化),就用常规冲洗方法反复冲洗色谱柱,再进样还是这个情况,而且很有规律:每次序列进样前5个样品没问题,从第6个样品开始那两个大杂峰就出现了。百思不得其解,后来查药物手册才知道这个药物与血浆蛋白的结合率达99%。 我的前处理方法是:200uL血浆+2mL正己烷/异丙醇(95:5,V/V)涡旋2min后10000r/min离心10min,取上层40度N2吹干,流动相复溶,12000r/min离心10min,取上清HPLC检测。 尝试过加酸(1mol/L盐酸)或者乙腈等沉淀蛋白方法,杂峰多、干扰严重且回收率低。用我上述方法回收率等方法学数据很好,峰形也很好,就是做实际样品时出现了那样的情况。 想请群里的朋友帮忙想想办法,解决这个问题!谢谢!
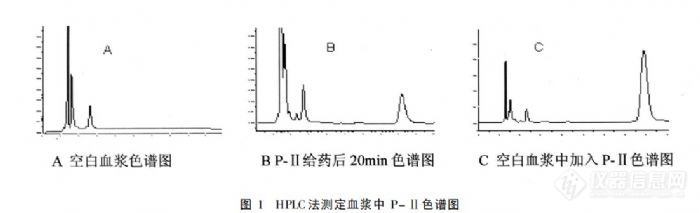
【作者】 阎雪莹; 高宏伟; 唐晓飞; 刁磊; 匡海学;【机构】 黑龙江中医药大学; 黑龙江省哈尔滨市香坊区疾病预防控制中心; 吉林农业科技学院;【摘要】 目的:建立大鼠血浆中胡黄连苦苷Ⅱ的HPLC-UV测定方法,研究在大鼠体内的药代动力学特征,同时测定其血浆蛋白结合率。方法:血浆样品经简单的甲醇沉淀蛋白后,上清液直接进样测定。采用Diamonsil(钻石)C18色谱柱(4.6mm×250mm,5μm)流动相为甲醇-水-醋酸(38:62:0.2),检测波长267nm,流速1mL.min-1,采用3p97药动学软件对药时数据进行拟合。结果:大鼠尾静脉注射胡黄连苦苷Ⅱ符合二室开放模型。结论:胡黄连苦苷Ⅱ在大鼠体内分布代谢很快,消除较快。 更多还原【关键词】 胡黄连苦苷Ⅱ; 药代动力学; 血浆蛋白结合率; 【基金】 国家自然科学基金项目资助(30600804)http://ng1.17img.cn/bbsfiles/images/2012/08/201208071031_382128_2352694_3.jpg
看到这么一句话:酸性药物多与清蛋白结合,为什么呢?
在前处理中,内脏组织大多杂质很多,需要沉淀蛋白质,沉淀后离心,提上清夜再萃取,但内源性物质中的待检物同时也会和蛋白质成结合状态,需要水解,再萃取。所以请问如果我先沉淀了蛋白,那么会不会把成结合状态的待检物一同沉淀,损失待检物。在运用中如何处理蛋白质杂质和蛋白质结合物的前处理问题?
[b][font=宋体]整合蛋白和跨膜蛋白定义:[/font][/b][font=宋体] [/font][font=宋体]整合蛋白和跨膜蛋白是两类重要的蛋白质,它们在细胞分子水平上起着重要的作用。[/font][font=宋体] [/font][font=宋体]整合蛋白,也称为内在蛋白或跨膜蛋白,部分或全部镶嵌在细胞膜中或内外两侧,以非极性氨基酸与脂双分子层的非极性疏水区相互作用而结合在质膜上。它们是生物膜的基本结构成分,许多具重要生理功能的膜蛋白均属整合蛋白,如膜结合的酶类、载体蛋白、通道蛋白、膜受体等。[/font][font=宋体] [/font][font=宋体]跨膜蛋白,是可以跨越细胞膜的蛋白,它在细胞的信号传递系统中担当着重要的角色。跨膜蛋白在结构上可以分为单次跨膜、多次跨膜、多亚基跨膜等,它们具有能够跨越细胞膜的能力。[/font][font=宋体] [/font][b][font=宋体]整合蛋白和跨膜蛋白在位置、结构和功能上存在显著的差异[/font][/b][font=宋体] [/font][font=宋体]①位置:整合蛋白主要存在于细胞质内,细胞核或其他非细胞膜结构中,它们容易在细胞中自由移动。而跨膜蛋白则嵌入细胞膜中,一部分位于细胞膜的胞外侧,另一部分位于细胞膜的胞内侧,形成了一个穿过细胞膜的通道。[/font][font=宋体][font=宋体]②结构:整合蛋白的结构通常由两个独立的部分组成,一个是靠近细胞膜的膜结合区域([/font][font=Calibri]TM[/font][font=宋体]),另一个是靠近细胞骨架的非膜结合区域([/font][font=Calibri]N-TM[/font][font=宋体])。当接受到外界的信号时,整合蛋白的[/font][font=Calibri]TM[/font][font=宋体]区域会被激活,把来自外界的信号转化为细胞内可以识别的信号,直接参与细胞信号传导系统中。[/font][/font][font=宋体]③功能:整合蛋白主要是用来从外界传达信号到细胞内,充当细胞与外界信号的桥梁。而跨膜蛋白则在细胞的信号传递系统中担当着重要的角色。[/font][font=宋体]总的来说,整合蛋白和跨膜蛋白在位置、结构和功能上存在显著的差异,这些差异使得它们在生物体中扮演着不同的角色。[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/resource/protein-review/transmembrane-proteins][b]跨膜蛋白表达与制备服务[/b][/url],制备流程图:基因合成[/font][font=宋体]→载体构建→细胞转化[/font][font=Calibri]/[/font][font=宋体]转染→蛋白表达→细胞收集→细胞破碎→膜脂提取→膜脂增溶→蛋白纯化→质量检测,同时义翘拥有[/font][/font][b][font=宋体]三大跨膜蛋白制备平台[/font][/b][font=宋体],可以为客户提供全面的多次跨膜蛋白产品和服务。同时,为基础研究和药物研发提供更加优质的原材料。[/font][font=宋体] [/font][b][font=宋体][font=Calibri]VLP[/font][font=宋体]技术平台[/font][/font][/b][font=宋体][font=宋体]正确折叠的膜蛋白在细胞膜上表达,类病毒颗粒[/font][font=Calibri]VLP[/font][font=宋体]通过出芽的方式包裹上携带有靶标蛋白的细胞膜,形成包膜的[/font][font=Calibri]VLP[/font][font=宋体]。它是由病毒的衣壳蛋白通过自组装而形成的纳米级颗粒(直径约[/font][font=Calibri]100[/font][font=宋体]~[/font][font=Calibri]300[/font][font=宋体]纳米),不含病毒核酸,不能进行自主复制,生产操作过程中较为安全。产生的[/font][font=Calibri]VLP[/font][font=宋体]蛋白可直接像可溶蛋白一样进行包被进行[/font][font=Calibri]ELISA[/font][font=宋体]检测。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州已成功开发[/font][font=Calibri]VLP[/font][font=宋体]技术平台,它可以将完整天然构象的膜蛋白展示在类病毒颗粒表面,这种方法不仅可以保留膜蛋白的完整结构,同时也能够真实地模拟其在细胞膜上的位置和构象。[/font][/font][font=宋体] [/font][b][font=宋体]去垢剂技术平台[/font][/b][font=宋体][font=宋体]由于存在疏水结构域,跨膜蛋白与膜的结合非常紧密,需要用去垢剂([/font][font=Calibri]detergent[/font][font=宋体])才能从膜上洗涤下来,[/font][font=Calibri]Detergent[/font][font=宋体]作为一种两亲性分子,疏水尾部包裹目的蛋白的疏水区域,亲水头部位于与溶液接触的界面。微团的形成是膜蛋白增溶的基础,当去垢剂浓度高于[/font][font=Calibri]CMC[/font][font=宋体]([/font][font=Calibri]Critical micelle concentration[/font][font=宋体],临界胶束浓度)时会形成微团,增溶后,去垢剂将蛋白周围的磷脂置换,从而实现收集目标膜蛋白的目的,后续再进行蛋白纯化,最终蛋白呈现在含有[/font][font=Calibri]Detergent[/font][font=宋体]的溶液中。义翘神州成功搭建了去垢剂技术平台,利用该平台可有效提高跨膜蛋白的产量和纯度。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]Nanodisc[/font][font=宋体]技术平台[/font][/font][/b][font=宋体][font=Calibri]Nanodisc[/font][font=宋体]结构稳定,与天然的生物膜非常相似,使得[/font][font=Calibri]Nanodisc[/font][font=宋体]能够很好地应用于膜蛋白的研究。目前[/font][font=Calibri]Nanodisc[/font][font=宋体]平台有[/font][font=Calibri]2[/font][font=宋体]种方式,一种是基于苯乙烯马来酸酐共聚物([/font][font=Calibri]SMA[/font][font=宋体])组装的[/font][font=Calibri]SMA-Nanodisc[/font][font=宋体]平台,如下图(左)所示,它可以直接从细胞膜上提取膜蛋白,使其变为可溶性蛋白,组装完成的蛋白样品很稳定,更能维持蛋白的天然构象。另一种是基于膜骨架蛋白([/font][font=Calibri]MSP[/font][font=宋体])的[/font][font=Calibri]MSP-Nanodisc[/font][font=宋体]平台(下图右),它需要先将膜蛋白利用去垢剂制备出来,然后再加入磷脂分子和[/font][font=Calibri]MSP[/font][font=宋体]进行组装。通过调整磷脂、[/font][font=Calibri]MSP[/font][font=宋体]和待组装膜蛋白三者的比例,可以使得待组装膜蛋白在[/font][font=Calibri]Nanodisc[/font][font=宋体]中呈不同聚集状态。义翘神州已成功搭建了[/font][font=Calibri]Nanodisc[/font][font=宋体]技术平台,利用跨膜蛋白与磷脂结合能够维持其良好活性的特性,制备出稳定的产品,满足动物免疫、抗体筛选、[/font][font=Calibri]cell-based assays[/font][font=宋体]等场景。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/transmembrane-proteins[/font][/font]
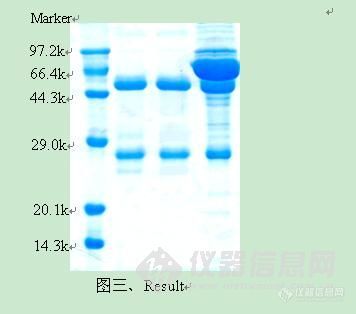
http://simg.instrument.com.cn/bbs/images/brow/em09511.gif一种新型的重组蛋白A柱 洗脱条件温和,充分防止蛋白变性蛋白A是一种金黄色葡萄球菌细胞壁蛋白质,能特异性地与人和哺乳动物抗体(主要是IgG)的Fc区结合。因而,将蛋白A与琼脂糖凝胶以一定的方式结合,可制备用于抗体纯化的亲和填料。早期的蛋白A柱结合的都是天然蛋白A。天然蛋白A由5个IgG结合域和其它未知功能的非Fc结合域组成,分子量约42KD,结构如图一所示。这种柱子对IgG的亲和能力很强,可以吸附大量的lgG。但同时,天然蛋白A的其他非结合域会和非目标蛋白结合,这样被洗脱下来的蛋白质纯度不够,会影响到后续的试验。为了解决这些问题,科学家们运用基因工程技术,克隆出蛋白A的基因,并对其进行改造,除去了一些不重要的非结合域。偶联这种重组蛋白A的琼脂糖凝胶柱在蛋白质纯化中,的确是提高了产物的纯度。目前,市场上绝大部分重组蛋白A柱都是这种产品。但是,纯化时所用的洗脱液一般为pH=2.7的甘氨酸溶液,如果洗脱效果不是很理想,还要降低pH,采用pH=1.9的甘氨酸溶液。由此可见,此法洗脱条件比较剧烈,最后收集的蛋白质很有可能变性,或者是复性困难。 这种洗脱条件剧烈的柱子结合的重组蛋白A一般具有5个串联结构域:E、D、A、B、C。虽然每个域均可以和IgG的Fc段结合,但不同的域结合强度略有差异。因此洗脱条件不均一,而且经常需要较低的pH值。GE的重组蛋白A柱即为这种类型,如图二所示。考虑到减少串联结构域的个数,并且采取同型结构域串联,就可以避免不同结构域与抗体Fc 段亲和性的差异从而使洗脱条件温和而均一,Putus研制出了含有三个串联B结合域的重组蛋白A,如图二所示。同时,我们用Putus重组蛋白A柱和GE重组蛋白A柱纯化人血浆,纯化的结果用于比较两种纯化柱的纯化效果,结果如图三所示。GE Putus 图二、重组蛋白A结构示意图待纯化样品:人血浆实验材料:GE公司的重组蛋白A柱(E、D、A、B、C结构域串联,见图二)Putus公司的重组蛋白A柱(3个B结构域串联,见图二)实验方法:分别按照每个公司的说明书来操作,洗脱条件分别为pH值3.0和4.5, SDS-PAGE检测结果如下: 上图从左边起,泳道1为标准蛋白Marker,泳道2为经过GE填料洗脱后抗体,泳道3为经过Putus填料洗脱抗体,泳道4为人血浆。从图中,我们可以看出,与GE 重组蛋白A填料从人血浆纯化抗体纯度比较,拥有3个同型结构域的Putus填料可以获得同样纯度的抗体。但是,后者的洗脱条件仅为4.5,高于前者的洗脱条件3.0。由此可见,使用具备较少B结构域的重组蛋白A柱也能获得高纯度的IgG,并且洗脱条件温和,能防止蛋白质聚集,保护蛋白质活性。http://cp00a3cee71b5f96adf6e669b5d7f56a9f11.jpg/http://C:\Documents and Settings\adim\桌面\001.jpghttp://ng1.17img.cn/bbsfiles/images/2017/01/201701191653_632703_1672347_3.jpghttp://ng1.17img.cn/bbsfiles/images/2009/12/200912021052_187444_1672347_3.jpghttp://ng1.17img.cn/bbsfiles/images/2009/12/200912021052_187445_1672347_3.jpg
北京易斯威特生物医学科技有限公司产品介绍 铁蛋白(FER)检测试剂盒 (胶体金法)1.国内第一家免疫层析法检测FER的产品。2.本产品应用世界上最先进的单克隆抗体技术结合胶体金(纳米金)免疫层析技术,以双抗体夹心法快速定性检测人血清,血浆中的铁蛋白,适用于急性贫血,肝脏损伤等相关疾病的辅助诊断3.最快速准确的辅助诊断方法。4.血清铁蛋白是血液去铁蛋白和铁核心Fe3+形成的复合物。是检查体内铁缺乏的最灵敏的指标。血清铁蛋白测定在临床上常用于缺铁性贫血的诊断。简单 便捷 快速 灵敏 环保 肌红蛋白/肌酸激酶/心肌肌钙蛋白I,心梗三项检测试剂盒(胶体金法)1.本产品应用世界上最先进的单克隆抗体技术结合胶体金(纳米金)免疫层析技术,以双抗体夹心法快速定性检测人血清,血浆中的肌红蛋白,肌酸激酶,心肌肌钙蛋白I检测,用于临床快速诊断急性心肌梗塞(AMI).2.最快速准确的辅助诊断方法。3.肌红蛋白:是心肌梗死的标志物,增高表示冠状动脉堵塞引起心肌严重缺血造成心肌梗死;4.肌钙蛋白:是一种心肌蛋白,升高见于心肌损伤,多见于心肌梗死,也见于心肌炎和心肺复苏后患者,特异性较高,阳性的话一般可确诊心肌损伤,阴性的话不能排除,因为肌钙蛋白的升高出现在心肌梗塞3-6小时之后,之前可能出现阴性。肌酸激酶敏感性较高,特异性较低,升高也出现在心梗3-8小时之后。5.肌酸激酶:主要存在于骨骼肌和心肌,在脑组织中也存在,是参与体内的能量代谢的一种酶。在临床上主要用于诊断心肌梗塞。心肌梗塞患者发病后2-4小时,血液中此酶活动即开始升高。比血清中谷草转酸酶和乳酸脱氢酶的活力变化都出现得早。 简单 便捷 快速 灵敏 环保 C反应蛋白(CRP)检测试剂盒(胶体金法)1.国内第一家免疫层析法检测CRP的产品。2.本产品应用世界上最先进的单克隆抗体技术结合胶体金(纳米金)免疫层析技术,以双抗体夹心法快速定性检测人血清,血浆中的C反应蛋白,适用于感染,炎性疾病,组织损伤,手术创伤及组织坏死等病变情况的辅助诊断3.最快速准确的辅助诊断方法。4.是一种能与肺炎球菌C多糖体反应形成复合物的急性时相反应蛋白。可用于细菌和病毒感染的鉴别诊断简单 便捷 快速 灵敏 环保

[img=,500,95]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021007141220_851_981_3.jpg!w690x132.jpg[/img]1 普通共聚焦(左半部分)和STED超分辨(右半部分)检测DNA蛋白互作效果对比。(5nM TFAM 647N,恒力4pN)[b]STED 超分辨[/b]单分子水平定量分析DNA与蛋白的相互作用要求技术水平达到在复杂的生物微环境中保证超高的时间分辨率。这种体内复杂的生物学反应尤其常见于在体外模拟体内实验,比如高浓度的蛋白与不断变化的DNA相互作用。采用受激发射损耗显微技术(STED)能够实现快速对复杂的DNA进行高分辨的扫描。LUMICKS公司研发的SuperC-Trap™ 技术结合STED,能够实现高分辨率可视化的研究多蛋白结合的DNA反应动力学。Figure 1 显示实时观测荧光标记的高浓度(大约 5nM)TFAM转录因子与λ-DNA的相互作用。SuperC-Trap™ 采用光镊技术原位拉直DNA,然后结合STED技术高分辨率(≥50 nm)高频率(≤200 Hz)线性追踪TASM的动态变化。STED 能够实现对单个结合或非结合、寡聚化蛋白基团的实时追踪(Figure 1, 右半部份)。然而利用共聚焦显微镜却分辨不出来 (Figure 1,左半部分)。共聚焦的点状激发原理决定了其只能追踪分布密度比较高的蛋白分子的动态变化,却不能进行广角扫描。而且采用共聚焦技术位置比较相近的两种蛋白也很难被分辨。但是利用STED的受激发射损耗技术可突破衍射极限,可以轻易分辨两种相邻蛋白。[img=,500,111]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021023463820_3909_981_3.png!w690x154.jpg[/img]2 光镊技术(红色部分)结合共聚焦技术(绿色部分)模式图,多激发模式。[img=,500,103]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021024169794_3597_981_3.png!w690x143.jpg[/img]3 光镊技术(红色部分)结合STED超分辨技术(黄色部分)模式图,单激发模式。[img=,500,198]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021025123269_5345_981_3.png!w535x212.jpg[/img]4 共聚焦 (左) 和超分辨率显微镜STED (右)分辨率对比。647N-标记的结合DNA的限制性内切酶。5 共聚焦(蓝色)和超分辨率显微镜STED(红色)对两个相邻蛋白的分辨率对比。[b]SuperC-Trap[/b]共聚焦显微镜和超分辨显微镜的区别很明显。从Figure 4中可以看出超分辨显微镜能够清晰的将两种相邻蛋白分辨出来,而共聚焦的分辨率并不能达到。这种对比明显的说明了超分辨在精确定位上的优势。LUMICKS公司的SuperC-Trap不仅能够实现实时超分辨可视化的观察,而且还可以在亚pN水平、亚nm分辨率监测分子间的相互作用。结合我们的超稳定液流系统和独立的整合软件,使得整个实验在数分钟之内就能完成。
想用ICP-MS检测一蛋白质结合的金属离子,不知道蛋白要怎么处理,直接消解掉上样吗?
尿微量蛋白(尿微量白蛋白/蛋白尿)试验(也称“白蛋白试验”,“尿微量白蛋白”和“蛋白尿”试验)何为尿微量白蛋白(白蛋白)试验?尿微量白蛋白试验是对尿液中的蛋白质进行测定的筛选试验。人体血液中有一种蛋白质称为白蛋白。在正常情况下,几乎无法在尿液中检测到。只有在肾脏受损,尤其是损伤早期,它可以优先于其他肾损伤标志物在尿液中被检测出,因此,尿微量白蛋白在诊断肾脏疾病、早期肾损伤等方面具有重要意义。此项试验有何目的?蛋白质是人体的基本构成“材料”,具备一些重要的功能和作用,可结合营养物质将其运输至各个组织,,并将人体中循环的体液量维持在适当水平。肾脏功能正常时,蛋白质几乎无法通过肾脏进入尿液(仅会排出血液循环产生的废料)。然而,如果人的肾功能受损或衰竭,该肾脏对蛋白质的过滤能力将有所下降,因而一些蛋白质将会透过肾脏而出现在尿液中,称为尿微量蛋白。尿微量白蛋白与蛋白尿有何不同?白蛋白是一种大量存在于血液中的典型蛋白质。因其分子个头小,当肾脏功能出现问题时,白蛋白是能够率先通过肾脏进入尿液的几种蛋白质之一。尿液中出现少量白蛋白的情况称为尿微量白蛋白。若肾脏功能受损严重,尿液中的白蛋白数量呈现出增长趋势,这种症状被改称为蛋白尿。尿微量白蛋白/蛋白尿有何症状?病症早期,并无明显症状或征兆显现。随着肾功能衰竭的加重,大量蛋白质出现在尿液中,手脚、腹部和面部可能出现肿胀。如果蛋白尿的情况加重,可能会造成永久性肾功能损伤,有些病人可能需要做透析或肾移植。不论上述症状是否存在,尿蛋白测定是确定有多少蛋白质进入尿液的唯一办法。蛋白尿还可能引发心血管疾病。血管受损除了会引发肾脏疾病外,还可能会造成窒息和心力衰竭。患蛋白尿(症)的高危人群有哪些?患有糖尿病、高血压、心血管疾病和其他类型肾脏疾病等慢性病的病人易出现蛋白尿。老年人、肥胖人群以及有肾脏疾病家族史的人群。其
[b][font=宋体]什么是膜蛋白?[/font][/b][font=宋体]膜蛋白是一类广泛存在于生物体细胞膜上的蛋白质分子。它们在维持细胞结构完整性、调控物质运输和信号传导等方面起着重要作用。根据蛋白分离的难易及在膜中分布的位置,膜蛋白基本可分为三大类:外在膜蛋白或称外周膜蛋白、内在膜蛋白或称整合膜蛋白和脂锚定蛋白。膜蛋白包括糖蛋白,载体蛋白和酶等。[/font][font=宋体] [/font][font=宋体][font=宋体]通常在膜蛋白外会连接着一些糖类,这些糖相当于会通过糖本身分子结构变化将信号传到细胞内。研究膜蛋白结构的技术包括[/font][font=Calibri]X[/font][font=宋体]射线衍射等,常用于重组膜蛋白的表达系统有真核表达系统。[/font][/font][font=宋体] [/font][b][font=宋体]膜蛋白的类型:[/font][/b][font=宋体]目前存在不同类型的膜蛋白,例如:[/font][font=宋体]①整合膜蛋白[/font][font=宋体]②外周膜蛋白[/font][font=宋体]③脂质结合蛋白[/font][font=宋体]④两性蛋白[/font][font=宋体] [/font][b][font=宋体]膜蛋白的特点:[/font][/b][font=宋体][font=宋体]膜蛋白有多种形状和大小,执行多种任务,但它们总是依赖于一些关键特征。[/font] [font=宋体]膜蛋白的一些区别特征如下。[/font][/font][font=宋体]①跨膜域: 跨膜结构域是延伸到脂质双层全长的蛋白质片段。 疏水性氨基酸残基是这些结构域的共同特征,它们介导与膜磷脂疏水性尾部的相互作用。[/font][font=宋体]②疏水和亲水区域: 膜蛋白包含疏水和亲水结构域,使它们能够与脂质双层和两侧的水环境进行交流。[/font][font=宋体]③选择性:膜蛋白的一个共同特征是它们能够调节某些分子或离子的通过。 通常是蛋白质的独特结构和电荷决定了它的选择性。[/font][font=宋体]④受体位点: 当膜蛋白上的受体区域与各自的目标分子或离子结合时,这些区域就会被激活。 大多数时候, 分子 或由受体检测到的离子在受体上具有与该位点结构或化学相容的结合位点。[/font][font=宋体]⑤构象变化: 当膜蛋白结合特定分子或离子时,它通常会发生构象变化,从而引发生物反应或允许蛋白质将结合的分子转运穿过膜。[/font][font=宋体]⑥锚固:多种机制,包括与其他蛋白质的相互作用和与膜中脂质分子的结合,可用于将膜蛋白锚定到细胞膜。[/font][font=宋体]⑦糖基化:碳水化合物链通过称为糖基化的过程与几种膜蛋白结合。 这种改变可以作为防止蛋白水解的保护措施,并作为细胞中下游蛋白质的信号。[/font][font=宋体][font=宋体]跨膜结构域、疏水和亲水区域、选择性、受体位点、构象变化、锚定和糖基化都是膜蛋白的特性,对它们在细胞膜中的功能至关重要。[/font] [font=宋体]由于这些特性,膜中的蛋白质能够运输分子、发送信号、提供结构支持和催化反应。[/font][/font][font=宋体] [/font][b][font=宋体]膜蛋白的功能:[/font][/b][font=宋体]①运输功能[/font][font=宋体]膜转运蛋白分为载体蛋白和通道蛋白两种。主动运输和协助扩散都需要载体蛋白。水分子进去细胞时需要水通道蛋白,还有一种离子通道蛋白,需要注意的是通过通道蛋白进出细胞因为不需要能量所以属于协助扩散。[/font][font=宋体] [/font][font=宋体]②识别功能[/font][font=宋体] [/font][font=宋体]两个不相邻细胞间信息交流是通过信号分子(如激素、神经递质、淋巴因子等)来完成的,而细胞膜上能与信息分子结合的便是细胞膜上的特异性受体。[/font][font=宋体] [/font][font=宋体][font=宋体]细胞与细胞之间可以通过相互接触而相互识别,例如精子与卵细胞的相互识别,效应[/font][font=Calibri]T[/font][font=宋体]细胞与靶细胞之间的相互识别就是依靠糖蛋白来完成的[/font][/font][font=宋体] [/font][font=宋体]③催化功能[/font][font=宋体] [/font][font=宋体][font=宋体]膜蛋白可能是某些反应所需要的酶。例如[/font][font=Calibri]Na+-K+[/font][font=宋体]泵中存在[/font][font=Calibri]ATP[/font][font=宋体]水解酶;光反应、有氧呼吸之所以在膜上发生的原因之一就是膜上存在反应所需的相关酶。[/font][/font][font=宋体] [/font][font=宋体]④抗原功能[/font][font=宋体] [/font][font=宋体][font=宋体]表面抗原能和特异的抗体结合,如人细胞表面有一种蛋白质抗原[/font][font=Calibri]HLA[/font][font=宋体],是一种变化极多的二聚体。不同的人有不同的[/font][font=Calibri]HLA[/font][font=宋体]分子,器官移植时,被植入的器官常常被排斥,这就是因为植入细胞的[/font][font=Calibri]HLA[/font][font=宋体]分子不为受体所接受之故。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/resource/protein-review/transmembrane-proteins][b]跨膜蛋白制备[/b][/url]平台及跨膜蛋白详解:详情可查看:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/transmembrane-proteins[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
蛋白多肽多肽:多肽是α-氨基酸以肽键连接在一起而形成的化合物,是蛋白质水解的中间产物。由两个氨基酸分子脱水缩合而成的化合物叫做二肽,同理类推还有三肽、四肽、五肽等。通常由10~100氨基酸分子脱水缩合而成的化合物叫多肽,它们的分子量低于10,000Da(Dalton,道尔顿),能透过半透膜,不被三氯乙酸及硫酸铵所沉淀。也有文献把由2~10个氨基酸组成的肽称为寡肽(小分子肽);10~50个氨基酸组成的肽称为多肽;由50个以上的氨基酸组成的肽就称为蛋白质。蛋白质:生物体中广泛存在的一类生物大分子,由核酸编码的α氨基酸之间通过α氨基和α羧基形成的肽键连接而成的肽链,经翻译后加工而生成的具有特定立体结构的、有活性的大分子。是α—氨基酸按一定顺序结合形成一条多肽链,再由一条或一条以上的多肽链按照其特定方式结合合而成的高分子化合物。蛋白偶联KLH/BSA/Ovalbumin etc 偶联小肽/半抗原必须耦合到载体蛋白(KLH,BSA,Ova),才可以获得高效的抗体。一般来说,多肽可以与蛋白偶联的条件如下:1 有一个自由的氨基或羧基2 半胱氨酸上的-SH也可以与载体蛋白偶联目前我公司提供高质量的偶联载体蛋白(KLH,BSA,OVA)[img=,690,300]https://ng1.17img.cn/bbsfiles/images/2019/02/201902191022256586_4193_3531468_3.jpg!w690x300.jpg[/img]我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。请移步百度搜“[b]合肥国肽生物[/b]”即可
[font=宋体][font=宋体]抗体融合蛋白([/font][font=Calibri]Ig[/font][font=宋体]融合蛋白)是指在基因水平上将目的基因同免疫球蛋白部分片段基因相连,并在真核或原核表达系统中表达的重组蛋白。抗体融合蛋白具有抗体的特性及融合功能蛋白的活性,可广泛应用于免疫诊断、免疫治疗、抗体纯化及抗体和抗原的定量分析等,特别可用于免疫导向药物的制备。根据结合的[/font][font=Calibri]Ig[/font][font=宋体]片段的不同,可以将抗体融合蛋白分为[/font][font=Calibri]Fab[/font][font=宋体]融合蛋白、[/font][font=Calibri]Fc[/font][font=宋体]融合蛋白与单链抗体([/font][font=Calibri]scFv[/font][font=宋体])融合蛋白。[/font][/font][font=宋体] [/font][font=宋体][b]抗体融合蛋白结构:[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]Fab[/font][font=宋体]融合蛋白、单链抗体融合蛋白研究表明,抗体可变区的[/font][font=Calibri]N[/font][font=宋体]端空间结构上与互补决定区([/font][font=Calibri]CDR[/font][font=宋体])形成的抗原结合部位十分接近,有的抗体可变区[/font][font=Calibri]N[/font][font=宋体]端残基甚至直接参与抗原结合部位的形成,如果将效应蛋白与抗体片段的[/font][font=Calibri]N[/font][font=宋体]端结合,可能对抗体可变区的空间构型造成较大影响,从而降低抗体与抗原的结合能力。因此,通常将蛋白与抗体片段的[/font][font=Calibri]C[/font][font=宋体]端进行结合,形成抗体融合蛋白。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]Fc[/font][font=宋体]融合蛋白[/font][/font][/b][font=宋体] [/font][font=宋体][font=Calibri]Fc[/font][font=宋体]融合蛋白在结构上是将抗体的[/font][font=Calibri]Fc[/font][font=宋体]区与功能蛋白进行融合,可将[/font][font=Calibri]Fc[/font][font=宋体]的[/font][font=Calibri]N[/font][font=宋体]端或[/font][font=Calibri]C[/font][font=宋体]端与目的基因进行融合。根据结合蛋白的不同,可以有多种构型。[/font][/font][font=宋体] [/font][font=宋体][b]抗体融合蛋白作用原理:[/b][/font][font=宋体] [/font][font=宋体]含有抗体可变区的抗体融合蛋白[/font][font=宋体] [/font][font=宋体][font=Calibri]Fab[/font][font=宋体]融合蛋白与[/font][font=Calibri]scFv[/font][font=宋体]融合蛋白含有抗体的可变区,可以进行抗原[/font][font=Calibri]-[/font][font=宋体]抗体反应,其作用原理为利用抗体[/font][font=Calibri]-[/font][font=宋体]抗原特异性结合的特性,通过这种特性的引导,将具有生物活性的蛋白靶向引导至细胞的特定部位,进而发挥一定的生物效应。[/font][/font][font=宋体] [/font][font=宋体]不含抗体可变区的抗体融合蛋白[/font][font=宋体] [/font][font=宋体][font=宋体]该类融合蛋白含有的抗体功能区为[/font][font=Calibri]Fc[/font][font=宋体]区,不能进行抗原[/font][font=Calibri]-[/font][font=宋体]抗体反应,[/font][font=Calibri]Fc[/font][font=宋体]段的作用为延长药物在血浆内的半衰期、增加融合蛋白的稳定性等。[/font][font=Calibri]Fc[/font][font=宋体]融合蛋白药理作用的发挥依赖于功能蛋白部分,利用受体[/font][font=Calibri]-[/font][font=宋体]配体之间的相互作用产生一系列的生物学效应。[/font][/font][font=宋体] [/font][font=宋体][b]抗体融合蛋白制备:[/b][/font][font=宋体] [/font][font=宋体]最初抗体融合蛋白制备的方法为化学交联法,但这种方法制备的抗体融合蛋白组成不均一、性能不稳定、免疫源性大,随着基因工程技术的发展,该技术已被淘汰。目前主要利用基因工程技术来进行抗体融合蛋白的制备。[/font][font=宋体] [/font][font=宋体][font=宋体]其制备原理为:将抗体基因与目的蛋白基因通过一段接头序列([/font][font=Calibri]linker[/font][font=宋体])进行链接,然后将链接产物亚克隆至载体中,并用原核或者真核表达系统进行表达。制备抗体融合蛋白过程中,一个关键的问题是两蛋白间的接头序列[/font][font=Calibri](Linker)[/font][font=宋体]的长度,[/font][font=Calibri]linker[/font][font=宋体]的长短对蛋白质的折叠和稳定性非常重要。如果接头序列太短,可能影响两蛋白高级[/font][font=Calibri]-[/font][font=宋体]结构的折叠,从而相互干扰;如果接头序列太长,又涉及免疫原性的问题。抗体融合蛋白与双特异性抗体抗体融合蛋白是将抗体的部分片段与目的蛋白进行融合表达得到的重组蛋白,若将两个具有不同抗原特异性的抗体片段连接至同一蛋白,即可得到双特异性抗体。[/font][/font][font=宋体] [/font][font=宋体][b]单克隆抗体与抗体融合蛋白区别:[/b][/font][font=宋体] [/font][font=宋体]单克隆抗体抗体[/font][font=宋体] [/font][font=宋体][font=宋体]结构:[/font][font=Calibri]Y[/font][font=宋体]型[/font][/font][font=宋体][font=宋体]制备方法:杂交瘤技术[/font][font=Calibri]/[/font][font=宋体]基因重组[/font][/font][font=宋体][font=宋体]表达系统:真核系统[/font][font=Calibri]/[/font][font=宋体]原核系统[/font][/font][font=宋体][font=宋体]真核系统[/font][font=Calibri]/[/font][font=宋体]原核系统[/font][/font][font=宋体][font=宋体]作用原理:特异性识别抗原,[/font][font=Calibri]Fc[/font][font=宋体]段引起[/font][font=Calibri]ADCC[/font][font=宋体]、[/font][font=Calibri]ADCP[/font][font=宋体]、[/font][font=Calibri]CDC[/font][font=宋体]等作用。[/font][/font][font=宋体] [/font][font=宋体]抗体融合蛋白[/font][font=宋体] [/font][font=宋体]结构:具有多种结构[/font][font=宋体]制备方法:基因重组[/font][font=宋体][font=宋体]表达系统:真核系统[/font][font=Calibri]/[/font][font=宋体]原核系统[/font][/font][font=宋体][font=宋体]作用原理:功能蛋白与靶分子间的受体[/font][font=Calibri]-[/font][font=宋体]配体的相互作用[/font][/font][font=宋体] [/font][font=宋体][font=宋体]详情可以参考:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/fusion-protein[/font][/font][font=Calibri] [/font]
[font=宋体]抗体,作为一类特殊的蛋白质,在免疫系统中发挥着至关重要的作用,它们能够特异性地识别并中和外来病原体,如细菌和病毒。而蛋白质,作为生命活动的基础分子,具有多种多样的功能,从酶催化到结构支撑,无所不包。抗体与蛋白的区别在于,抗体是一类具有特定功能的蛋白质,而蛋白质则是更广泛的一类生物分子。本文将深入探讨抗体与蛋白的具体区别,并详细解析抗体蛋白的结构与功能,为读者提供一个全面而深入的理解。[/font][font=宋体] [/font][b][font=宋体]抗体与蛋白的区别?[/font][/b][font=宋体] [/font][font=宋体]定义:[/font][font=宋体][font=宋体]抗体([/font][font=Calibri]antibody[/font][font=宋体])是指机体由于抗原的刺激而产生的具有保护作用的蛋白质。它(免疫球蛋白不仅仅只是抗体)是一种由浆细胞(效应[/font][font=Calibri]B[/font][font=宋体]细胞)分泌,被免疫系统用来鉴别与中和外来物质如细菌、病毒等的大型[/font][font=Calibri]Y[/font][font=宋体]形蛋白质,仅被发现存在于脊椎动物的血液等体液中,及其[/font][font=Calibri]B[/font][font=宋体]细胞的细胞膜表面。抗体能识别特定外来物的一个独特特征,该外来目标被称为抗原。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]抗体是一类能与抗原特异性结合的免疫球蛋白。抗体按其反应形式分为凝集素、沉降素、抗毒素、溶解素、调理素、中和抗体、补体结合抗体等。按抗体产生的来源分为正常抗体(天然抗体),如血型[/font][font=Calibri]ABO[/font][font=宋体]型中的抗[/font][font=Calibri]A[/font][font=宋体]和抗[/font][font=Calibri]B[/font][font=宋体]的抗体,和免疫抗体如抗微生物的抗体。按反应抗原的来源分为异种抗体,异嗜性抗体,同种抗体和自身抗体。按抗原反应的凝集状态分为完全抗体[/font][font=Calibri]IgM[/font][font=宋体]和不完全抗体[/font][font=Calibri]IgG[/font][font=宋体]等。抗体在医疗实践中应用甚为广泛。如用于疾病的预防、诊断和治疗方面都有一定的作用。临床上用丙种球蛋白预防病毒性肝炎、麻疹、风疹等,国际上用抗[/font][font=Calibri]Rh[/font][font=宋体]免疫球蛋白预防因[/font][font=Calibri]Rh[/font][font=宋体]血型不合引起的溶血症。诊断上如类风湿因子用于类风湿性关节炎,抗核抗体([/font][font=Calibri]ANA[/font][font=宋体])、抗[/font][font=Calibri]DNA[/font][font=宋体]抗体用于系统性红斑狼疮,抗精子抗体用于原发性不孕症的诊断等;治疗上如毒素中毒用抗毒治疗以及免疫缺陷性疾病的治疗等。[url=https://cn.sinobiological.com/resource/antibody-technical][b]抗体相关资源[/b][/url][/font][/font][font=宋体] [/font][font=宋体]蛋白:[/font][font=宋体][font=宋体]蛋白质是生命的物质基础,是有机大分子,是构成细胞的基本有机物,是生命活动的主要承担者。没有蛋白质就没有生命。氨基酸是蛋白质的基本组成单位。它是与生命及与各种形式的生命活动紧密联系在一起的物质。机体中的每一个细胞和所有重要组成部分都有蛋白质参与。蛋白质占人体重量的[/font][font=Calibri]16%~20%[/font][font=宋体],即一个[/font][font=Calibri]60kg[/font][font=宋体]重的成年人其体内约有蛋白质[/font][font=Calibri]9.6~12kg[/font][font=宋体]。人体内蛋白质的种类很多,性质、功能各异,但都是由[/font][font=Calibri]20[/font][font=宋体]多种氨基酸([/font][font=Calibri]Amino acid[/font][font=宋体])按不同比例组合而成的,并在体内不断进行代谢与更新。点击查看:[url=https://cn.sinobiological.com/resource/protein-review][b]蛋白相关资源[/b][/url][/font][/font][font=宋体] [/font][b][font=宋体]区别与联系:[/font][/b][font=宋体][font=宋体]蛋白质还是有一定的区别以及关联性的,虽然说抗体是蛋白质,但是蛋白质不一定是抗体。[/font] [font=宋体]主要是因为抗体是通过人体内的浆细胞所产生的,而且还可以喝相应的抗原特异性相互结合,这样在一定程度上就能发挥出蛋白质。[/font][/font][font=宋体] [/font][b][font=宋体]抗体[/font][font=宋体]蛋白[/font][font=宋体]结构[/font][font=宋体]解析[/font][font=宋体]:[/font][/b][font=宋体][font=宋体]抗体是一种免疫球蛋白,由[/font][font=Calibri]B[/font][font=宋体]淋巴细胞产生。抗体的单体是一个[/font][font=Calibri]Y[/font][font=宋体]形的分子,有[/font][font=Calibri]4[/font][font=宋体]条多肽链组成。其中包括两条相同的重链,以及两条相同的轻链,之间由双硫键连接在一起。每条重链[/font][font=Calibri]50kDa[/font][font=宋体],每条轻链[/font][font=Calibri]25kDa[/font][font=宋体],轻重链间存在二硫键链接。[/font][/font][font=宋体] [/font][font=宋体]轻链[/font][font=宋体][font=宋体]轻链包括可变区和恒定区,可变区约占轻链的[/font][font=Calibri]1/2[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体]重链[/font][font=宋体][font=宋体]重链包括可变区和恒定区。根据重链的不同,可以将抗体分为不同的种类,例如哺乳动物[/font] [font=Calibri]Ig [/font][font=宋体]的重链有α、δ、ε、γ和 μ 五种[/font][font=Calibri],[/font][font=宋体]相对应可以将哺乳动物[/font][font=Calibri]Ig[/font][font=宋体]分为 [/font][font=Calibri]IgA[/font][font=宋体]、[/font][font=Calibri]IgD[/font][font=宋体]、[/font][font=Calibri]IgE[/font][font=宋体]、[/font][font=Calibri]IgG [/font][font=宋体]和 [/font][font=Calibri]IgM [/font][font=宋体]五类。[/font][/font][font=宋体] [/font][font=宋体]可变区[/font][font=宋体][font=宋体]抗体分子的[/font][font=Calibri]N[/font][font=宋体]端存在一段氨基酸序列变化较大的区域,该区域称为可变区。可变区中存在可以与抗原特结合的部位,即抗原结合位点。一个抗体有两个抗原结合位点,可以同时结合两个抗原分子。在可变区中有三个区域的序列高度变化,成为高变区([/font][font=Calibri]hypervariable region[/font][font=宋体],[/font][font=Calibri]HVR[/font][font=宋体])又称为抗原互补决定区([/font][font=Calibri]complementarity determining region[/font][font=宋体],[/font][font=Calibri]CDR[/font][font=宋体])。可变区主要通过其[/font][font=Calibri]3[/font][font=宋体]个[/font][font=Calibri]CHR[/font][font=宋体]区形成[/font][font=Calibri]3[/font][font=宋体]个环状结构与抗原特异性结合。可变区中非[/font][font=Calibri]CDR[/font][font=宋体]部分成为骨架区([/font][font=Calibri]framework region[/font][font=宋体],[/font][font=Calibri]FR[/font][font=宋体]),其氨基酸组成和排列变化相对[/font][font=Calibri]CDR[/font][font=宋体]较少。[/font][/font][font=宋体] [/font][font=宋体]恒定区[/font][font=宋体][font=宋体]抗体分子[/font][font=Calibri]C[/font][font=宋体]端氨基酸序列相对稳定,该区域称为恒定区。同一种抗体的恒定区是相同的。抗体轻链的恒定区由一个[/font][font=Calibri]Ig[/font][font=宋体]结构域构成;重链的恒定区由[/font][font=Calibri]3-4[/font][font=宋体]个串联的[/font][font=Calibri]Ig[/font][font=宋体]结构域及一个用于增加灵活性的铰链区构成。[/font][font=Calibri]IgA[/font][font=宋体]、[/font][font=Calibri]IgE[/font][font=宋体]、[/font][font=Calibri]IgG[/font][font=宋体]有三个结构域([/font][font=Calibri]CH1[/font][font=宋体]、[/font][font=Calibri]CH2[/font][font=宋体]、[/font][font=Calibri]CH3[/font][font=宋体]),[/font][font=Calibri]IgD[/font][font=宋体]、[/font][font=Calibri]IgM[/font][font=宋体]有四个结构域([/font][font=Calibri]CH1[/font][font=宋体]、[/font][font=Calibri]CH2[/font][font=宋体]、[/font][font=Calibri]CH3[/font][font=宋体]、[/font][font=Calibri]CH4[/font][font=宋体])。不同种类抗体的铰链区存在一定的差异,[/font][font=Calibri]IgA[/font][font=宋体]的铰链区较短,[/font][font=Calibri]IgD [/font][font=宋体]的铰链区较长,[/font][font=Calibri]IgM [/font][font=宋体]和[/font][font=Calibri]IgE [/font][font=宋体]无铰链区。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Fab[/font][font=宋体]片段[/font][/font][font=宋体][font=Calibri]IgG[/font][font=宋体]分子在木瓜蛋白酶的作用下可以被降解为两个[/font][font=Calibri]Fab[/font][font=宋体]段及一个[/font][font=Calibri]Fc[/font][font=宋体]段。[/font][font=Calibri]Fab[/font][font=宋体]段由抗体轻链的可变区、轻链的恒定区、重链的可变区及重链恒定区构成。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Fc[/font][font=宋体]段[/font][/font][font=宋体][font=Calibri]Fc[/font][font=宋体]段包含了所有抗体分子共有的蛋白质序列以及各个类别独有的决定簇。[/font][font=Calibri]Fc[/font][font=宋体]段有多种生物学活性,具有结合补体、结合[/font][font=Calibri]Fc[/font][font=宋体]受体、通过胎盘等作用。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多关于[url=https://cn.sinobiological.com/resource/antibody-technical/antibody-structure-function][b]抗体的结构和功能[/b][/url]详情:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/antibody-structure-function[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
我是做蛋白结构解析的。蛋白与配体具有强亲和性结合,那么每个氨基酸化学位移的变化是否能用化学位移滴定法跟踪,为何?这个问题困扰我的实验,求解……谢谢帮助!
实验目的:提取海参中的金属结合蛋白我看很多文献做鱼肝脏什么的都是先用制作成丙酮粉,或用其他方法脱色脱脂,我想问一下,不脱色脱色对提取蛋白结果影响大吗?
[font=宋体] [font=宋体]重组蛋白纯化要利用不同蛋白间内在的相似性与差异,利用各种蛋白间的相似性来除去非蛋白物质的污染,而利用各蛋白质的差异将目的蛋白从其他蛋白中纯化出来。每种蛋白间的大小、形状、电荷、疏水性、溶解度和生物学活性都会有差异,利用这些差异可将蛋白从混合物如大肠杆菌裂解物中提取出来得到重组蛋白。[/font][/font][font=宋体] [font=宋体][b]重组蛋白纯化常用的几个方法如下:[/b][/font][/font][font=宋体] [font=Calibri]1.[/font][font=宋体]蛋白纯化色谱法:[/font][/font][font=宋体] [font=宋体]色谱法无疑是下游处理中主要和常用的操作,因为色谱法相比其他单元操作具有某些优势。例如色谱法支持高分辨率的效率,可以分离分子性质非常相似的复杂粗制混合物。此外,色谱法是生物工艺中遇到的稀释溶液中捕获分子的理想选择。[/font][/font][font=宋体] [font=宋体]柱色谱法[/font][font=Calibri]([/font][font=宋体]层析法[/font][font=Calibri])[/font][font=宋体]的原理是将一个大的蛋白池分离成许多小的蛋白池,其中一些富集了目标蛋白。虽然柱色谱法有昂贵的专业设备,但只需要基本的设备就可以了。[/font][/font][font=宋体] [font=Calibri]2.[/font][font=宋体]亲和色谱法:[/font][/font][font=宋体] [font=宋体]亲和色谱法依赖于蛋白对基质结合配体的特异性和可逆性结合。该配体可以直接与目的蛋白结合或共价连接到蛋白的标签上与其相结合。亲和层析通常是最有效的纯化方法,通常用在纯化方案的早期阶段。这种特定的亲和相互作用能够捕获目标物,同时去除溶液中的污染物或其他分子,并一步富集或纯化目标分子,使其与其他不能结合配体的分子分离。[/font][/font][font=宋体] [font=宋体]除了理论上蛋白能够通过免疫亲和色谱纯化之外,亲和法仅限于具有特异结合特性的蛋白,而免疫亲和色谱是所有亲和技术中特异性最高的。[/font][/font][font=宋体] [font=Calibri]3.[/font][font=宋体]离子交换色谱法:[/font][/font][font=宋体] [font=宋体]离子交换色谱[/font][font=Calibri](IEX)[/font][font=宋体]是一种主要基于蛋白净电荷的色谱分离方法,通常用于追踪脱酰胺和琥珀酰亚胺的形成。[/font][font=Calibri]IEX[/font][font=宋体]有两种类型:阳离子交换和阴离子交换色谱法。当缓冲液[/font][font=Calibri]pH[/font][font=宋体]值高于此[/font][font=Calibri]IP[/font][font=宋体]时,蛋白带负电(阴离子);当[/font][font=Calibri]pH[/font][font=宋体]值低于此[/font][font=Calibri]IP[/font][font=宋体]时,蛋白带正电(阳离子)。[/font][/font][font=宋体] [font=宋体]所有蛋白都表现出净电荷,这取决于蛋白氨基酸组成和任何共价连接的修饰。蛋白净电荷受溶解它的溶剂[/font][font=Calibri]pH[/font][font=宋体]所影响,因为溶剂会与蛋白进行氢离子交换。通常情况下,蛋白与[/font][font=Calibri]IEX[/font][font=宋体]的结合必须通过反复试验来确定,使用一系列[/font][font=Calibri]pH[/font][font=宋体]值的溶剂以确定蛋白保留的最佳[/font][font=Calibri]pH[/font][font=宋体]。通常溶剂的[/font][font=Calibri]pH[/font][font=宋体]值与[/font][font=Calibri]pI[/font][font=宋体]相差约一个[/font][font=Calibri]pH[/font][font=宋体]单位就足以实现蛋白结合。[/font][/font][font=宋体] [font=Calibri]4.HPLC[/font][font=宋体]法蛋白纯化:[/font][/font][font=宋体] [font=宋体]色谱法是一种常用分析技术,可以将混合物分离成单独的成分。高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法通常称为[/font][font=Calibri]HPLC[/font][font=宋体],在化学生物学研究实验室中广泛应用。[/font][/font][font=宋体] [font=宋体]在化学生物学中,单个分析物(如多肽)通常经色谱纯化后作为一种功能工具使用。高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法[/font][font=Calibri](HPLC)[/font][font=宋体]是一种用于分析和分离液体样品的方法。在化学生物学实验室中,[/font][font=Calibri]HPLC[/font][font=宋体]是纯化多肽(人工合成或用合成器自动合成)和其他中小型有机分子不可或缺的过程。它还允许使用颗粒非常小的柱填料,这就给固定相和流经它的分子之间产生相互作用提供了更大的表面积,这样可以更好地分离混合物的成分。[/font][/font][font=宋体][font=宋体]针对特定应用开发的[/font][font=Calibri]HPLC[/font][font=宋体]色谱柱有很多种类,如正相[/font][font=Calibri]HPLC(NP-HPLC)[/font][font=宋体]和反相[/font][font=Calibri]HPLC(RP-HPLC)[/font][font=宋体]。正确选择色谱柱是获得良好的[/font][font=Calibri]HPLC[/font][font=宋体]结果的关键。色谱柱的选择取决于我们希望分离的混合物的组分特性。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供从基因合成、载体构建到蛋白质表达、纯化的一站式服务,可以根据客户需求,选用不同表达[/font][font=Calibri]/[/font][font=宋体]纯化标签、表达宿主等,真正为客户实现深度私人定制。多种纯化体系,为蛋白表达、纯化提供多种选择,我们致力于为客户提供高质量、低成本的重组蛋白。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多[url=https://cn.sinobiological.com/services/recombinant-protein-expression-service][b]重组蛋白表达纯化服务[/b][/url]详情尽在:[/font][font=Calibri]https://cn.sinobiological.com/services/recombinant-protein-expression-service[/font][/font]
[font=宋体]跨膜蛋白是生物体内广泛存在的一类蛋白质,它们在细胞膜上以不同的方式与其相互作用,从而发挥各种生物学功能。根据不同的结构和功能,[/font][b][font=宋体]跨膜蛋白可以分为三种类型:通道型跨膜蛋白、受体型跨膜蛋白和泵型跨膜蛋白。[/font][/b][font=宋体] [/font][font=宋体][font=宋体]通道型跨膜蛋白是跨膜蛋白中最为简单的类型,它们主要的功能是在细胞膜上形成一些具有选择性通透性的孔道,使得离子和小分子物质能够通过。通道型跨膜蛋白具有多个跨膜域,通常由[/font] [font=宋体]α 螺旋和 β 折叠两种二级结构组成。α 螺旋通道如 [/font][font=Calibri]K+ [/font][font=宋体]通道能够容纳阳离子,β 折叠如离子泵[/font][font=Calibri]Na+/K+-ATPase [/font][font=宋体]能够承载各种离子。[/font][/font][font=宋体] [/font][font=宋体]受体型跨膜蛋白是一类比较复杂的蛋白质,它们能够接受信号分子的结合,从而调节细胞内的生物学路径。受体型跨膜蛋白通常由单个跨膜域和两个不同构的端基组成,其中一个端基是细胞外的受体结构域,能够特异性地与信号分子结合;另外一个端基是细胞内的调节结构域,能够将受体活性传递到细胞内部。受体型跨膜蛋白具有多种作用方式,如酪氨酸激酶受体,转录因子受体等。[/font][font=宋体] [/font][font=宋体][font=宋体]泵型跨膜蛋白是一类能够通过能量输入来驱动物质运输的蛋白质。它们能够将离子或者小分子物质从低浓度区域转运到高浓度区域,从而维持细胞内的化学平衡和稳态。泵型跨膜蛋白一般由多个跨膜域组成,并能借助外源性能量如[/font][font=Calibri]ATP[/font][font=宋体]进行运输。常见的泵型跨膜蛋白有[/font][font=Calibri]Na+/K+-ATPase, H+/K+-ATPase[/font][font=宋体]等。[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州提供跨膜蛋白制备平台,包括:[/font][font=Calibri]VLP[/font][font=宋体]技术平台[/font][font=Calibri]/[/font][font=宋体]去垢剂技术平台[/font][font=Calibri]/Nanodisc[/font][font=宋体]技术平台。[/font][/font][font=宋体][font=Calibri]VLP[/font][font=宋体]技术平台[/font][/font][/b][font=宋体][font=宋体]正确折叠的膜蛋白在细胞膜上表达,类病毒颗粒[/font][font=Calibri]VLP[/font][font=宋体]通过出芽的方式包裹上携带有靶标蛋白的细胞膜,形成包膜的[/font][font=Calibri]VLP[/font][font=宋体]。它是由病毒的衣壳蛋白通过自组装而形成的纳米级颗粒(直径约[/font][font=Calibri]100[/font][font=宋体]~[/font][font=Calibri]300[/font][font=宋体]纳米),不含病毒核酸,不能进行自主复制,生产操作过程中较为安全。产生的[/font][font=Calibri]VLP[/font][font=宋体]蛋白可直接像可溶蛋白一样进行包被进行[/font][font=Calibri]ELISA[/font][font=宋体]检测。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州已成功开发[/font][font=Calibri]VLP[/font][font=宋体]技术平台,它可以将完整天然构象的膜蛋白展示在类病毒颗粒表面,这种方法不仅可以保留膜蛋白的完整结构,同时也能够真实地模拟其在细胞膜上的位置和构象。[/font][/font][font=宋体][font=宋体]利用[/font][font=Calibri]VLP[/font][font=宋体]平台制备跨膜蛋白具有以下优势:[/font][/font][font=宋体]? 全长跨膜蛋白,保持完整的天然构象[/font][font=宋体][font=宋体]? 适用于动物免疫、[/font][font=Calibri]ELISA[/font][font=宋体]检测、[/font][font=Calibri]CAR[/font][font=宋体]阳性率检测、抗体筛选等。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州搭建了基于[/font][font=Calibri]HEK293[/font][font=宋体]表达系统的[/font][font=Calibri]VLP[/font][font=宋体]([/font][font=Calibri]virus-like particle[/font][font=宋体])技术平台,能够将目的膜蛋白完整展示在[/font][font=Calibri]VLP[/font][font=宋体]表面,使其能够像普通蛋白一样进行检测,义翘神州目前可以为客户提供膜蛋白定制服务,助力药物研发进程。[/font][/font][font=宋体] [/font][b][font=宋体]去垢剂技术平台[/font][/b][font=宋体][font=宋体]由于存在疏水结构域,跨膜蛋白与膜的结合非常紧密,需要用去垢剂([/font][font=Calibri]detergent[/font][font=宋体])才能从膜上洗涤下来,[/font][font=Calibri]Detergent[/font][font=宋体]作为一种两亲性分子,疏水尾部包裹目的蛋白的疏水区域,亲水头部位于与溶液接触的界面。微团的形成是膜蛋白增溶的基础,当去垢剂浓度高于[/font][font=Calibri]CMC[/font][font=宋体]([/font][font=Calibri]Critical micelle concentration[/font][font=宋体],临界胶束浓度)时会形成微团,增溶后,去垢剂将蛋白周围的磷脂置换,从而实现收集目标膜蛋白的目的,后续再进行蛋白纯化,最终蛋白呈现在含有[/font][font=Calibri]Detergent[/font][font=宋体]的溶液中。义翘神州成功搭建了去垢剂技术平台,利用该平台可有效提高跨膜蛋白的产量和纯度。[/font][/font][font=宋体]去垢剂技术平台的优势:[/font][font=宋体]? 可精确定量[/font][font=宋体]? 胶束为膜蛋白疏水基团提供保护并稳定构象[/font][font=宋体][font=宋体]? 适用于动物免疫、[/font][font=Calibri]ELISA[/font][font=宋体]检测、[/font][font=Calibri]SPR/BLI[/font][font=宋体]检测等[/font][/font][b][font=宋体] [/font][font=宋体][font=Calibri]Nanodisc[/font][font=宋体]技术平台[/font][/font][/b][font=宋体][font=Calibri]Nanodisc[/font][font=宋体]结构稳定,与天然的生物膜非常相似,使得[/font][font=Calibri]Nanodisc[/font][font=宋体]能够很好地应用于膜蛋白的研究。目前[/font][font=Calibri]Nanodisc[/font][font=宋体]平台有[/font][font=Calibri]2[/font][font=宋体]种方式,一种是基于苯乙烯马来酸酐共聚物([/font][font=Calibri]SMA[/font][font=宋体])组装的[/font][font=Calibri]SMA-Nanodisc[/font][font=宋体]平台,如下图(左)所示,它可以直接从细胞膜上提取膜蛋白,使其变为可溶性蛋白,组装完成的蛋白样品很稳定,更能维持蛋白的天然构象。另一种是基于膜骨架蛋白([/font][font=Calibri]MSP[/font][font=宋体])的[/font][font=Calibri]MSP-Nanodisc[/font][font=宋体]平台(下图右),它需要先将膜蛋白利用去垢剂制备出来,然后再加入磷脂分子和[/font][font=Calibri]MSP[/font][font=宋体]进行组装。通过调整磷脂、[/font][font=Calibri]MSP[/font][font=宋体]和待组装膜蛋白三者的比例,可以使得待组装膜蛋白在[/font][font=Calibri]Nanodisc[/font][font=宋体]中呈不同聚集状态。义翘神州已成功搭建了[/font][font=Calibri]Nanodisc[/font][font=宋体]技术平台,利用跨膜蛋白与磷脂结合能够维持其良好活性的特性,制备出稳定的产品,满足动物免疫、抗体筛选、[/font][font=Calibri]cell-based assays[/font][font=宋体]等场景。[/font][/font][font=宋体][font=Calibri]SMA-Nanodisc[/font][font=宋体]技术平台的优势:[/font][/font][font=宋体]? 可精确定量[/font][font=宋体][font=宋体]? [/font][font=Calibri]SMA[/font][font=宋体]共聚物包裹的膜蛋白稳定性更好,有助于更好地研究膜蛋白的结构和功能[/font][/font][font=宋体][font=宋体]? 适用于动物免疫、[/font][font=Calibri]ELISA[/font][font=宋体]检测、[/font][font=Calibri]SPR/BLI[/font][font=宋体]检测、[/font][font=Calibri]CAR[/font][font=宋体]阳性率检测及细胞实验等[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多[url=https://cn.sinobiological.com/resource/protein-review/transmembrane-proteins][b]跨膜蛋白[/b][/url]详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/transmembrane-proteins[/font][/font][font=Calibri] [/font]
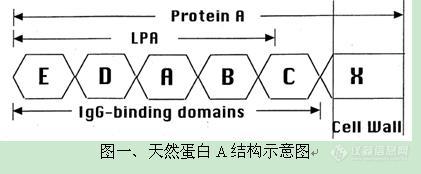
[em09511]一种新型的重组蛋白A柱 洗脱条件温和,充分防止蛋白变性蛋白A是一种金黄色葡萄球菌细胞壁蛋白质,能特异性地与人和哺乳动物抗体(主要是IgG)的Fc区结合。因而,将蛋白A与琼脂糖凝胶以一定的方式结合,可制备用于抗体纯化的亲和填料。早期的蛋白A柱结合的都是天然蛋白A。天然蛋白A由5个IgG结合域和其它未知功能的非Fc结合域组成,分子量约42KD,结构如图一所示。这种柱子对IgG的亲和能力很强,可以吸附大量的lgG。但同时,天然蛋白A的其他非结合域会和非目标蛋白结合,这样被洗脱下来的蛋白质纯度不够,会影响到后续的试验。为了解决这些问题,科学家们运用基因工程技术,克隆出蛋白A的基因,并对其进行改造,除去了一些不重要的非结合域。偶联这种重组蛋白A的琼脂糖凝胶柱在蛋白质纯化中,的确是提高了产物的纯度。目前,市场上绝大部分重组蛋白A柱都是这种产品。但是,纯化时所用的洗脱液一般为pH=2.7的甘氨酸溶液,如果洗脱效果不是很理想,还要降低pH,采用pH=1.9的甘氨酸溶液。由此可见,此法洗脱条件比较剧烈,最后收集的蛋白质很有可能变性,或者是复性困难。 这种洗脱条件剧烈的柱子结合的重组蛋白A一般具有5个串联结构域:E、D、A、B、C。虽然每个域均可以和IgG的Fc段结合,但不同的域结合强度略有差异。因此洗脱条件不均一,而且经常需要较低的pH值。GE的重组蛋白A柱即为这种类型,如图二所示。考虑到减少串联结构域的个数,并且采取同型结构域串联,就可以避免不同结构域与抗体Fc 段亲和性的差异从而使洗脱条件温和而均一,Putus研制出了含有三个串联B结合域的重组蛋白A,如图二所示。同时,我们用Putus重组蛋白A柱和GE重组蛋白A柱纯化人血浆,纯化的结果用于比较两种纯化柱的纯化效果,结果如图三所示。GE Putus 图二、重组蛋白A结构示意图待纯化样品:人血浆实验材料:GE公司的重组蛋白A柱(E、D、A、B、C结构域串联,见图二)Putus公司的重组蛋白A柱(3个B结构域串联,见图二)实验方法:分别按照每个公司的说明书来操作,洗脱条件分别为pH值3.0和4.5, SDS-PAGE检测结果如下: 上图从左边起,泳道1为标准蛋白Marker,泳道2为经过GE填料洗脱后抗体,泳道3为经过Putus填料洗脱抗体,泳道4为人血浆。从图中,我们可以看出,与GE 重组蛋白A填料从人血浆纯化抗体纯度比较,拥有3个同型结构域的Putus填料可以获得同样纯度的抗体。但是,后者的洗脱条件仅为4.5,高于前者的洗脱条件3.0。由此可见,使用具备较少B结构域的重组蛋白A柱也能获得高纯度的IgG,并且洗脱条件温和,能防止蛋白质聚集,保护蛋白质活性。[IMG]http://CP00A3CEE71B5F96ADF6E669B5D7F56A9F11.jpg[/IMG][URL=http://C:\Documents and Settings\adim\桌面\001.jpg]http://C:\Documents and Settings\adim\桌面\001.jpg[/URL][img]http://ng1.17img.cn/bbsfiles/images/2009/12/200912021052_187443_1672347_3.jpg[/img][img]http://ng1.17img.cn/bbsfiles/images/2009/12/200912021052_187444_1672347_3.jpg[/img][img]http://ng1.17img.cn/bbsfiles/images/2009/12/200912021052_187445_1672347_3.jpg[/img]
1、C反应蛋白概述 1930年Tillet和Francis在急性大叶性肺炎患者血清中发现一种物质,能在钙离子存在时与肺炎球菌C-多糖起沉淀反应,随后证实这种能与C-多糖反应的物质是一种蛋白质,因而将这种蛋白质命名为C反应蛋白(C-reactive protein,CRP)。 CRP是机体受到微生物入侵或组织损伤等炎症性刺激时肝细胞合成的急性相蛋白(注:急性时相反应包括感染、炎症及创伤时某些血清蛋白浓度的变化,这些蛋白除CRP外,还包括血清淀粉样蛋白A、纤维蛋白原、触珠蛋白、α1酸性糖蛋白、铜蓝蛋白、α1抗胰蛋白酶等。其中CRP在健康人血清中浓度<5mg/L,而在细菌感染或组织损伤时,浓度可升高上千倍,循环中的CRP半衰期为19小时,故被认为其最有价值),由五个相同的亚基依靠非共价键形成的环状五聚体,这一特征性结构使其归类于五聚素(一组具有免疫防御特性的钙结合蛋白)家族。CRP是机体非特异性免疫机制的一部分,它结合C-多糖,在Ca2+存在时可结合细胞膜上磷酸胆碱,可激活补体的经典途径,增强白细胞的吞噬作用,调节淋巴细胞或单核/巨噬系统功能,促进巨噬细胞组织因子的生成,在动脉粥样硬化斑块中也可检测到CRP。 人CRP主要生物学功能: 通过与配体(凋亡与坏死的细胞,或入侵的细菌、真菌、寄生虫等的磷酰胆碱)结合,激活补体和单核吞噬细胞系统,将载有配体的病理物质或病原体清除。 (1)识别外来物质,激活补体系统; (2)增强条理作用,增强吞噬细胞吞噬作用; (3)与血小板激活因子(RAF)结合,降低炎症反应; (4)与染色体结合,消除坏死组织里的细胞DNA。
[font=宋体][font=宋体]膜联蛋白([/font][font=Calibri]Annexin[/font][font=宋体])是一类分布广泛的钙依赖性磷脂结合蛋白,与磷脂酰丝氨酸([/font][font=Calibri]PS[/font][font=宋体])能特异性结合,参与一系列[/font][font=Calibri]Ca2+[/font][font=宋体]依赖型的膜相关的过程,包括细胞的胞吐和内吞作用、囊泡运输、调节血液凝固以及炎症反应等多种生物学事件,在许多人类疾病的发病机制或进展中起着非常重要的作用。膜联蛋白[/font][font=Calibri]V[/font][font=宋体]([/font][font=Calibri]Annexin V[/font][font=宋体])染色是检测细胞凋亡的常用方法。[/font][/font][b][font=宋体][font=宋体]膜联蛋白[/font][font=Calibri]V[/font][font=宋体]染色原理及应用[/font][/font][/b][font=宋体] [/font][b][font=宋体][font=宋体]一、膜联蛋白[/font][font=Calibri]V[/font][font=宋体]染色原理[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]膜联蛋白[/font][font=Calibri]V[/font][font=宋体]染色,也称为[/font][font=Calibri]Annexin V[/font][font=宋体]染色,是一种用于检测细胞凋亡的方法。其核心原理基于细胞凋亡过程中的一种生物化学变化。在正常细胞中,磷脂酰丝氨酸([/font][font=Calibri]PS[/font][font=宋体])只分布在细胞膜脂质双层的内侧。然而,当细胞开始凋亡时,这一分布会发生改变,磷脂酰丝氨酸会从细胞膜内侧翻到外侧。膜联蛋白[/font][font=Calibri]V[/font][font=宋体]是一种能够与这种外翻的磷脂酰丝氨酸特异性结合的蛋白。通过结合荧光物质,这种结合可以被检测和观察,从而确定哪些细胞正在经历凋亡。[/font][/font][b][font=宋体] [/font][font=宋体][font=宋体]二、膜联蛋白[/font][font=Calibri]V[/font][font=宋体]染色的应用[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]①流式细胞术:膜联蛋白[/font][font=Calibri]V[/font][font=宋体]染色常用于流式细胞术中,以检测和分类正常细胞和凋亡细胞。通过流式细胞仪,可以快速分析大量细胞,并准确地识别出凋亡细胞。[/font][/font][font=宋体][font=宋体]②光学显微镜成像:膜联蛋白[/font][font=Calibri]V[/font][font=宋体]染色也可用于光学显微镜成像技术,这使得研究者能够在显微镜下直接观察细胞的形态变化,从而对凋亡过程有更深入的理解。[/font][/font][font=宋体][font=宋体]③与其他染色方法的结合:膜联蛋白[/font][font=Calibri]V[/font][font=宋体]染色可以与其他染色方法如碘化丙啶[/font][font=Calibri](PI)[/font][font=宋体]染色结合使用。[/font][font=Calibri]PI[/font][font=宋体]是一种能够进入凋亡晚期细胞核的染料,因此可以用于区分凋亡早期和晚期细胞。这种联合使用的方法能提供更全面的细胞凋亡信息。[/font][/font][font=宋体][font=宋体]④临床应用:膜联蛋白[/font][font=Calibri]V[/font][font=宋体]染色在许多临床领域中都有应用,例如肿瘤学、血液学和药理学等。它可以帮助研究者深入理解疾病的发展过程,评估新药物对细胞凋亡的影响,以及监测疾病的进展和治疗的效果。[/font][/font][font=宋体][font=宋体]总的来说,膜联蛋白[/font][font=Calibri]V[/font][font=宋体]染色是一种强大的工具,可以帮助科学家们更好地理解细胞凋亡的过程,从而为疾病的治疗和药物研发提供有价值的信息。[/font][/font][font=宋体] [/font][font=宋体]更多关于膜联蛋白详情可以关注[url=https://cn.sinobiological.com/][b]义翘神州[/b][/url]![/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
[font=宋体]蛋白质是包括人类在内的各种生物有机体的重要组成成分,是生命的物质基础之一。生物体的生长、发育、遗传和繁殖等一切生命活动都离不开蛋白质。[/font][font=宋体] [/font][font=宋体]随着分子生物学、结构生物学、基因组学等研究的不断深入,人们意识到仅仅依靠基因组的序列分析来试图阐明生命活动的现象和本质是远远不够的。只有从蛋白质组学的角度对所有蛋白质的总和进行研究,才能更科学地掌握生命现象和活动规律,更完善地揭示生命的本质。[/font][font=宋体] [/font][font=宋体]由此许多学者将生命科学领域的研究焦点从基因转向蛋白质,使蛋白质成为揭示生命活动现象和分子生物学机理的重要研究对象。研究蛋白质首要的步骤是将目的蛋白从复杂的大分子混合物中分离纯化出来,得到高纯度具有生物学活性的目的物。因此,高效的纯化技术和手段是蛋白质研究的重要基础和关键之一。[/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体][font=宋体]蛋白纯化的目的[/font] [/font][/b][font=宋体][font=宋体]蛋白纯化的目的是将目标蛋白质从细胞裂解液的全部组分中分离出来,同时仍保留蛋白的生物学活性及化学完整性。蛋白质的分离和提纯工作是一项艰巨而繁重的任务,需根据蛋白的特性选择合适的纯化方法来提高获得的蛋白制品的纯度。[/font] [/font][font=宋体] [/font][b][font=宋体][font=宋体]蛋白纯化的原理[/font] [/font][/b][font=宋体][font=宋体]不同蛋白质的氨基酸序列及空间结构不同,导致其在物理、化学、生物学等性质上存在差异,利用待分离蛋白质与其它蛋白质性质上的差异,即可以设计出一套合理的蛋白纯化方案。蛋白的纯化大致分为粗分离阶段和精细纯化阶段两个阶段。粗分离阶段主要将目的蛋白和其他细胞成分如[/font] [font=Calibri]RNA[/font][font=宋体]、[/font][font=Calibri]DNA [/font][font=宋体]等分开,常用的方法为硫酸铵沉淀法。精细纯化阶段的目的是把目的蛋白与其他大小及理化性质接近的蛋白区分开来,[/font][/font][b][font=宋体][font=宋体]常用的方法有:凝胶过滤层析、离子交换层析、疏水层析、亲和层析等。[/font] [/font][/b][font=宋体] [/font][b][font=宋体]①[/font][font=宋体]凝胶过滤层析[/font][/b][font=宋体]凝胶过滤层析(又叫做分子筛)是根据样品的分子大小对样品进行分离的一种简单温和的层析技术。凝胶过滤层析也称分子筛层析、排阻层析,是利用具有网状结构的凝胶的分子筛作用,根据被分离物质的分子大小不同来进行分离。不同于离子交换层析和亲和层析,凝胶过滤的层析样品不与层析柱料结合,因此,缓冲液成分不直接影响分辨率。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]原理:层析柱中的填料是球状颗粒的惰性的多孔网状结构的柱料,多是交联的聚糖[/font][font=Calibri]([/font][font=宋体]如葡聚糖或琼脂糖[/font][font=Calibri])[/font][font=宋体]类物质。在加入样品之后,样品中的小分子物质能进入球状填料内部,在柱子中停留时间较长;而大分子物质不能进入球状填料内部,停留时间较短。所以当样品经过凝胶过滤层析柱分离后,样品中的不同分子大小的物质就可以被分离开了。[/font][/font][font=宋体] [/font][font=宋体]特点:[/font][font=宋体] [/font][font=宋体]根据分子大小和形状进行分离[/font][font=宋体] [/font][font=宋体]是一种非吸附的分离方式[/font][font=宋体] [/font][font=宋体]缓冲液成分不直接影响分辨率,只需要一种缓冲液[/font][font=宋体] [/font][font=宋体]操作便捷[/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体]②[/font][font=宋体]离子交换层析[/font][/b][font=宋体]离子交换层析是目前蛋白质分离纯化中应用最广泛的方法之一。[/font][font=宋体] [/font][font=宋体]原理:不同蛋白等电点差异,分子大小差异,在同一个流动相中电荷密度分布不同,电荷量不等,与具有相反电荷的离子交换介质结合强度不同,在流动相洗脱时保留时间不同,从而得以分离。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体]特点:[/font][font=宋体] [/font][font=宋体]根据分子大小和等电点差异进行分离[/font][font=宋体] [/font][font=宋体]灵敏度高,重复性,选择性好,分析速度快[/font][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体]③[/font][font=宋体]疏水层析[/font][/b][font=宋体]原理:疏水层析是依据蛋白质疏水性差异分离的。即根据蛋白质和疏水介质表面的疏水基团的可逆相互作用进行分离。蛋白的疏水性在高离子强度下被增强,因此在高离子强度环境中结合,通常采用降低离子强度的方式进行洗脱。独特的吸附分离模式使得疏水层析成为硫酸铵盐析后或离子交换高盐洗脱后理想的纯化方式。[/font][font=宋体] [/font][font=宋体]特点:[/font][font=宋体] [/font][font=宋体]采用了盐的水溶液作为流动相,色谱条件温和,生物大分子的活性回收率很高。[/font][font=宋体] [/font][font=宋体][font=宋体]蛋白质在[/font][font=Calibri]HIC[/font][font=宋体]操作过程中是高盐上样,低盐洗脱(高盐浓度的样品不必作处理就可直接上样)。[/font][/font][font=宋体] [/font][font=宋体]在一次色谱中可同时实现出去盐酸胍、蛋白质复性和分离三个目的。[/font][font=宋体] [/font][font=宋体][font=宋体]温度升高,蛋白质天然折叠伸展,暴露出更多内部疏水集团,使蛋白质的[/font][font=Calibri]HIC[/font][font=宋体]保留发生变化。[/font][/font][font=宋体] [/font][font=宋体]色谱填料稳定性好,盐水体系作流动相无环境污染。[/font][font=宋体] [/font][b][font=宋体]④[/font][font=宋体]亲和层析[/font][/b][font=宋体][font=宋体]原理:[url=https://cn.sinobiological.com/resource/protein-review/protein-purification-by-ac][b]亲和层析[/b][/url]是应用生物高分子与配基可逆结合的原理,将配基通过共价键牢固结合于载体上而制得的层析系统。这种可逆结合的作用主要是靠生物高分子对它的配基的空间结构的识别。常用的生物亲和关系有酶[/font][font=Calibri]-[/font][font=宋体]底物、底物类似物、抑制剂、激活剂、辅因子,抗体[/font][font=Calibri]-[/font][font=宋体]抗原,激素[/font][font=Calibri]-[/font][font=宋体]受体蛋白、载体蛋白,外源凝集素[/font][font=Calibri]-[/font][font=宋体]多糖、糖蛋白、细胞表面受体,核酸[/font][font=Calibri]-[/font][font=宋体]互补核苷酸序列、组蛋白、核酸结合蛋白等,具有高效、简单、快速的优点,是当前最为理想的分离纯化蛋白的方法。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多详情可以参看蛋白纯化技术[/font][font=Calibri]/[/font][font=宋体]方法:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-purification-techniques[/font][/font][font=Calibri] [/font]