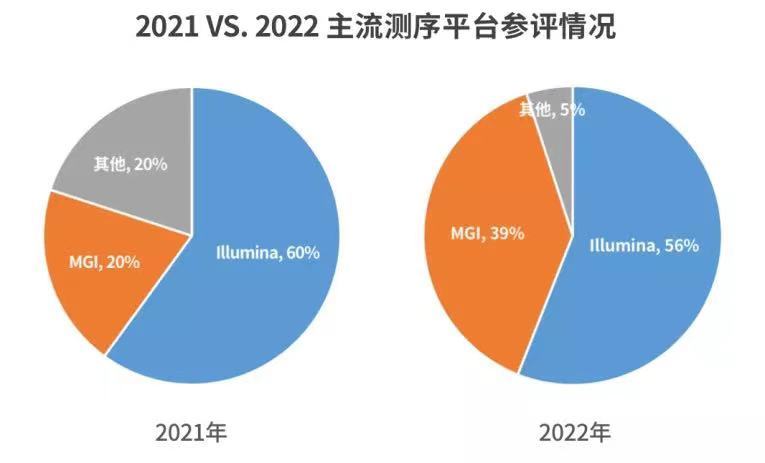
高分辨质谱平台实现mRNA mapping流程化
在之前的一篇微信稿中,咱们介绍了mRNA疫苗的质谱表征方法,“Orbitrap 高分辨质谱助力mRNA疫苗表征”,今天小编继续为大家详细拓展mRNA mapping的质谱表征应用。作为一种新的药物形式,mRNA在多个疾病领域具有显着的治疗潜力。进入细胞后,mRNA药物使用内源性细胞机制来表达预编程的蛋白质。这种表达的蛋白质可以实现多种目的,从促进特定的免疫反应到调节或恢复各种代谢过程等[1]。据WHO官网统计,全球目前正在临床试验阶段的mRNA药物已有几十种,应用方向覆盖传染性疾病、罕见病、肿瘤免疫学等。与大多数生物治疗药物一样,序列分析也是mRNA药物的一个关键质量属性(CQA)。经典的检测方法如Sanger测序和二代测序 (NGS)等已被用于核酸链高通量及大规模的测序。然而在生物制品的表征分析中,往往需要正交方法以获取更全面的信息。对于核酸分析,LC-MS 作为Sanger和NGS的正交方法,与传统测序技术相比具有独特的优势:可直接对核酸样品进行分析(无需扩增等处理步骤);更高的检测灵敏度(直接检测低水平的序列变异体或修饰杂质(由于核酸样品与蛋白样品的较大差异,其测序流程的前处理及LC/MS方法也大不相同。核酸仅有4个特定碱基,在组合形式上远小于蛋白序列,因此会有多个重复序列片段,需要酶解成较长的片段(通常大于15nt)以得到可用于序列覆盖的特征片段。此外核酸样品极不稳定,非常容易降解。基于此需求,我们在前处理上需要选择特异性较强的酶,并且减少酶解时间,得到具有漏切位点的较长片段。下图显示了优化后的核酸mapping分析流程,从前处理到液相分离、质谱检测、数据分析的一套完整方案。点击查看大图 No.01# 前 处 理Nuclease T1是一种真菌核酸内切酶,可切割鸟嘌呤残基后的单链RNA,具有较强的特异性,常用于核酸测序应用。但由于核酸内切酶效率很高,酶解时间较难控制,且传统的溶液酶解方法会使核酸酶残留在分析柱上造成污染。基于以上需求,赛默飞推出了一款前处理磁珠RNase T1 Mag Bulk Kit,将Nuclease T1酶固定在磁珠上,通过简单快速的磁铁吸附及可有效控制酶解时间,并去除溶液里的T1酶,该方式可以有效提高实验的重现性并降低酶的干扰(如下图)。有离线及在线两种方式可供选择:a) 将样品配成200 μL体积放于eppendorf管中(如下图a所示),置于酶解仪中震荡孵育(37-50℃, 2000 rmp)5min ,通过磁铁吸附的方式将酶解上清与磁珠分离,再加入1%甲酸终止反应;图a:手动前处理示意图(点击查看大图)b) 采用全自动磁珠纯化仪,反应、分离及纯化均可根据设置好的程序进行自动操作,适用于高通量前处理需求(图b)。图b: 全自动化在线前处理示意图(点击查看大图)反应条件的优化:a. 反应时间:酶解时间控制在5min 内,随着反应时间的增加(30min, 1h, 4h, overnight),序列覆盖度明显降低。对于修饰mRNA(如甲基化修饰),需要增加反应时间至30min.b. 反应温度:37℃与50℃的结果类似No.02# 色 谱 柱色谱分离采用一款专用于核酸分析的色谱柱,Thermo Scientific™ DNAPac™ RP,该色谱柱由球形宽孔径 4 µm 聚合树脂构成,可耐受极端 pH (0-14) 和温度 (5-110°C) 条件,在HPLC 和UHPLC仪器上均可使用,针对寡核苷酸可实现高分辨率和高通量,较小和极大的核酸链均可分辨(如下图A)。图A(点击查看大图)图B显示DNAPac™ RP色谱柱的各类型号,mRNA mapping建议选用2.1*100 mm型号。图B(点击查看大图)