重量法蒸汽吸附仪 产品简介重量法动态蒸汽吸附仪DVS系列在测量水和有机蒸汽在粉体表面吸附方面处于世界领先地位,它通过在一定相对湿度下气体通过样品后重量的变化来测定蒸汽吸附,比传统的干燥法测量更快,更节省时间。由于其独特的优势,DVS系列产品世界各地的实验室有广泛的应用,可用于研发部门以及质控部门确定产品结构、产品稳定性、吸湿性、包装和产品开发中固体材料存在的问题。结合了微天平、气体流动和蒸汽的测量技术的优势使用干燥的载气,通常为氮气,可以选择任何两个蒸汽源中的一个质量流量控制和独特的水和有机蒸汽浓度实时监控结合可以精确控制饱和干燥载气流量的比例整个体系的温度可以由选择,并且在闭合环条件下可以精确控制,以保证吸附质的蒸汽压恒定具有极其高的灵敏度和精确度,仅需少量的样品(通常1-30mg),因而可快速达到平衡全自动惰气吹扫装置和有机泄露检测器可在发生有机蒸气泄漏时关闭联锁装置,保证安全 DVS Advantage软件可程序控制仪器,用户界面友好,满足数据完整性和安全性的最高标准待测样品置于微量天平上,已知浓度的蒸汽通过样品,记录式微天平可以测量由蒸汽吸附或脱附引起的质量变化。这种动态流动环境易于快速研究吸附/脱附过程。如果进一步实验选择需要,样品可以首先预热,这样可以加速体相吸附或者无机氧化物干燥过程的分析循环时间。加热过程可独立进行或通过软件来控制升温速率。
各位朋友,请问哪里有测蒸汽吸附(水蒸气和有机蒸汽)的仪器,我有一个样品,微孔,需要测试这些性质。我问了中山大学和福建物质结构研究所,要么坏了,要么时间排的很紧!
能进行物理吸附、化学吸附和蒸汽吸附测试,如果需要联系电话:13235197591QQ:2405917320如此贴违反相关版规,望谅,请删除
各位老师,我打算用一氧化碳鼓泡法代入水汽到红外原位池中进行测试,大家知道这样的红外原位吸附测试能用溴化钾窗片吗?水蒸气会不会腐蚀溴化钾窗片呢?谢谢了
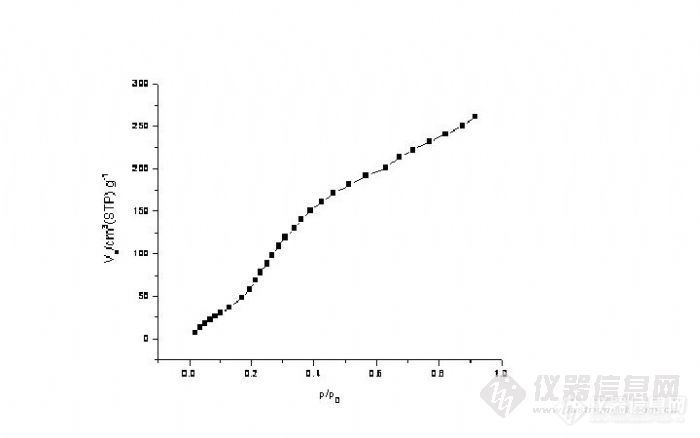
最近做了一个硅铝分子筛的水蒸气吸附,得出来的图像吸附量一直在上升,不知道该怎么分析,能否麻烦行家给点意见?[img]http://ng1.17img.cn/bbsfiles/images/2010/01/201001201631_197947_1601643_3.jpg[/img]
动态水分吸附法是一种非常适合分析材料水分吸附性能和记录水分吸附等温线的检测方法,适用于粉末,颗粒,碎片、片剂或块状固体。吸附仪常用来进行新材料的稳定性测试,这种长时间的测试可能需要几天、几周甚至是几个月,能够为评估环境温湿度对产品保质期产生的影响提供非常有价值的数据。 更进一步来说,分析研究在某一温湿度条件下有多少水分能够透过包装渗透到内部被材料本身吸附非常重要,被吸附的水分从外界环境中迁移到包装内部是影响带包装物体保质期的主要原因。 采用动态水分吸附仪来检测带包装药品或食品的水蒸气吸附性能,对于产品防潮性的检测和保质期的预测有着重要的指导意义。
在[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]前装了一个干燥器,里面是变色硅胶,然后反应出来的气体有CO,CO2,CH4,CH3OH,水蒸气,想知道变色硅胶除了吸附水还会吸附其他的气体嘛。
[font=arial, helvetica, sans-serif][color=#000000]大气气溶胶是指悬浮在大气中的固体和液体颗粒共同组成的多相体系。人们所处的大气环境实际就是由不同相态的颗粒物均匀分散在空气中形成的一个气溶胶体系。常见的大气气溶胶包括直接排放至大气的沙尘、道路扬尘和黑炭等一次颗粒物,以及通过化学反应形成的二次颗粒物,例如二氧化硫和氮氧化物通过大气氧化形成的硫酸盐和硝酸盐等。由于大气气溶胶的环境、气候及健康效应,在过去几十年里,对它的理化性质的研究正日益受到包括化学家、环境学家等科学家等的重视。[/color][/font][font=arial, helvetica, sans-serif][color=#000000]吸湿性是气溶胶最重要的物理化学性质之一(Tang et al., 2019a)。例如对于研究大气化学来说,吸湿性会影响实际环境条件下大气颗粒物的含水量,从而会影响颗粒物的大气化学反应活性;从大气能见度和直接辐射强迫的角度来看,在实际大气环境中,颗粒物吸水会导致其粒径增大,从而影响颗粒物的光学性质,继而影响气溶胶的消光系数、对能见度的影响以及对直接辐射强迫的影响;另外,气溶胶的吸湿性也与气溶胶颗粒物的云凝结核活性和冰核活性密切相关。[/color][/font][font=arial, helvetica, sans-serif][color=#0070c0]1. 已有吸湿性测量技术的局限性[/color][/font][font=arial, helvetica, sans-serif][color=#000000]现有研究中常用的吸湿性测量技术主要有吸湿性分级差分迁移率分析仪(H-TDMA)、电动力天平、显微镜以及红外光谱等(Tang et al., 2019a)。目前最常用的吸湿性测量技术为H-TDMA,该仪器是通过测定不同相对湿度下气溶胶的电迁移率直径来研究其吸湿性。使用该仪器对气溶胶的吸湿性进行表征时,必须假设气溶胶为球形,但某些颗粒物的形貌并不规则,例如花粉、烟炱以及矿质颗粒物等。另外,H-TDMA的测量精度较为有限,仅可测定颗粒物大于1%的直径变化。[/color][/font][font=arial, helvetica, sans-serif][color=#000000]电动力天平是通过测量单个颗粒物的质量变化来研究其吸湿性,虽然它对颗粒物的形貌没有要求,但该仪器的灵敏度同样比较有限,一般只能测量大于1%的质量变化。此外,显微镜也常用于测量颗粒物的吸湿性,它可以通过测量颗粒物的形貌变化来直接观察颗粒物粒径的大小变化从而研究其吸湿性。然而该技术同样基于球形颗粒物的假设,且灵敏度有限。另外,红外光谱是一个非常灵敏的吸湿性测量方法,该方法通过测量颗粒物中水的红外光谱来研究吸湿性,但把颗粒物中水的红外吸收光谱定量转换为颗粒物的含水量时存在一定的限制。[/color][/font][font=arial, helvetica, sans-serif][color=#0070c0]2. 蒸汽吸附分析仪[/color][/font][font=arial, helvetica, sans-serif][color=#000000]虽然目前用于颗粒物吸湿性的测量手段较为丰富,但准确测定非球形的或者吸湿性较弱的颗粒物的吸湿性仍然是一个很大的挑战。本课题组自主开发和建立了使用蒸汽吸附分析仪测量大气颗粒物吸湿性的新方法,相关研究成果由Atmospheric Measurement Techniques发表(Gu et al., 2017a)。该方法通过测定不同相对湿度下颗粒物的质量变化来研究其吸湿性,其原理如图1所示。[/color][/font][align=center][img=图片1.png]https://img1.17img.cn/17img/images/202104/uepic/616e1c5d-0f0c-45d0-8af1-47ca370a87e5.jpg[/img][/align][align=left]更多详见:[url]https://www.instrument.com.cn/news/20210420/578041.shtml[/url][/align]
在深的吸附势阱中,对低相对压下的分子就具有相当强的捕捉能力,表现为I型吸附等温线,这是由于微孔内相对孔壁吸附势的重叠从而引起低相对压力下促进的微孔充填(Micropore Filling)。初看起来微孔充填与毛细凝聚有些类似,但实际上微孔充填是取决于吸附分子与表面之间增强的势能作用的微观现象,而毛细凝聚则是取决于吸附液体弯液面(Meniscus)特性的宏观现象,两者应区别对待;另外对于极性分子和表面官能团作用的情形,应考虑除Lennard-Jones相互作用势以外的其它相互作用。http://www.best17.cn/admin/editor/UploadFile/2007122522298474.jpg Fig.1-8 10-4-3 Potential of nitrogen in slit-like pores (Here,the zero point of z as the center of pores) 图1-8狭缝型孔隙中氮的吸附势(零点Z看作孔隙中心) 这种吸附力场的改善已经由高的吸附等容热提供了实验证据;同时Everett和Powl通过理论计算表明,在小于两个分子直径的狭缝型孔隙内以及在小于六个分子直径的圆形孔隙内会引起吸附势的增强;Gregg和Sing等表明这种改善效应可以在比Everett和Powl所预测的孔径更大的孔隙内发生。 正是由于纳米空间内分子间相互作用的增强,不仅使固体-吸附质之间的相互作用增强,而且使吸附质-吸附质之间的相互作用改善,这就使得对于吸附在纳米空间的物质表现出一些特异的现象。用α-FeOOH改性的ACF通过铁氧化物的化学助吸附(Chemisorption-Assisted)表现为对NO较高的吸附容量(303K,300mg/g),可以形成NO的二聚体(NO)_2,而且该二聚体相当稳定。在与SO_2共存的条件下,NO会发生如下歧化反应生成N_2O:3(NO)_2=2N_2O+2NO_2,而该反应在通常条件下只有在高压下才得以进行。Kaneko假设在纳米空间吸附的分子形成的分子簇(Molecular Clusters)为液滴,这时,液滴周围的蒸气与液滴之间的压差△P由Young-Laplace方程计算,液滴的大小与表面张力γ之间存在如下关系:△P = 2γ/r_m,r_m是液滴、蒸气界面的曲率半径,代表液滴大小。当液滴为lnm时,在纳米空间中的水受到约相当于1400atm的压力,对于相似条件下的液氮则受到约相当于200atm的压力,由此吸附在纳米空间内的分子可以看成是处于高压环境之中。 不仅纳米空间内的分子簇会形成特定的结构,在吸附的同时,吸附剂的固体结构也会发生变化。当沸石(Zeolite)上发生氮吸附时,沸石晶态的对称性发生改变,而活性炭上发生氮吸附时,其结构单元微晶石墨的层间距会变小。所有这些都表明吸附质分子间的相互作用也非常强。纳米空间独特的分子场,有可能会发现一些新的分子功能。 实际上由于孔隙的微观性以及纳米尺度(分子级)的原因,要想对孔隙的起源作较为理想的阐明非常困难。Dubinin认为炭质吸附剂中含有各种不同尺寸的孔隙,最大的孔隙甚至可以用光学显微镜观察出。要想提供有关孔隙的直接证据目前较为先进的分析仪器主要有扫描隧道显微镜(STM-Scanning Tunnel Microscopy)、透射电子显微镜(TEM-Transmission Electric Micros-copy)、原子力显微镜(AFM-Atom Force Microscopy)等。Illinois大学以Economy为首的研究小组通过STM建立了一套较为完整的ACF数据库,共包含有800多张图片。由STM照片可以清晰的看到ACF表面和端面上孔隙结构的差异,以及不同尺度的孔隙,进一步由STM照片可以看出在不同位置由于刻蚀程度的差异而形成不同的孔隙;当然由此也可推断孔隙的发展历程。 图1-9所示为用于表征不同孔径的方法及其简单机理。压汞法主要用来表征大孔区域和大部分中孔区域的孔隙。该法利用液态Hg在200MPa高压下压入孔体系,所填充的容积是压力的函数。中孔的容积和分布可以由毛细凝聚的蒸气吸附来进行表征,有关蒸气凝聚的压力与孔隙的半径密切相关。这些方法都利用了吸附凝聚的密度与其液相密度相一致的假设,但实际上按照t法,所形成的吸附膜其吸附相密度与正常的凝聚相密度之间存在一定的差异。http://www.best17.cn/admin/editor/UploadFile/20071225224041766.jpg 在微孔范围的孔隙填充可以用基于Polanyi势能理论的Dubinin方程来表达:W = Woexp。此处,W是吸附量;A=RTLn(Po/P)代表Polanyi的吸附势(吸附相与平衡气体间的自由能变化);Wo为微孔容积;Eo为特征吸附能,是依赖于微孔结构的参数;β是由表面-分子间相互作用所决定的系数,被称为亲和系数(β = 1,以苯为标准);n为指数(1~3)。n = l时对应孔径分布较宽的炭质吸附剂,n = 2时对应孔径分布较窄的炭质吸附剂,n = 3时对应特别结构的CMS。从Dubinin方程解析可以获得吸附模式、细孔体积以及吸附热等有关信息。依据特征吸附能Eo可以推测细孔直径,还可进一步算出微孔范围内的孔径分布。Marsh认为通过Dubinin方程对吸附等温线进行分析可以提供一些非常有价值的信息。由于极微孔的尺度与吸附质分子大小具有几乎相同的量级,故而吸附质分子要想穿透整个孔隙比较困难,尤其在较低的温度和较低的相对压力下,表现更加明显。这是受被称之为活性扩散控制的结果,如前所述活性扩散类似于化学反应需要一活化能,随着温度的升高以及相对压力的增加,吸附速率呈指数增加。这些小的孔隙对小于其尺度的分子表现出吸附而对大于其尺度的分子表现为不与吸附,呈现出狭义的筛分效应。实际上不仅这些小的孔隙,只要吸附质分子的有效直径大于吸附剂孔口尺寸,就应表现出筛分效应。利用活性扩散可以对尺寸较小的孔隙如极微孔进行分析。 另外常用于表征微孔孔隙的方法还有比较作图法,该法将吸附等温线与标准等温线(通常是表面化学组成相类似的非孔性固体的吸附等温线)进行比较。实际上前面提及的t法也是一种比较法,但由于t法在微孔体系中的实用性受到质疑,目前α_s法正成为主流。α_s法是Sing和Gregg提议的用于细孔性固体的解析方法。α_s值定义为标准等温线上各相对压力下的吸附量除以P/Po = 0.4时标准物的吸附量(W_(P/Po=0.4))而得的比值,即α_s = W/W_(P/Po=0.4),将P/Po变换为α_s表示,这样试样的吸附等温线就可与标准等温线进行比较。特别是由Kaneko等提议的从低α_s值范围获得的高分辨α_s法是对微孔固体孔隙解析非常有效的方法,图1-10所示为具有代表性的α_s图。http://www.best17.cn/admin/editor/UploadFile/2007122522440719.jpg Fig.1-10 Various α s-plots 图1-10不同类型的α -图 平坦表面(包含大孔表面)、中孔以及微孔其α_s图各不相同。一般来讲随着大孔性、 中孔性固体向微孔性固体偏移,其吸附容量增加。中孔的毛细凝聚、微孔的容积充填(F偏离F-Swing)以及协同的微孔充填(C-偏离C-Swing)出现在图1-11的上部,由此可以对孔隙的尺度进行简单的判定。微孔型固体的α_s图可分为:F偏离的F型、C偏离的C型以及两种偏离共存的FC型。F型一般认为其孔径宽度在0.7nm以下,由于受极微孔内强的分子场的影响,在比平坦表面吸附更低的分压下就发生了单分子层吸附;C型可以看作是在单分子“涂层"(即孔壁上的单层吸附)之外的残余空间内发生的促进吸附,其孔径大于1.4nm;表现为FC型的吸附剂孔径范围在.7nm到1.4nm之间。从α_s图高压端引出的外推直线的截距给出微孔容积,其斜率给出外表面积;而从原点引出的直线的斜率可获得全表面积,与全表面积相比外表面积非常小时,高压端外推直线
如题,请教。GC,在线分析,想在气路中加一段净化装置,气体由N2,H2,CO,CO2组成,可能会有水蒸汽,加了硅胶怕对气体有吸附。请问硅胶能吸附N2,H2,CO,CO2吗?
测量空气VOC成分,低温富集可能达到-30度,空气中水蒸气会不会结冰堵塞富集管,或者损坏吸附剂。如果富集前对空气除水,该如何除水呢?
2011年3月22日大昌华嘉商业(中国)有限公司在广州中山大学举办了“吸附仪在新材料上的应用”研讨会。来自高校和科研院所的专家和技术人员100余人出席研讨会。此次研讨会主讲人是日本拜尔BEL公司Keita Tsuji博士。 在研讨会之前,王磊经理首先向大家介绍了大昌华嘉公司的历史及发展现状。大昌华嘉是一家具有200年历史的瑞士国际集团,作为BEL比表面分析仪,Kruss接触角测量仪,Microtrac激光粒度产品在中国总代理,负责其所有产品、技术的推广销售和服务。 日本BEL公司专业研究生产容量法气体吸附分析仪的专业制造厂商,推出一批又一批吸附领域的前沿技术。多站式蒸汽吸附仪系统和多站式化学吸附仪系统,将仪器测定的高效率和高精度完美结合起来。 http://bimg.instrument.com.cn/lib/editor/UploadFile/20114/20114185116423.jpg 会上Tsuji博士介绍了国际上第一双站微孔吸附仪在2006年面试,唯一一个使用0.1Torr压力传感器系统,多站式蒸汽吸附仪系统和多站式化学吸附仪系统,将仪器测定的高效率和高精度完美结合起来。固体电解质膜水分吸附和质子传导分析仪,燃料电池综合评价装置等,极大地丰富了表面吸附表征方法,同时也为拜尔公司高品质的产品和服务赢得了口碑。 物理吸附同步连接XRD、GC、磁悬浮天平 化学吸附仪链接质谱、红外、低温脉冲和TPR 高压吸附仪在储氢材料的应用 http://bimg.instrument.com.cn/lib/editor/UploadFile/20114/20114185116575.jpg
渗透率是薄膜类材料的重要特性,精确测量薄膜、纸张等的水分子渗透率对于评估其作为包装材料在不同水蒸汽分压环境下隔绝水分的功能有着重要的意义。采用动态水分吸附仪法检测渗透率的具体方法如下:将薄膜(纸张)覆盖在样品盘上,将盘内放置干燥剂、饱和食盐水溶液或水来制造一个与环境不同的水蒸汽分压,从而使水分子透过薄膜(纸张),迁移到达另一边。这种水分子的迁移可以通过称量样品盘的重量来检测。 这种方法比NIR检测法耗时长,但是结果非常准确,可以得到薄膜(纸张)材料的精确渗透率。德国Proumid公司的动态水分吸附仪包括一个高灵敏度的天平和能够调节温湿度,气流循环的密闭空间。为渗透率的检测提供最理想的环境。 仪器有六个样品盘,可以同时测量5个薄膜(纸张)样品的渗透率,大大节省了试验时间。
气体吸附法是测量材料比表面积和孔径分布的常用方法。其原理是依据气体在固体表面的吸附特征,在一定的压力下,被测样品表面在超低温下对气体分子可逆物理吸附作用,通过测定出一定压力下的平衡吸附量,利用理论模型求出被测样品的比表面积和孔径分布等与物理吸附有关的物理量。其中氮气低温吸附法是测量材料比表面积和孔径分布比较成熟而且广泛采用的方法。在液氮温度下,氮气在固体表面的吸附量取决于氮气的相对来说压力表(P/P0),P为氮气压力表,P0为液氮温度下氮气的饱和蒸气压,当P/P[0在0.05-0.35范围内时,吸附量与相对压力P/P0符合BET方程,这是氮吸附法测定比表面积的依据;当P/P0符合BET方程,这是氮吸附法测定比表面积的依据,当P/P0≥0.4时,由于产生毛细凝聚现象,氮气开始在微孔中凝聚,通过实验和理论分析,可以测定孔容-孔径分布(孔容随孔径的变化率)。 比表面积是多孔材料、超细粉体材料和催化剂的最重要物性之一。有两种常用的表示方法:一种是单位质量的固体所具有的表面积(m2/g),表示为 Sg=S/m 另一种方法是单位固体具有的表面积(m2/m3),表示为Sv=S/V式中:m-被测样品质量(g); V-被测样品体积(m2). 一般多用第一种方法来表示比表面积,计算比表面积的一般BET公式。假设Vd为吸附量(体积),Vm为单分子层的饱和吸附量,P/P0为N2的相对压力,C为第一层吸附热与凝聚热有关常数,P0为饱和蒸气压,W为样品质量,则BET公式为P/Vd(P0-P)=1/VmC+(C-1)/P/P0式中,P/P0一般选择相对压力在0.05-0.35范围内,仪器可以测得dV值。如果只需要的比表面积,就可以只选P/P0=0.05-0.35之间5点进行测量就可以了,也就是通常所说的五点法确定比表面积。
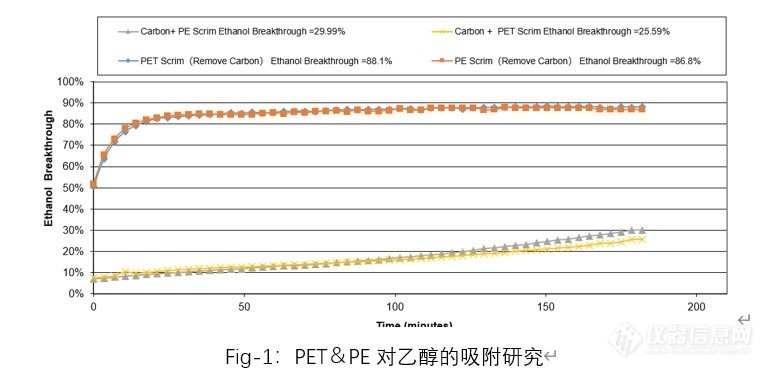
[align=left] 气固吸附:当气体或者水蒸汽分子接触到一种固体时,固体会吸收或者吸附一部分。这种现象被称之为气固吸附。这种固体被叫做吸附剂,气体或者水蒸汽被称之为被吸附物。[/align][align=left] 当气体分子接近固体表面的时候,这种分子由于物理力而被固体表面吸附,这就是范德瓦尔斯表面张力。气固吸附的主要作用也是范德华力的作用。[/align][align=left] 吸附剂是一种有很多细小微孔的固体,细小的微孔有着很强的吸附能力,主要原因是因为如下:[/align][align=left] (1) 细小的微孔提供了大的表面积;[/align][align=left] (2) 细小的微孔提供了很强的吸附力。[/align][align=left] 活性炭是非常常见的一种吸附材料,特别是对有机物的吸附。[/align][align=left] 最近客户提出活性产品对乙醇的吸附能力的质疑:认为乙醇是极性物质,活性炭是非极性物质,活性炭对乙醇的吸附能力较差,如果外层材料使用PET材料包裹活性炭的产品吸附乙醇的会效果好于使用PE材料,因为PET材料是极性,而PE是非极性。[/align][align=left] 那真的是这样吗?为了验证客户的猜测,我们买来100ppm的乙醇混合气体,进行对PET包裹活性炭和PE包裹活性炭的效果验证,另外也测试了单独的PET和PE材料对乙醇的吸附测试.经过验证(Fig-1),发现PET材料包裹活性炭的吸附效果超微优于PE材料包裹活性炭的吸附能力;但是单独的PET材料和PE 材料对乙醇的吸附没有差别。[/align][align=center][img=,690,333]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311626418215_4501_2942222_3.jpg!w690x333.jpg[/img][/align][align=left] 这说明了PET材料对乙醇的吸附并没有什么效果,可能PET材料包裹活性炭时,裸漏活性炭的面积更多,会导致PET材料包裹活性炭的吸附效果略好点。[/align]
对于99.995%的高纯吸附载气和吸附质气体,其中的主要杂质气体为水份。假设气源气体中水份的含量为0.004%,则样品处在-195.8℃、30ml/min的流速中120min内停留在粉末表面的水的量为 0.14ml(标况下的体积),而对于500mg比表面积为1m2/g的材料,在其表面形成水的单分子层吸附所需要的水蒸汽的量为:0.12 ml(标况),与实际停留在粉末表面的水量相当,材料表面已经被水分饱和;如果不吹扫处理继续测试,那测试结果将不可能正确。对于色谱法孔径测试需要测试三四十个分压点,影响更是显著,若分压点之间不做吹扫处理,最后得到的结果将不是固体材料本身对氮分子的吸附了,而是包覆了水分子的颗粒对氮分子的吸附了,孔隙也早已被高沸点易吸附气体杂质H2O、CO2饱和。 要消除吸附质气源中的气体杂质H2O、CO2等的影响, 可采用冷阱气体净化装置,冷阱是消除高沸点气体杂质的有效方式;比表面仪配备的冷阱,使本会被样 品吸附的水份等高沸点杂质提前被冷阱捕获,使得经过净化后的高纯氮和高纯氦气体中的水分含量低于10-17Pa,达到超高纯气体状态; 3H-2000系列比表面仪是国内唯一配备冷阱的比表面仪器,这也是该系列仪器能够取得高精度和高分辨率的因素之一。
看环境标准废气分析,用吸附管吸附后使用二硫化碳解吸,想问一下为什么要用二硫化碳,用乙醇或丙酮的话解吸能力会差很多吗?顺便问一下,我们自己实验室分析的废气结果经常与环保局测定结果不一致,请问如何验证废气分析结果准确性?
[size=3]1 活性炭吸附的优点及其在VOCs 治理中的应用活性炭微孔结构高度发达,使它具有很大的比表面积,由表面效应所产生的吸附作用是活性炭吸附最明显的特征之一。活性炭吸附主要有以下特点:(1)活性炭是非极性的吸附剂,能选择吸附非极性物质;(2)活性炭是疏水性的吸附剂,在有水或水蒸气存在的情况下仍能发挥作用;(3)活性炭孔径分布广,能够吸附分子大小不同的物质;(4)活性炭具有一定的催化能力; (5)活性炭的化学稳定性和热稳定性优于硅胶等其他吸附剂。活性炭吸附法适用于大风量、低浓度、温度不高的有机废气治理。此法工艺成熟,效果可靠,易于回收有机溶剂,因此被广泛地应用于化工、喷漆、印刷、轻工等行业的有机废气治理,尤其是苯类、酮类的处理。王淑勤等[7]利用亚硫酸氢钠和碳酸钠改性的活性炭对室内空气污染中甲醛进行了治理研究,考察了颗粒活性炭、粉末活性炭、改性活性炭对甲醛去除率的影响,测试了改性活性炭的平衡吸附量,吸附穿透时间。结果表明,亚硫酸氢钠和碳酸钠改性的活性炭对甲醛的去除率为 60 %,动态治理后能够达到国家室内空[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]量标准。 2 活性炭吸附挥发性有机气体的影响因素 2.1 活性炭孔隙结构对VOCs 吸附的影响孔隙结构是指孔隙容积、孔径分布、表面积和孔的形状。按照杜比宁(Dubinin)的分类,孔的半径(r) 苯甲苯。通常而言,吸附能力随吸附质的相对分子质量增大而提高,即有机物相对分子质量越大,穿透时间越长。但这个实验中,苯比甲苯的穿透时间长,这估计是因为活性炭具有非极性表面,在较低的浓度下更易于吸附同为非极性物质的苯。 2.5 混合VOCs 对活性炭吸附的影响多组分VOCs 吸附时,除了各组分吸附亲和力大小不同外,各吸附组分之间会发生相互作用和竞争效应,使得吸附过程复杂化。活性炭对不同有机废气吸附的过程中其吸附结合常数不同,而有机废气在活性炭表面的吸附过程实际上是一个吸附和解离相平衡的过程,当吸附能力强的有机废气达到一定浓度后必然对吸附能力弱的有机废气的吸附位点形成竞争性结合,使得吸附能力弱的有机废气解离量大于吸附量,从而在局部形成浓度高于进气浓度的现象,当这种竞争性结合达到稳定之后,吸附能力弱的有机废气在活性炭上的吸附和解离又重新达到平衡,其表现在穿透曲线上即为浓度跃升现象。金一中等[16]对MA-70 型活性炭吸附苯、甲苯进行了研究,结果表明,MA-70 活性炭对甲苯的吸附能力强于苯,吸附能力较强的甲苯组分能将已被吸附的苯组分置换出来。王长林[17]对多组分有机气体(包括乙酸乙酯、正己烷、丁酮和氯仿)在活性炭上的吸附行为进行了考察,结果表明:活性炭对非极性乙酸乙酯和极性丁酮的吸附能力非常接近,对正己烷的吸附能力稍差,对氯仿的吸附能力最差。吸附能力弱的有机废气发生浓度跃升现象,但吸附能力强的有机废气不能完全置换吸附能力弱的有机废气。 2.6 其他因素对活性炭吸附的影响温度、流量、吸附柱填充密度等对活性炭的吸附也有影响。孙辉[11]研究了吸附法去除室内苯系物,结果表明,气流量加大会较快到达穿透点和吸附饱和点,使穿透曲线发生左移,曲线斜率不变;填充密度对穿透时间与饱和时间都有影响,密度大有利于吸附。 3 总结活性炭吸附法是处理挥发性有机气体最广泛应用的方法。本文归纳了活性炭吸附有机气体的几个重要影响因素,指出活性炭的孔隙结构及其活化方法对挥发性有机气体的吸附有重要的影响,并指出了进气的初始浓度越高,到达穿透点时间和完全饱和时间越短;VOCs 的物化性质(如吸附质的极性、分子质量、沸点等)对穿透点有影响;多组分有机气体共存时,会发生相互作用和竞争效应,吸附能力强的有机废气置换吸附能力弱的有机废气,从而在局部形成浓度高于进气浓度的现象。此外,温度、流量、吸附剂填充密度等也是重要的影响因素。在实际应用中,应该结合考虑活性炭吸附VOCs 的综合影响因素,设计出最佳的工业应用参数和流程。[/size]
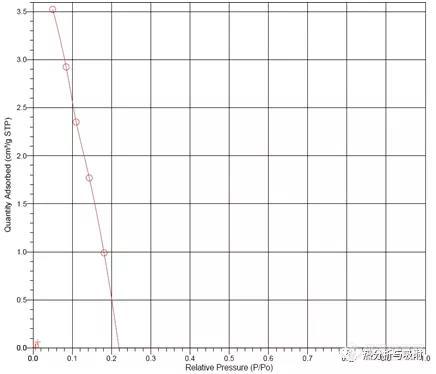
[b]作者:[/b]丁延伟,[color=#2d374b]中国科学技术大学理化科学实验中心副主任。[/color]在上一篇文章中介绍了《物理吸附实验中样品用量的选择》,按照物理吸附实验程序,在确定了样品用量之后,接下来要对样品进行脱气处理。脱气条件的选择与样品量均十分重要,是取得理想的实验结果的前提。在本文中,将对吸附实验中的脱气条件的选择进行阐述。脱气的目的是最大程度地去除表面吸附的溶剂和从环境中吸附的水蒸气等其他分子。如果表面吸附的这些物种不能有效去除,在进行吸附实验时势必会影响最终的吸附等温线的吸附量数值,由此导致所得到的比表面积、孔容积等参数的数值变小。因此,只有选择合理的脱气条件,有效地脱除样品表面吸附的溶剂、水蒸气等分子,才可以得到理想的实验结果。常用的脱气方式分动态脱气和真空脱气两种。其中,动态脱气是在一定的温度下,使加入到样品管中的样品上方流通一定流速的气体(通常为氦气或者氮气),流动的气氛将加热时表面吸附的溶剂、水分子等带离样品管,从而达到脱气的目的。而真空脱气则是在一定的温度下,将装有样品的样品管连接在仪器的脱气装置的真空,通过负压将表面吸附的溶剂、水分子等带离样品管。显然,真空脱气方式的脱气效果要优于动态脱气方式。实际上,大多数的物理吸附实验采用在一定的温度(通常高于室温)下抽真空的方法。在选择脱气条件时,通常需要设定合适的脱气温度和等温时间。一般来说,脱气温度越高,表面吸附的溶剂、水分子等的脱除效果越好。设定合适的脱气时间可以使这些分子有足够的时间被脱除。通常,在较高的脱气温度下所需的脱气时间可以适当缩短。在实际设定脱气条件时,与脱气时间相比,合适的脱气温度显得更加重要。如果脱气温度设定过高,通常会引起样品发生熔融、分解、表面结构变化、孔塌缩,由此得到的结果并非测试样品的实验结果。图1为在较高的脱气温度下得到的异常等温线。由图可见,即使样品中含有大量的孔结构,过高的脱气温度引起了孔的塌缩,从而导致吸附能力减弱,无法得到正常的等温线。 [align=center] [img=,436,374]https://ng1.17img.cn/bbsfiles/images/2019/10/201910241425496214_771_3224499_3.jpg!w436x374.jpg[/img] [/align][align=center]图1[/align]另一方面,在过低的脱气温度下,即使采用过长的等温时间(如12小时或24小时)也无法有效地脱除表面吸附的溶剂、水等分子。这些分子的存在会挤占表面的吸附位或者堵塞孔道,导致比表面积和孔容积下降。通常用热分析技术中的热重法(TG)和差示扫描量热法(DSC)来选择合适的脱气温度。理想的脱气温度应在熔点和分解温度之前。如果材料中含有结晶水,实验时如果不考虑结晶水存在时的结构状态,则脱气温度应在结晶水的分解温度之上。以下举例说明。例1 图1中的绿色曲线为含有结晶水的草酸钙样品的热重曲线,121℃开始的第一个失重台阶对应于结晶水的失去过程,389℃开始的第二个失重台阶对应于草酸钙分子结构中的CO的失去过程。(1)如果需要测量不含结晶水的草酸钙的物理吸附实验并由此得到比表面积孔容积等信息,则脱气温度应设置在300-350℃范围内。(2)如果需要测量含有结晶水的草酸钙样品的物理吸附实验并由此得到比表面积孔容积等信息,则脱气温度不得高于120℃。[b]需要特别指出,由于热重实验是在常压下的动态气氛下以恒定的加热速率条件下得到的,而吸附实验的真空脱气是在很定温度下的真空环境下进行的,设定的脱气温度应低于热重曲线的开始温度20-50℃,以免样品在脱气过程中发生分解。如果采用动态气体吹扫法进行脱气,则温度可以适当提高。由于脱气在等温下进行,所设定的脱气温度也应低于热重的开始分解温度5-10℃。[/b]例如,对于以上第(1)种情形的脱气温度可以设在80-100℃范围中的一个温度,对于以上第(1)种情形的脱气温度可以设在320-350℃中的一个温度。设置的温度越低,则脱气时间可以适当延长。常用的脱气时间为60-600分钟不等。另外,样品中孔的含量越多,脱气时间也应越长。[align=center][img=,560,270]https://ng1.17img.cn/bbsfiles/images/2019/10/201910241425579422_175_3224499_3.jpg!w560x270.jpg[/img][/align][align=center]图2 含有结晶水的草酸钙的TG曲线[/align]例2 为一种有机物的DSC曲线,由图可见样品自130℃开始逐渐发生熔融,如果需要对这种样品进行物理吸附实验,则脱气温度可以设置在80-110℃。如果温度设置过高,则易引起样品中孔结构的塌缩。[align=center][img=,560,271]https://ng1.17img.cn/bbsfiles/images/2019/10/201910241426055932_7531_3224499_3.jpg!w560x271.jpg[/img][/align][align=center]图3 一种有机物的DSC曲线[/align]综合以上两个实例,在设置脱气温度时应综合TG和DSC曲线来确定合理的脱气温度,对于熔点较高(高于400℃)或者不存在熔点的样品而言,只通过TG实验就足够了。另外,如果样品在加热过程存在不可逆相变,由于不同的结构形式的吸附能力也有差异,则脱气温度也应低于该温度。需要特别指出,[b]如果样品已经经过高温(高于400℃)热处理过程,由于脱气装置的最高工作温度在400-450℃范围,则可以直接将脱气温度设定在300-400℃[/b]。[b][color=black]如果样品中含有大量的微孔,在样品可以承受的最高温度下脱气时还应大幅度延长脱气时间,以使微孔中的吸附水、溶剂等分子彻底脱除。[/color][/b][color=black]如果样品中含有在合成或处理过程中引入的一些稳定性很好的无机盐如钠盐、钾盐等,这些化合物会堵塞表面的缺陷或孔,影响测量结果。如果不希望样品受这些无机化合物的影响,则应对样品进行再次处理。对于一些再合成或处理过程中有意在样品中负载的一些活性组分如铂、金等,则无需在处理时将这些活性组分进行置换。[/color]
阀进样连续测量污染源的非甲烷总烃,现场用水喷淋的方式吸附VOC,导致废气里面的液态水和水蒸气含量超高。色谱柱一个小时就没法用了。有没有什么不怕水分子、不会吸附水、容易反吹干净的的甲烷色谱柱?[color=#333333]TDX-1可以吗? [color=#333333]PLOT Q能否满足要求?[/color][/color]测试条件: 甲烷柱 Q柱 ,120度柱温。测量周期4分钟,甲烷大概30秒出峰。余下时间都是反吹时间。
怎样评价活性炭的吸附能力 吸附分液相吸附和[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]吸附两类,液相吸附能力常以吸附等温线进行评价,[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]吸附能力以溶剂蒸气吸附量评价。 吸附等温线表示一定温度下吸附系统中被吸附物质的分压或浓度与吸附量之间的关系,即当保持温度不变,可测得平衡吸附量和分压或浓度间的变化关系。以剩余浓度为横轴,以活性炭单质量的吸附量为纵轴可绘出关系曲线。 当保持分压或浓度不变,可测得平衡吸附量和温度间的变化关系,绘出关系曲线,即吸附等压线。由于在工业装置中少量成分吸附大致在等温状态下进行,所以吸附等温线最为重要和常用。 溶剂蒸气吸附量表示[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]吸附性能,可用颗粒活性炭的四氯化碳吸附率的测定为例,在规定的试验条件下,即规定的炭层高度、气流比速、吸附温度、测定管截面积、四氯化碳蒸气浓度的条件下,持含有一定四氯化碳蒸气浓度的混合空气流不断地通过活性炭,当达到吸附饱和时,活性炭试样所吸附的四氯化碳的质量与试样质量之百分比作为四氯化碳的吸附率。 活性炭应用中对于吸附能力,最好用实际拟用的活性炭、操作的条件、具体的处理物进行评价测试。 活性炭的吸附量,即单位活性炭所吸附的吸附质的量,工业上也有称为活性炭的活性,活性有两种表示方法: 静活性-----即通常所指的吸附剂达到平衡的吸附量。 动活性----是指流体混合物通过活性炭床层,其中吸附质被吸附,经一些时间的运作,活性炭床层流出的流体中开始出现含有一定的吸附质,说明活性炭床层失去吸附能力,此时活性炭上已吸附的吸附质的量,就称为活性炭的活性。是设计大量的、经常的、重要的吸附系统所需的数据。 用液相等温线法测定活性炭吸附能力的标准实用方法,可用于测定原始的和再活化的和粉状活性炭的吸什能力影响吸附有哪些因素 影响吸附的因素有三方面: A、活性炭方面 理想的活性炭要具有在多孔中能容纳最大重量的吸附质的内表面和大孔容。微孔多的活性炭倾向于吸附小分子,大孔多的活性炭倾向于吸附较大的分子。因此总表面和孔容的数据不能用来评估活性炭的可能有效性。 B、吸附质方面 一般有机物的吸附随着分子量的增加而增加,直至分子太大进不了炭孔。非极性有机物较极性有机物更易从水溶液中被吸附,有其他有机物混存时会影响吸附,一般无机物不易被吸附。易液化或高沸点的气体较易吸附。混合气体中,纯净状态下易被吸附的气体优先被吸附。 C条件方面 温度影响扩散速率和吸附平衡,扩散速率与黏率有关,提高温度会提高扩散速率,而达到平衡加快,但是最终的吸附量也较低。压力增高,气体的吸附量增大,尤其常压下吸附性较小的气体,这是变压吸附的基础。 PH值会影响溶液中有色物的吸附。许多有色化合物在不同PH值下会改变结构和色泽,在不同的PH值下会改变结构和色泽,在不同的PH值下用同样的活性炭处理同样的溶液,一般在较代PH值下有较佳的吸附。 由于活性炭制造时活化条件的不同而PH有异,为配合应用,活性炭PH值可在制造时调整。活性炭产品之间如何区分,应该如何选择活性炭呢? 活性炭是由各种富含碳的原料制造而成。因此,用不同的原料制造的活性炭必然会有不同的特性。一般来说,以煤为原料制造的活性炭通常采用水蒸气或二氧化碳气体活化,产品的形状以颗粒状为主,其孔径分布以微孔居多,更适合于吸附液相和[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]中分子量和分子直径较小的物质,吸附性能指标通常以亚甲蓝吸附值和碘吸附值表示;以木屑为原料制造的活性炭通常采取化学法活化,产品的形状以粉状为主,其孔径分布可通过调节化学活化剂的配比来进行控制,比较灵活,既可以制造出孔径分布以微孔居多的产品也可制造出孔径分布中孔(过渡孔)占较大比例的产品,后者则比较适合于吸附液相中分子量和分子直径较大的物质吸附性能指标以焦糖脱色率表示;以果壳类为原料制造的活性炭通常采取水蒸气和二氧化碳气体活化,产品的形状以颗粒状为主,由于其特殊材质的因素,其孔径分布介于上述两类活性炭之间,因此其应用范围更为广泛,缺点是受国内原材料的限制,成品较高。选用粉状活性炭还是粒状活性炭 要根据具体工艺目的结合两种活性炭的各自优点而选用。 粉状活性炭通常在液相应用,加入液体后经搅拌混合、过滤或沉降,而得所要的液体。以粉状活性炭处理的优点是:适用于间歇工艺;易控制加入量;可利用现成过滤设备;价格较低。 粒状活性炭可用于液相,也可用于[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]。一般将要处理的液体或气体连续通过活性炭柱。以粒状活性炭处理的特点是:适用于连续工艺与自动控制;较少活性炭耗量,使用的炭/液比高;较易清洁操作;因价较高大量使用时应予再生,且较易再生。用过的活性炭怎样再生 再生是活性炭应用后的延伸工序,再生的方式随应用的具体情况而不同:有的边应用边再生,即边吸附边解吸;有的多次应用,合并再生;有的分散应用,集中再生。 再生方法可分为两大类:(1)加热再生 a、 热空气再生-----以空气为脱附载体。 b、 水蒸气再生-----低沸点溶剂用一般蒸汽,高沸点溶剂用过热蒸汽。 加热再生是常用的方法,过程如下: 干燥----加热到100~150摄氏度蒸发活性炭中的水分和一部分低沸点有机物; 碳化-加热到300~700摄氏度,挥发或分解一些有机物,有部分有机物碳化留在活性炭中。 活化---加热到700摄氏度以上,使留在活性炭中的碳和活化气体反应,逸出所生成的气态产物,重新造孔。 冷却---活化后急冷以防氧化。 (2)无热再生 (3)移动床再生 (4)流化床再生 (5)加热再生 (6)生物再生 (7)催化废炭再生 (8)微波再生 (9)超生再生 (10)化学法再生 (11)用表面活化剂再生 (12)废水处理炭再生
酶联免疫吸附法怎样做方法验证?酶联免疫吸附法以农业部1025号公告为代表,在2008年推出了一系列标准,后来又很少见了。
adsorption,absorption,desorption单看这三个英文单词就知道这三种现象之前存在关联却又各不相同。吸附(sorption)描述的是吸收(absorption)和吸附(adsorption)的动作——脱附(desorption)是一种与吸附相反的动作。吸附和吸收是化学和生物学科当中一种非常重要的过程。因此当我们考虑分离方案的时候,尤其是在使用气相色谱法和液相色谱法时,我们有必要弄清楚这些过程并理解他们之间的差异。吸附和吸收的一个最主要区别在于,一个是表面处理而另一个是本体处理。吸附——发生在基质的表面。吸收——指的是一种物质进入到另一种物质的主体或者体积内部,比如说气体被液体所吸收。Adsorption吸附吸附是一种表面过程,表示气体或者液体在另外一种液体或者固体表面形成的积累现象。我们可以根据吸附质(化学物质所吸附的基质)和吸附剂分子之间的相互作用强度进一步解释何为吸附现象。物理吸附——物理吸附也称范德华吸附(Van der Waals),它是由吸附质和吸附剂分子间作用力所引起,此力也称作范德华力。化学吸附——化学吸附是吸附质分子与固体表面原子(或分子)发生电子的转移、交换或共有,形成吸附化学键的吸附。化学吸附过程所涉及的能量比物理吸附过程要多。这两种吸附作用的差异性主要体现在分子之间相互作用所产生的结合能大小的差异。Absorption吸收吸收是涉及固体、液体或气体的整体性质的现象。吸收所描述的是原子或者分子经由材料表面进入到材料体内的一种现象。和吸附现象类似的是,吸收也存在物理吸收和化学吸收两种情况。物理吸收——指的是溶解的气体与溶剂或溶剂中某种成分并不发生任何化学反应的吸收过程。此时,溶解了的气体所产生的平衡蒸汽压与溶质及溶剂的性质、体系的温度、压力和浓度有关。化学吸收——指的是当原子或者分子被吸收时所发生的化学反应。一个典型的例子就是当硫化氢从沼气流取出并转化成固体硫。Desorption解吸解吸是吸收的逆过程,又称气提或汽提,是将吸收的气体与吸收剂分开的操作。解吸是一种物质被另外一种物质释放的过程,或者也可以理解为一种物质从另外一种物质的表面或者穿过其表面而被释放出来的过程。当均衡情况发生改变时,解吸现象就会发生。想象一下,有一罐与周围环境相平衡的水,进入并离开这罐水的空气的量是相同的——水中氧气的浓度是恒定不变的。如果水温升高,水的平衡和溶解性发生变化,那么水中的氧气会被释放出来,因此水中氧气的含量降低。Adsorption and Desorption in Chromatography色谱法当中的吸附与解吸现象吸附和解吸是色谱法中的主要操作过程。通过待分离样本与固定相之间发生的吸附和解吸速率来实现样本的分离。如果色谱柱的条件有利于分子的吸附,那么分子就会附着在固定相上面,从而实现了与其他样本化学物质的分离。当色谱柱的条件有利于解吸,那么就会发生与吸附相反的现象——化学物质就会进入流动相当中。
近期读到一篇关于晶体潮解动力学的研究论文,采用动态水分吸附仪对于潮解点的判定和潮解动力学的研究分析非常深入。最近对这一课题很感兴趣,希望做类似研究的各位多多讨论。文章摘要如下:晶体材料及其混合物的潮解动力学传热模型Heat transport model for the deliquescence kinetics of crystalline ingredients and mixturesNa Li a, Lynne S. Taylor b, Lisa J. Mauer a, *a Department of Food Science, Purdue University, 745 Agriculture Mall Drive, West Lafayette, IN 47907, United Statesb Department of Industrial and Physical Pharmacy, Purdue University, 575 Stadium Mall Drive, West Lafayette, IN 47907, United States关键词:吸附速率,晶体材料,潮解,传热Key words: Sorption rate, crystalline ingredients, deliquescence, heat transport 摘要:当环境的相对湿度超过潮解点RH0时,易潮解的晶体发生一级溶解过程。对于压片易潮解材料,潮解的速率随着RH超出RH0差值的增加而加速;但是,迄今还没有关于晶体食物材料粉末的潮解动力学模型被发表。本文采用一种多样品重量法水分吸附仪SPSx测定了常见的粉末食品材料(如柠檬酸、氯化钠、蔗糖、果糖、山梨糖醇和木糖醇)及其混合物的水分吸附速率。水蒸气的吸附速率与样品的直径、温度和组成有关。实验证明样品压片的潮解传热模型能够成功的应用于粉末材料和其混合物,其实验结果进一步的论证了潮解的理论基础,为在可控的恒湿箱内预测潮解过程中的水分吸附速率提供了有力的工具。Abstract:Deliquescent crystalline solids undergo the first order dissolution process of deliquescence when the environmental relative humidity (RH) exceeds the deliquescence point (RH0). The rate at which deliquescence occurs increases as the RH increases above the RH0 in compressed disks of select deliquescent ingredients; however, a kinetic model for the deliquescence of powdered crystalline food ingredients and blends thereof has not been published. The water vapor sorption rates of commonly used powder food ingredients (citric acid, sodium chloride, sucrose, fructose, sorbitol, and xylitol) and blends were determined using a multi-sample gravimetric moisture sorption analyzer. The water vapor sorption rate was dependent on sample radius, temperature, and sample composition. The heat transport model for the deliquescence of compressed disks was successfully extended to the powder ingredients and blends. Such results enable further understanding of fundamental theories of deliquescence and provide a useful tool in the prediction of water vapor uptake rate during deliquescence in controlled RH chambers.

[img=材料表征之物理吸附,690,517]https://ng1.17img.cn/bbsfiles/images/2020/02/202002241040543064_4373_3904283_3.jpg!w690x517.jpg[/img][img=物理吸附仪,690,517]https://ng1.17img.cn/bbsfiles/images/2020/02/202002241041301720_2977_3904283_3.jpg!w690x517.jpg[/img][img=物理吸附分析仪,690,517]https://ng1.17img.cn/bbsfiles/images/2020/02/202002241043459714_5656_3904283_3.jpg!w690x517.jpg[/img][img=物理吸附测试仪,690,517]https://ng1.17img.cn/bbsfiles/images/2020/02/202002241044185308_7597_3904283_3.jpg!w690x517.jpg[/img][img=物理吸附仪,690,517]https://ng1.17img.cn/bbsfiles/images/2020/02/202002241044444424_9357_3904283_3.jpg!w690x517.jpg[/img][img=物理吸附表征,690,517]https://ng1.17img.cn/bbsfiles/images/2020/02/202002241045065334_3428_3904283_3.jpg!w690x517.jpg[/img][img=材料表征之物理吸附,690,517]https://ng1.17img.cn/bbsfiles/images/2020/02/202002241045557845_1528_3904283_3.jpg!w690x517.jpg[/img][img=物理吸附测试,690,517]https://ng1.17img.cn/bbsfiles/images/2020/02/202002241045552293_6474_3904283_3.jpg!w690x517.jpg[/img]
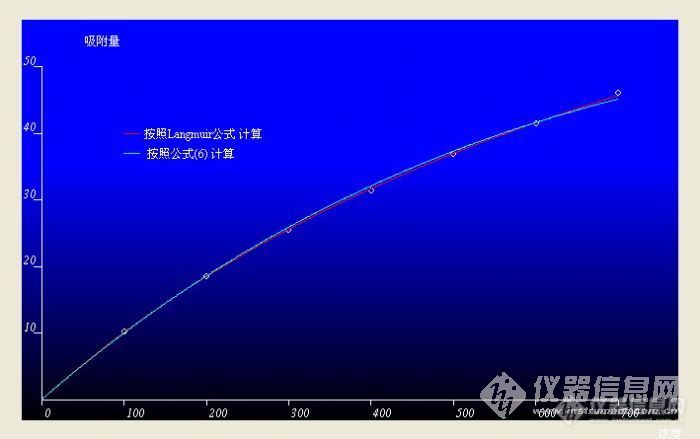
请阅览附件……………………为了方便大家查看,帮楼主贴出内容………………………… 二元溶液吸附方程验证汇集 Daichaozheng通常认为在溶液中的吸附是多层吸附的,但是多层吸附与van der Waals作用能与分子间有效距离六次方成反比这一原理是矛盾的。原因是吸附剂表面生成的van der Waals作用能其力度不足以克服“第二层分子”的热运动。因此溶液吸附不会是多层吸附。运用统计力学方法,在均一位势模型和理想势阱点阵模型基础上,考虑分子之间van der Waals作用能和溶液吸附过程的顶替效应可以推导出二元溶液单分子层吸附方程为:http://ng1.17img.cn/bbsfiles/images/2012/08/201208091006_382640_2961690_3.jpg在第三届科学仪器网络原创大赛 “二元溶液体系吸附方程的验证”一文中,作者计算了苯胺、苯酚、环己醇、正丁醇、正己酸、正戊醇、正戊酸在六种炭吸附剂上的吸附数据。四十二组数据计算值与实验值的均方差在0.008-0.047之间。为了更充分的考察公式(1)、(2)的适应性,作者采用了更多的文献数据进一步进行验证。今汇集如下。在18℃的恒温条件下,用骨炭从水溶液中吸附醋酸。在不同的醋酸平衡浓度下,每公斤骨炭中吸附醋酸量 与溶液中醋酸的摩尔浓度 的关系如表1所示:http://ng1.17img.cn/bbsfiles/images/2012/08/201208091007_382642_2961690_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208091007_382643_2961690_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208091007_382644_2961690_3.jpg从公式(5)可以看到,溶液浓度的改变引起分子间环境的变化,从而导致分子之间势能场的变化,最终影响吸附过程的焓变。公式(5)表示的是一摩尔吸附值从溶液态进入吸附态这一过程的焓变的量,这也是吸附剂表面吸附吸附质时van der Waals作用能所作的净功。物理吸附是一个可逆的动态平衡过程,平衡时物质在吸附剂表面的化学位与在溶液中的化学位相等。从道理上讲,只有吸附的作用能大于分子的动能才能形成稳定的吸附层。由公式(5)可以看出,随着溶质浓度的改变,血炭从水溶液中吸附正丁醇van der Waals作用能作的净功在4.1868*984J/mol到4.1868*1258.6J/mol之间。根据理论,分子的平均动能为http://ng1.17img.cn/bbsfiles/images/2012/08/201208091010_382646_2961690_3.jpgJ/mol,在室温情况下(300K)分子的平均动能大约为4.1868*450 J/mol。这个数值小于吸附过程的焓变。如果设想吸附是单层的,这个吸附过程是可以进行的;作一个粗放的估计如果形成多层吸附,根据van der Waals作用能公式,第二层与吸附剂表面有效距离增加一倍,吸附过程焓变只能及第一层的1/64,也就大约是在4.1868*11J/mol 到4.1868*20 J/mol之间。这个数值远小于分子的平均动能为http://ng1.17img.cn/bbsfiles/images/2012/08/201208091009_382645_2961690_3.jpg J/mol(4.1868*450j/mol)。因此吸附剂的表面依靠van der Waals作用能是不能够约束住溶质分子形成第二吸附层的。至于第三层、第四层则更不可能了。http://ng1.17img.cn/bbsfiles/images/2012/08/201208091011_382648_2961690_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208091011_382649_2961690_3.jpg硅胶可以从水溶液中吸附碱金属离子,表3则列出了硅胶自水溶液中吸附无机碱计算值与实验值的比较。计算采用的公式为:http://ng1.17img.cn/bbsfiles/images/2012/08/201208091012_382650_2961690_3.jpg从计算结果可见,对于不同的碱金属离子有不同的A,B 值,但是不管是Li+、Na+ 、 K+还是NH4+,每吸附一个碱金属离子就要从硅胶表面顶替下来七个水分子。 带电荷的离子型化合物,由于电荷同性相排斥的原理,形成多层吸附则更不可能了。http://ng1.17img.cn/bbsfiles/images/2012/08/201208091013_382651_2961690_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208091026_382653_2961690_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208091026_382654_2961690_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208101148_382997_1688674_3.jpg 图6 一氧化碳在木炭上吸附量计算值与实验值的比较http://ng1.17img.cn/bbsfiles/images/2012/08/201208091027_382656_2961690_3.jpg计算的数值。 图6表示一氧化碳在木炭上吸附量计算值与实验值的比较。由图可见二元溶液单分子层吸附方程(1)在 p=0 的情况下也可以很好地描述气体的吸附过程。 结论:通过对van der Waals作用能的分析,解释了在溶液吸附只能形成单分子层吸附的原因。在过去推导的溶液吸附方程的基础上,拟合了多组吸附质、吸附剂的实验数据,得到良好结果。证明了溶液单分子吸附理论成立。所推导的溶液吸附公式成立。 参考文献 戴朝政,卢佩章,色谱 ,1994年第3期 戴朝政,第三届科学仪器网络原创大赛,二元溶液体系吸附方程的验证 赛冷LG,兰吉PW,加布里桑CD著,傅献彩等译。物理化学习题集,北京:人民教育出版社,1959:299。 严继民,张启元,高敬综。吸附与凝聚固体的表面与孔。北京:科学出版社。1986:93 段世铎,谭逸玲。界面化学。北京:高等教育出版社,1990:107 顾惕人编,傅鹰选集。北京:冶金工业出版社,1990:41

S2。对于两种重金属离子,土壤对Pb的吸附能力明显高于对Cd的吸附能力。当初始浓度较低时,3个土壤对Cd、Pb的吸附量都随溶液中平衡浓度的增加而急速增加。但当浓度再加大时,Cd、Pb吸附等温线的斜率随溶液平衡浓度的增加而降低,这种吸附行为可能是因为Cd和Pb在实验土壤样品上有多个吸附位点造成。http://ng1.17img.cn/bbsfiles/images/2011/08/201108311455_313311_1601823_3.jpg2.3 Cd、Pb 1:1浓度时的竞争吸附Cd、Pb 1:1浓度时竞争吸附的等温吸附曲线见图2。从图中可看出,Cd、Pb 1:1浓度竞争吸附时的曲线和Cd、Pb单一离子吸附时的曲线相似,都随Cd、Pb离子加入浓度的增加,土壤对其吸附量也增大。但当Cd、Pb离子共存时,由于不同重金属离子对吸附位点的竞争作用,三个土壤对Cd、Pb的吸附性能明显不同于Cd、Pb单一离子存在时的吸附情况。随着竞争离子的加入,[font='Times New Ro
做溶出时,是需要做滤膜吸附验证的,一般都怎么做呢?
[b]洁净蒸汽与工业蒸汽的不同[/b]杭州瓦特节能工程有限公司 李少鹏[b]工业蒸汽[/b]主要是指普通自备锅炉产生的蒸汽和电厂供应的热网蒸汽。[b]普通蒸汽锅炉[/b]直接加热炉水而产生的蒸汽。工业蒸汽作为热量载体一般用于间接加热或直接接触加热使用,也可以用于加湿使用。普通蒸汽锅炉产生的工业蒸汽基本满足大多数的直接或间接加热要求,相对于其它加热介质或流体,蒸汽是干净、安全、无菌、高效的热媒介。自备蒸汽锅炉的给水品质会影响蒸汽的品质。我们知道,锅炉内蒸汽在蒸发的同时,不可避免会携带部分炉水进入蒸汽系统,而蒸汽携带的肮脏炉水对蒸汽系统产生一定的破坏和影响。同时根据美国FDA的规范, 用来作为蒸汽锅炉阻垢的六偏磷酸钠,缓蚀用的氢氧化钠,除氧用水处理药剂是不能用于和食材或食品和食品容器有直接接触的。这对直接接触加热和灭菌是有一定影响的。蒸汽在输送中,会由于冷凝而产生对碳钢管道的腐蚀,腐蚀物,形成黄水。一旦黄水、杂质被携带至生产工艺中,可能对产品形成影响。当蒸汽中含有3%以上的冷凝水时,在产品表面的冷凝水对热量传递的阻碍,使得到达产品的实际接触温度会低于设计温度要求。所以通常在蒸汽入口采用瓦特高效汽水分离器会非常有效。锅炉给水中除氧不彻底,会导致蒸汽中混有空气等不凝性气体,空气等不凝性气体的存在会对蒸汽的温度形成另外的影响,蒸汽系统内的空气未排除或未完全排除,一方面由于空气是热的不良导体,空气的存在会形成冷点,使得附着空气的产品达不到设计温度。[b]电厂供应的热网蒸汽[/b]一般是热电厂发电以后的副产品,首先为了确保发电效率和安全,蒸汽的过热是必不可少的,有时过热度超过100℃。蒸汽过热度是影响蒸汽加热和灭菌的一个重要因素,经常会被忽略。饱和蒸汽灭菌原理是蒸汽遇冷产品凝结而释放出大量的潜热能,使产品的温度上升。而过热蒸汽,其性质相当于干燥的空气,其本身的传热效率低下;另外一方面,过热蒸汽释放显热而温度下降没有达到饱和点时,不会发生冷凝,此时放出的热量非常小,使得热量传输达不到加热和灭菌要求。此现象在过热3℃以上时即表现明显。蒸汽过热还可导致物品快速老化。热网蒸汽在远距离输送中,会由于散热冷凝而产生大量冷凝水,冷凝水的存在对碳钢蒸汽管道形成腐蚀,典型的腐蚀后冷凝水呈现黄水或黄褐色污水。这些污染蒸汽会对蒸汽系统产生较大的影响。热网蒸汽的其它用户在建设、维护、使用过程中,也会有潜在的风险杂质进入蒸汽系统。瓦特蒸汽工程师在实践中,在热网蒸汽中发现过多余的连接材料、没有完全冲洗的管道焊接杂质、甚至一些安装工具、阀门内件和垫片等。热网蒸汽往往是同时供应多个客户,客户负载的变化会导致管网蒸汽的温度、压力、流量、过热度变化,这些变化有时会影响到蒸汽用户的正常使用。所以常见热网蒸汽问题包含蒸汽黄水污染、蒸汽中各种杂质、压力波动等现象,也包含蒸汽中含有的空气、过热蒸汽、蒸汽潮湿等不容易发现的潜在影响因素。所以洁净蒸汽至少包含给水纯度、蒸汽本身的干度(冷凝水含量)、不凝性气体含量、过热度、合适的蒸汽压力和温度、以及足够的流量。洁净蒸汽是经过处理的蒸汽,包括超滤蒸汽、水浴蒸汽和汽—汽洁净蒸汽发生器产生的干净的、符合要求的蒸汽。[b][color=black]超净过滤装置[/color][/b][color=black]滤材采用不锈钢烧结毡(纤维高温烧结)多级过滤蒸汽中的杂质,同时通过汽水分离及时去被污染的冷凝水和溶解在冷凝水中的可溶性固态和气体。超净过滤装置的自动排气阀有效地排除蒸汽中的不凝性气体。[/color][color=black]超净过滤装置的过滤精度高达0.5[/color]μm,其过滤效率完全符合3-A关于洁净蒸汽过滤的标准,可以有效过滤蒸汽中含有的水垢、铁锈、颗粒等杂质,提高蒸汽质量。[b]水浴蒸汽装置[/b]专为电厂的热网蒸汽设计,热网不干净的蒸汽在RO水中洗澡,在去除污染物的同时,消除过热度,稳定供给压力,将洁净蒸汽发生器、减温器和蓄热器集于一体,实现热网蒸汽的洁净供应,而几乎没有工业蒸汽的衰减和效率下降。[b]汽—汽洁净蒸汽发生器[/b]把RO水经不锈钢板式换热器加热后,以汽水混合物的状态进入汽水分离罐。在汽水分离罐中实现汽水分离后,洁净的干蒸汽由上部出口输出进入用汽设备,未蒸发的水分保留在汽水分离罐内。分离罐中的水位通过自动水位控制器,由进水电动控制阀控制在设定的水位。自动排污检测系统不断检测汽水分离罐中水的盐值,控制盐水的排放。工业蒸汽在进入板式换热器之前通过气动控制阀,受到洁净蒸汽所需压力的控制,从而调节进入换热器的工业蒸汽的流量,确保产生的洁净蒸汽达到要求的压力和温度,也使得洁净蒸汽发生器的效率得到提高。瓦特食品级洁净蒸汽发生器具有本质的区别。洁净蒸汽发生器的流程、结构、能耗、控制和文件,与洁净蒸汽品质作为核心要素予以考量。特别是洁净蒸汽的流量,流量的波动直接导致洁净蒸汽的压力和温度变化,同时洁净蒸汽流量的变化也会很大程度地影响到蒸汽的干度。洁净蒸汽的洁净度保证不仅在于洁净蒸汽的产生,还包含其洁净输送管道系统设计以及洁净蒸汽加热系统的控制和冷凝水排放方案。所以其初始投资和运行费用、管理和维护成本都有较大幅度的提高。只有依据蒸汽来源不同,品质不同,蒸汽品质的需求不同,来选择适合的蒸汽等级和蒸汽处理装置。
测量比表面和孔径分析的方法包括:气体吸附法、压汞法、电子显微镜法(SEM 或 TEM)、小角 X 光散射(SAXS)和小角中子散射(SANS)、电声电振法、核磁共振法、图像法大孔分析技术等。其中气体吸附法是常见的分析方法。气体吸附法孔径测量范围从 0.35nm~ 100nm 以上,涵盖了全部微孔和介孔,甚至延伸到大孔。另外,气体吸附技术相对于其它方法,容易操作,成本较低。如果气体吸附法结合压汞法,则孔径分析范围就可以覆盖从大约 0.35nm到1mm 的范围。气体吸附法也是测量所有表面的最佳方法(不规则的表面和开孔内部的面积)。使用气体吸附法进行分析的仪器常用来测定物质的比表面及孔径特征,也可以直接测量物质的吸附特性,因此也常统称为吸附仪。从实际用途来看,主要包含:比表面及孔径分析仪、多组分气体吸附仪、高压吸附仪、蒸汽吸附仪、真密度仪、化学吸附仪等。气体吸附法原理:当固体表面的原子所处的环境与体相原子不同,它受到一个不平衡的力的作用;因此,当气体与清洁固体表面接触时,将与固体表面发生相互作用;气体在固体表面上出现累积,其浓度高于[url=https://insevent.instrument.com.cn/t/Mp]气相[/url],这种现象称为吸附现象。吸附气体的固体物质成为吸附剂,被吸附的气体成为吸附质。依据吸附剂和吸附质之间的不同作用力,气体吸附分为物理吸附仪和化学吸附仪。物理吸附也称范德华吸附,它是由吸附质和吸附剂分子间作用力(范德华力)所引起,吸附于固体表面的气体分子,不与固体产生化学反应,这种吸附称为物理吸附;利用物理吸附原理测量的仪器被称为物理吸附仪。由于范德华力存在于任何两分子间,所以物理吸附可以发生在任何固体表面上。吸附剂表面的分子由于作用力没有平衡而保留有自由的力场来吸引吸附质,由于它是分子间的吸力所引起的吸附,所以结合力较弱,吸附热较小,吸附和解吸速度也都较快。被吸附物质也较容易解吸出来,所以物理吸附在一定程度上是可逆的。如:活性炭对许多气体的吸附,被吸附的气体很容易解脱出来而不发生性质上的变化。物理吸附的特点是:吸附热小,吸附速度快,无选择性,可逆,通常是发生在接近气体液化点的温度,一般是多层吸附。物理吸附仪可以测定物质的比表面积、平均孔径和孔径分布等,此外也可以直接测试物质吸附性能。化学吸附是吸附质分子与固体表面原子(或分子)发生电子的转移、交换或共有,形成吸附化学键的吸附,利用化学吸附原理进行测量的仪器被称为化学吸附仪。由于固体表面存在不均匀力场,表面上的原子往往还有剩余的成键能力,当气体分子碰撞到固体表面上时便与表面原子间发生电子的交换、转移或共有,形成吸附化学键的吸附作用。与物理吸附相比化学吸附具有吸附力强、对吸附气体有选择性、单层吸附、通常不可逆,样品不可回收再利用等特点,常用于测定催化剂酸碱活性位、活性金属表面积、金属分散度等。