推荐厂家
暂无
暂无
 银牌1年
银牌1年
 400-860-5168转4607
400-860-5168转4607
 留言咨询
留言咨询
 留言咨询
留言咨询
 留言咨询
留言咨询

 400-875-3676
400-875-3676
 留言咨询
留言咨询

 400-886-5615
400-886-5615
 留言咨询
留言咨询
 留言咨询
留言咨询

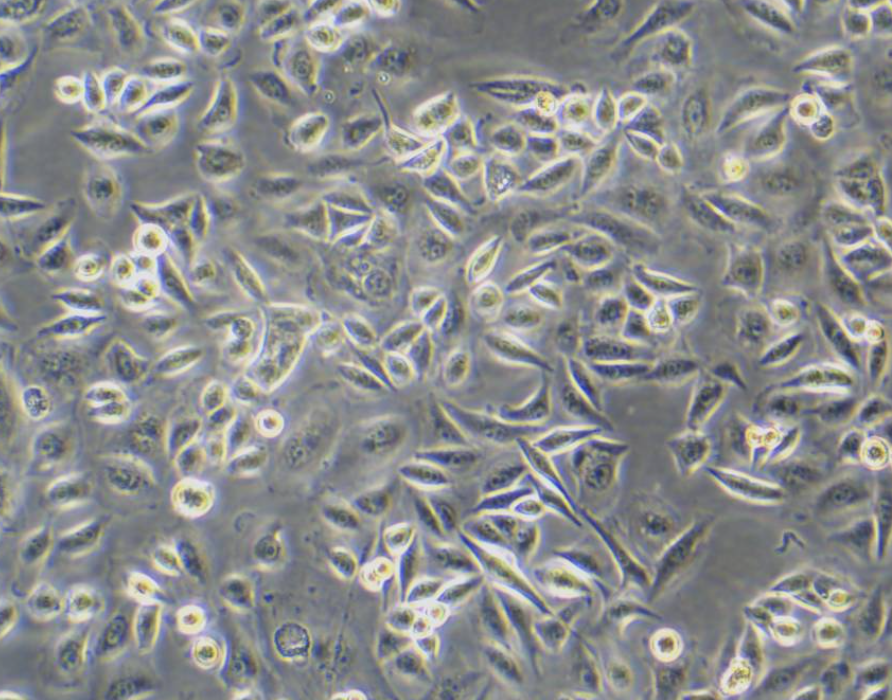


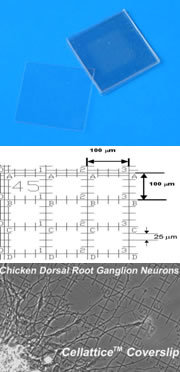

现在一般都是选择在液相中扫描活细胞,那么在空气中直接扫描固化好的细胞,查看其表面形貌还有应用价值吗?制样时对细胞的处理方法也多种多样,这些方法是不是大家现在都不用了?
目前血细胞分析仪在国内外医院都是进行血常规检查的必备仪器,它不但减轻了工作人员劳动强度,提高了实验结果的准确性,还提供了更多的相关实验指标,对疾病的诊断和鉴别诊断起了重要的作用。1检测系统 按照过去的老观念,添置设备就是买仪器,货比三家按性价比来选购仪器。但是传统的与当今理念显然存在差距,随着对检验管理的完善,政府对检验科开展的每个检验项目提出了更高的要求,卫生部关于印发《医疗机构临床实验室管理办法》的通知(卫医发〔2006〕73号)(下面简称《管理办法》)指出:“医疗机构临床实验室应当保证检测系统的完整性和有效性”。什么叫检测系统?《全国临床检验操作规程》3版明确指出:完成一个检验项目的检测所涉的仪器、试剂、校准品、质控品、消耗品、操作程序、维护保养程序等的组合,称为检测系统,若是人工操作,还必须包括操作人员。2检测系统重要性 检测系统的好坏将直接影响检测结果精密度、准确性和溯源性,但是如果每一个临床实验室对每一检验项目都做检测系统的评价是无法完成的,因此,国外厂商除了提供仪器以外,还将提供配套试剂、配套校准品,也规定了操作程序,形成了可靠的有溯源性的检测系统。上个世纪九十年代美国FDA、欧盟有关部门己经明确规定,在申报产品许可证时,不再是一台仪器的认可,而是要整个检测系统的申报与认可。用户按规定的检测系统(即封闭系统)去检测病人标本,质量是有保证的。现在我国有关部门也十分重视,有一定规模的国产血细胞分析仪厂家除了提供仪器以外,还可提供配套试剂、配套校准品和质控品,以及相应的检测系统评价报告,包括结果的溯源性。长期实践证明,只有形成固定的组合的检测系统才能保证检测结果的准确性和可靠性。选择单一的血细胞分析仪或是具有溯源性评价的检测系统,既是传统与当今理念的区别,笔者认为选择后者才能保证检测质量,保证结果的准确性。
一、酶消化法1、胰酶。这是用得最多的。一般浓度在0.25-0.5%。作用时间根据细胞种类、作用温度等因素而变化很大,从几分钟到几十分钟不等。0.25%的胰酶作用于单层贴壁的细胞,在37度条件下,一般消化1-5分钟就足够了。终止是用血清。主要作用于细胞间。配制时不能用含钙、镁的平衡液,否则影响活性。保存于-20度。2、胶原酶。这种方法比较少,一般是用原代培养时,从组织消化下细胞。这种方法作用温和,对细胞损伤较小,但是,价格也较贵。中止同样是用血清。二、离子螯合剂 不破坏细胞表面分子,仅与CAMs螯合,因此,如果检测细胞表面分子的话,尽量,甚至是一定不要用酶消化法。1、EDTA。用得也是非常多。一般浓度在0.02%左右。作用于细胞与间质,对细胞间也有一定作用。注意,它能显著影响pH值,而且在弱碱性条件下才易溶。因此,配制时应调节好酸碱度。它不能被终和。因此,消化下来的细胞要洗一遍。2、商品化的无酶消化液。个人的使用经常觉得对细胞的损伤比较大,但是分离成单细胞悬液的能力确实比较强。三、物理法 直接吹打或用细胞刮子将细胞刮下来。四、冷冻法 这是本人做细胞培养时发现的方法。此方法仅能用于细胞传代时。无法使组织上的细胞脱落下来。本方法的原理,我想是因细胞冷冻后收缩,从而从培养瓶上脱落下来。优点是:对细胞损伤小,不需要中止或洗细胞,方便,不需要另外配制消化液。特别适用那些贴壁不是特别紧,又特别娇气的细胞。不足是细胞常成小片脱落。此种方法曾用于因用其它方法传代导致大量细胞死亡操作的间充质干细胞、DC细胞的培养,效果非常满意。具体过程是:1、用较多的4度的PBS洗涤一遍细胞(以6孔板为例,加1.5 ml/孔);2、再加0.5 ml 4度的PBS,静置操作台上,很快细胞就小片脱落;3、轻轻吹打,细胞即完全脱落;4、按一定比例传代。


