看了热重分析仪/热天平(TGA)的用户又看了
热重分析法(TG、TGA)是在升温、恒温或降温过程中,观察样品的质量随温度或时间的变化,目的是研究材料的热稳定性和组份。广泛应用于塑料、橡胶、涂料、药品、催化剂、无机材料、金属材料与复合材料等各领域的研究开发、工艺优化与质量监控。
热重量分析的主要特点,是定量性强,能准确地测量物质的质量变化及变化的速率。根据这一特点,可以说,只要物质受热时发生质量的变化,都可以用热重量分析来研究。可用热重量分析来检测的物理变化和化学变化过程。我们可以看出,这些物理变化和化学变化都是存在着质量变化的,如升华、汽化、 吸附、解吸、吸收和气固反应等。
型号 | TGA-209A | TGA-209B | TGA-209C |
显示方式 | 24bit 色,7 寸LCD触摸屏显示 | ||
TG范围 | 1mg ~ 3g ,可扩展至 30g | ||
TG精度 | 0.01mg | ||
温度范围 | 室温~1200℃ | 室温~1350℃ | 室温~1550℃ |
温度分辨率 | 0.01℃ | ||
温度波动 | ±0.1℃ | ||
温度精度 | ±0.1℃ | ||
温度重复性 | ±0.1 ℃ | ||
升温速率 | 0.1 ~ 100℃/min | ||
控温方式 | 升温,恒温,降温(全自动程序控制) | ||
程序控制 | 可实现四段升温控制,特殊参数可定制 | ||
曲线扫描 | 升温扫描、恒温扫描、降温扫描 | ||
气氛控制气体 | 两路自动切换(仪器自动切换) | ||
气体流量 | 0-300mL/min | ||
气体压力 | ≤0.5MPa | ||
恒温时间 | 0 ~ 300min可任意设定 | ||
数据接口 | 标准USB接口 | ||
工作电源 | AC220V/50Hz | ||
产品尺寸 | 500*550*500(长宽高mm) | ||





第6章 热 重 法
6.1 引 言
对于一种物质或一种材料进行分析时,第一步通常是确定其质量。质量是确定物质含量的主要方法, 因此出现了在常规分析的基础上进行高精度质量测量的技术。这些仪器不仅是科学仪器,也常可以作为商用的工具被广泛应用于各行各业,例如各种秤或天平。热重法(Thermogravimetry,TG)或热重分析法(Thermogravimetric Analysis, TGA)也仅仅是作为这一基础性质测量的拓展,只不过其主要用来研究偏离室温或长时间进行的质量的测量。
作为热分析方法中应用领域最广的一种技术,热重法广泛应用于物理、化学、化工、矿物、食品、医药等材料相关的领域。在本章中,将主要介绍热重方法的工作原理/仪器组成、影响热重实验的因素、数据分析和应用等内容。
6.2 与热重法相关的术语与定义
6.2.1 热重法
热重法也称热重分析,是在程序控制温度和一定气氛下,测量试样的质量与温度或时间的关系的技术。
在早期与热重法相关的文献中,少数研究人员习惯将其称为“热失重分析法”。其实这种称谓是不合适的,这是因为有些试样在实验中会发生质量几乎不变(即恒重)或质量增加(即增重)等现象。例如,许多金属在空气气氛下加热至某一温度时, 往往会由于发生氧化反应而开始增重。
热重法的数学表达式为
在上式中,M为任意时间或温度下的质量,一般用质量的百分比表示;T为温度,单位通常为℃。在进行动力学和热力学分析时,其单位为K;t为时间,一般用秒(s)作为单位。当实验时间较长时,也可用分钟或小时等作为单位。
根据热重法的定义,其可以用来研究液态或固态物质的质量随温度或时间的连续变化,并且这种变化可在不同的气氛环境下进行。
通过热重法可以在不同气氛下进行实验,可以模拟物质在这些环境中质量的变化过程。实验中所用的气氛可以是惰性的,即在实验过程中不与试样发生任何作用,其作用是使试样分解时产生的分解产物及时脱离试样周围,使反应得以顺利进行。另一方面,实验气氛也可以与试样或试样在加热或等温过程中的中间产物发生作用,起到改变反应机理的作用。在一些特殊条件下,需要研究试样在特殊环境下(例如氧化、还原等环境下)的反应过程。
目前,商品化的热重仪的工作温度范围可以从室温至2800C。实验时, 温度的变化方式不仅仅可以实现线性升温和降温,还可以采用更加复杂的温度程序。
在表述热分析法时如果使用简称,应尽可能地使用“TG”。这是因为TG所对应的英文名称Thermogravimetry中己包含了“方法”的含义,如果再加上分析,在逻辑上略显冗余。在实际应用中,仍有相当多的文献采用“TGA”的表达方式。但在表示由热重法得到的曲线时,大多数人习惯于用“TG曲线”而不是“TGA曲线”来表示。另外,当热重法与其他方法联用时,热重部分的简称一般用TG表示。例如,热-差热分析简称为“TG-DTA”,热重/红外光谱联用法简称为“TG/IR”。
6.2.2 热重法的测量模式
热重法的测量模式主要有动态质量变化测量和等温质量变化测量两种。
6.2.2.1 等温质量变化测量模式
等温质量变化测量(isothermal mass-change determination)简称等温模式(isothermalmode),是在恒温T和一定气氛下,测量试样的质量随时间t变化的技术。
上述定义中所指的等温可以通过加热使试样处于高于室温的某一个恒定温度,也可以通过降温使试样处于低于室温的某一个恒定温度。从其他温度达到恒定温度的时间应尽可能短,即温度扫描速率越快越好。另外,在达到目标恒定温度时,不能出现“过冲”的现象(见图6.1)。
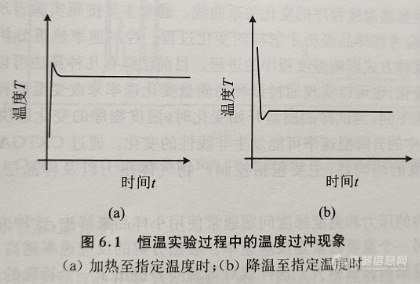
上述两种方法是TG实验中常用的两种实验方法。需要特别指出,在实际应用时可能在一次实验中会用到以上两种实验方式,例如,试样可以在以一定的加速速率加热至某一温度后等温一段时间,然后再继续加热。在该温度程序中,包含了“非等温一等温一非等温”三个阶段(图6.2)。
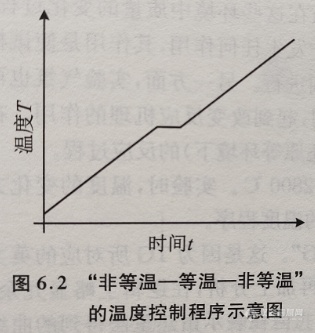
理论上,等温实验方法比非等温实验方法准确,但耗时长,操作繁琐,不宜广泛采用。
6.2.2.2 动态质量变化测量模式
动态质量变化测量模式(dynamic mass-change determination mode),又称温度扫描质量变化测量模式(temperature-scanning mass-change mode),是在程序升温、降温和一定气氛下,测量试样的质量随温度变化的技术。
这种模式是热重实验中最常用的测量模式。实验时,根据需要选择合适的温度扫描范围和温度扫描速率,在一定的实验气氛下测量试样的质量变化。
与等温法相比,非等温热重法快捷方便,一次实验可以获得较宽的温度范围的质量变化情况。但是,这种方法得到的实验结果受加热速率的影响较大,与真正的反应温度相比,有一定偏离。
6.2.3 控制速率热重分析
控制速率热重分析(Controlled-Rate Thermogravimetric Analysis,CRTGA),也称高分辨热重分析法,是控制速率热分析中的一种技术,其通过控制温度-时间曲线,使试样的质量按照恒定的速率变化的技术。
该方法是一种根据试样的失重速率而自动调整加热速率的热分析方法。目前,采取控制反应速率的主要方式有多阶恒温控制(即步阶升/降温方式)、动态速率控制和恒定分解速率控制等几种温度控制技术。主要通过热重仪器的软件来实现以上温度控制方式。
大多数常规的热重实验基于预定的温度控制程序(大多数为等温或线性控制的温度程序),测量试样的质量随温度程序的变化关系曲线。通常主要按照实验者所选择的温度程序来进行实验,很少会考虑样品经历了怎样的变化过程。控制速率热重分析通过允许测量样品的质量变化以某种方式影响温度程序的进程。目前已经有几种算法可以用来确定温度程序随试样行为的变化,也可以实现通过试样的质量变化速率来改变温度程序。与常用的线性升降温加热方式不同,当试样的质量开始变化时, 温度程序的变化取决于试样的分解过程,即在实验过程中的升降温速率可能发生非线性的变化。通过CRTGA的方法能够更精确地控制反应环境的均匀性,主要包括控制产物气体压力以及样品层内的温度和压力梯度。
对于样品层内的压力和温度梯度问题通常使用小样品来解决,这种方式可以减少质量和热传输问题。另一个重要因素是反应速率。吸热分解的反应速率越高,样品内出现显著的温度和压力梯度的机会就越大。这样就对等温实验提出了一个特殊的问题,因为在实验开始时反应速率太高所引起的潜在危险必须与结束时的反应速率太慢的问题相平衡,从而导致在实际时间尺度上反应不完全。线性升温实验也会带来类似的问题。对于这种类型的实验而言,反应速率在反应步骤的中点附近达到最大值。通过调整加热速率来限制这个最大值,会造成实验时间的不必要的延长。一旦选择了足够低的速率来避免过度大的温度梯度,在使用CRTGA方法时须确保实验可以在尽可能短的时间内完成,并且获得的结果不会发生失真。利用这种方法不仅可以有效地提高热重仪的分辨力,还可缩短实验时间。
这种实验方式可以通过调整敏感度因子和分辨因子来实现加热速率对质量变化速率的判断。
图6.3为线性加热和高分辨实验条件下CuSO4·5H2O的热重实验曲线。由图可见,5℃·min-1的线性加热速率无法使CuSO4·5H2O的5个结晶水的失去过程分离开来。而通过高分辨热重实验方法可以清楚地看到5个结晶水的失去过程。根据所设置的实验参数的不同,使用这两种方法所需的运行时间也将有所不同。
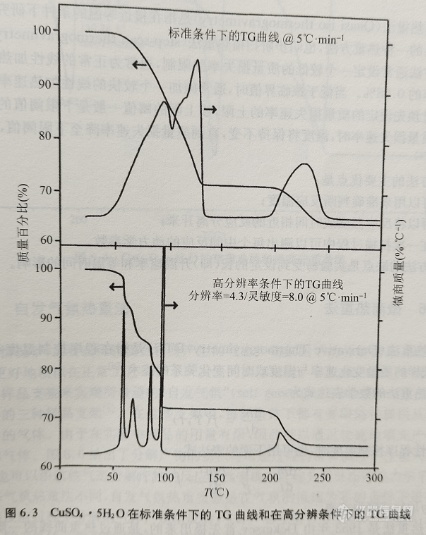
6.2.4 步阶式热重分析
步阶式热重分析,也称自动分步TGA(auto step TGA),是控制速率热重分析的一种方法,这种方法的原理是:在温度达到或者高于设定的失重速率时,仪器自动降低升温速率或者等温。而当失重速率低于设定的速率时,试样继续按照升温程序升温,从而达到失重台阶自动分步的解析效果。
这种方法可以提高热分析仪的分辨能力,有时会节省时间。但对于多个质量变化阶段的实验而言,其实验时间相比于线性升降温过程则会延长很多。在设定实验程序时,可以通过调整软件中的敏感度因子和分辨率因子来设定何时开始调整温度扫描速率。
该方法常用来使多连续分解的多步过程得到有效的分离,常用于研究多结晶水化合物或混合物。
6.2.5 准等温热重法
准等温热重法(Quasi iso thermogravimetry)是指在接近等温的条件下研究试样的质量与温度关系的一种热重方法,也叫步阶扫描热重法(step-scan thermogravimetry)。
这种方法通常设定一个较低的质量损失率的限制, 通常为正常的线性加热速率下最大质量损失率的0.08%。当低于该临界值时, 通常施加一个较快的线性加热速率直到质量损失速率超过预先设定的质量损失速率的上限,该上限的阈值一般是下限阈值的100倍。当达到这种质量损失速率时,温度将保持不变,直到质量损失速率降至下限阈值,之后继续重复该循环。
这种方法的主要优点是:
(1)可以用来准确判断反应温度;
(2)可以将反应温度或时间相近的反应分离开来;
(3)在一次扫描过程中可以测出每个中间反应的动力学参数。
这种方法的缺点是实验易受到设定的长(即)升温速率和等温时间的影响。
6.2.6 热重法
热重法(Derivative Thermogravimetry,DTG)是指在程序控制温度和一定气氛下,测量试样的质量变化速率与温度或时间变化关系的技术。
热重法的数学表达式为
当线性程序控制温度时,也可用下面的表达式:
式中,β为加热或降温速率。
热重法是1953年由Dekersey首先提出来的,是通过热重曲线的一阶导数得到的。对于目前的大多数商品化仪器而言,热重曲线的微分曲线可以使用仪器的分析软件附带的微分功能转换得到。早期的热重仪器的DTG曲线是通过热重仪信号输出部分增加一个线路单元来获得的。与TG曲线相比,DTG曲线可以更加清晰地显示出试样的质量随温度的变化信息。图6.4是CaC2O4·H2O在20℃·min-1的加热速率下得到的热重曲线和热重曲线,由图可见,CaC2O4·H2O随着温度的升高在99~220℃范围内逐步失去结晶水,DTG曲线的峰面积对应于TG曲线的失重台阶。图6.4中,DTG曲线的峰面积为0.602%·min-1·℃-1,该数值乘以加热速率(即20℃·min-1),其值为0.602×20=12.04%,与由TG曲线计算得到的台阶的失重量(12.27%)接近。一般来说,由DTG曲线得到的数值略低于TG曲线,这与在对峰进行积分时所选取的虚拟基线有关。
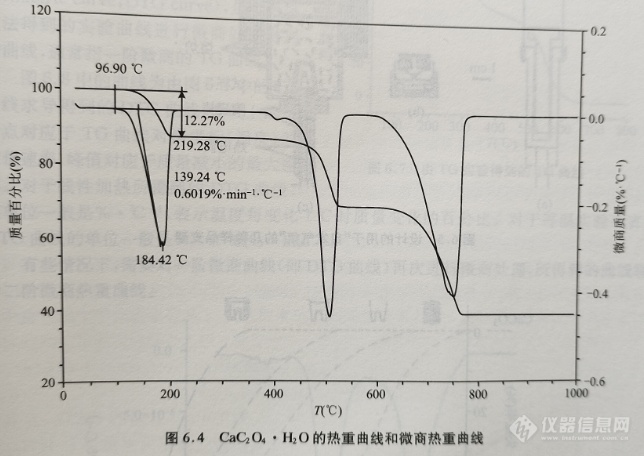
6.2.7 自发气氛热重法
在某些情况下,需要获得物质在自身产生的气态产物氛围下的分解信息。通过这样的条件,可以更好地模拟在正常工艺条件下所发生的实际情况。在文献[9-12]中设计了几种不同形式的样品支架来实现所希望的“自发气氛”(self generated atmosphere),在图6.5中描述了其中的三种样品支架。在这些支架中,每种条件下都有受限路径提供从较少的样品量中逸出的气体。由于在实验中样品的用量有限,因此可以通过快速地填充产物气体来置换原来的气体。图6.6给出了分解产物的累积对可逆过程的特征温度产生很大影响的实例。另外,也可以由这些气态分解产物的反应活性来确定这些分解反应的热力学平衡常数。
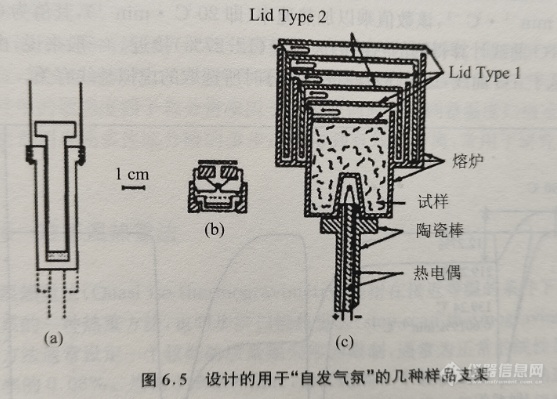
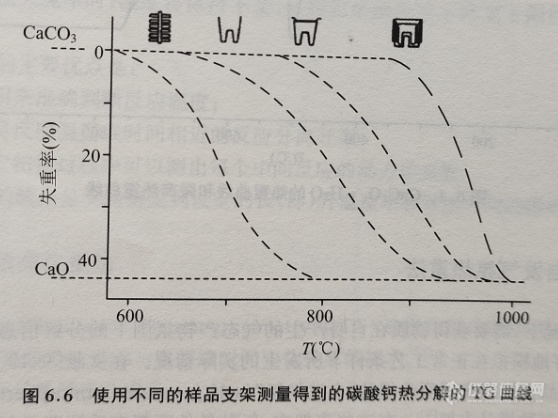
与动态气氛热重法不同,自发气氛热重实验是在气氛的流速为零的条件下进行的。自发气氛是由反应过程中分解的气体产物组成的,气体产物主要分布于试样的周围,并与试样紧密接触。随着气体产物浓度的增加,气体逐渐扩散到气相中,由不同的坩埚得到的热重曲线会有较大的差异。
研究自发气氛下材料的热分解过程有利于模拟材料在自然状态下随温度或时间变化的反应过程,有利于更深入地了解过程中的热力学和动力学信息。
6.2.8 热重曲线
热重曲线(Thermogravimetric curve, TG curve),也称TG曲线,是将热重法测得的数据以质量(或质量分数)随温度或时间变化的形式而表示的曲线,是热重实验结果的最直接的表现形式。
曲线的纵坐标为质量m或者质量百分数,向上表示质量增加,向下表示质量减小;横坐标为温度T或时间t,自左向右表示温度升高或时间增长。图6.7所示为试样按照一定的加热速率所得到的TG曲线。为便于比较,热重曲线的纵坐标大多用质量百分比表示,而不用试样的绝对质量表示。
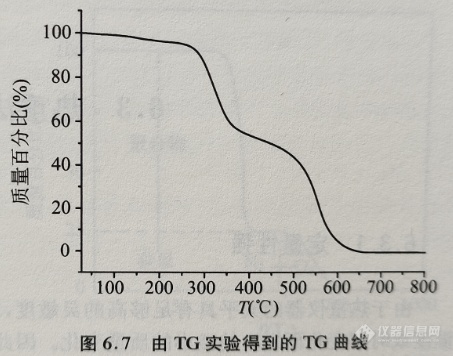
6.2.9 热重曲线
热重曲线(Derivative Thermog-ravimetric curve,DTG curve),是对由热重法得到的实验曲线进行处理得到的曲线,通常指一阶的TG曲线。
图6.8中的曲线为由图6.7中的TG 。曲线求导得到的DTG曲线,曲线上的每一点对应于TG曲线对横坐标(温度)的变化速率,峰值对应于质量减小的最大速率。对于线性加热所得到的DTG曲线,其单位一般是%·℃-1,表示温度每变化1℃时质量变化的百分比。对于等温实验而言,DTG曲线的单位一般是%·s-1或%·min-1。
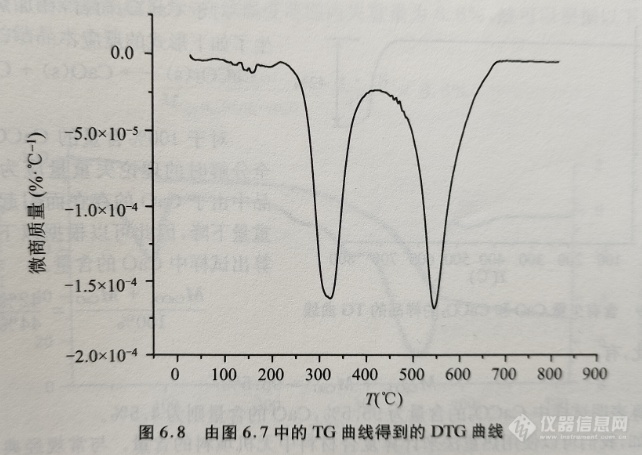
有些情况下,需要对一阶曲线(即DTG曲线)再次进行处理,所得到的曲线称为二阶热重曲线。
6.3 热重法的特点
6.3.1 定量性强
由于热重仪器的天平具有足够高的灵敏度,利用热重法可以连续地定量记录下试样随温度或时间变化而发生的微小的质量变化。因此,可以用热重法来定量地确定材料中组分的含量及一些未知物结构等,也可以根据物质热稳定性的差异对一些含量较高的多元混合物进行定量和定性分析。
例如,对于含有氧化钙和CaCO3的混合物,可以通过热重曲线计算出这两种组分的含量。图6.9为由含有少量CaO和CaCO3的样品进行热重实验所得到的TG曲线,由图可以看出试样在650~750℃范围内表现出一个明显的质量损失过程,失重量为42%。
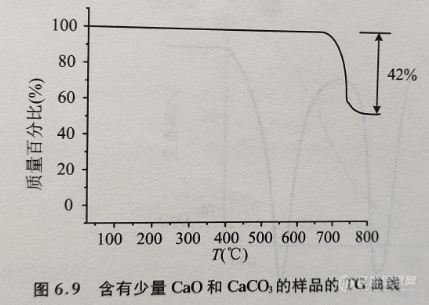
对于CaCO3而言,在加热过程中发生了如下形式的反应:
对于100%含量的CaCO3,在其完全分解时的理论失重量应为44%。样品中由于CaO的存在而引起CO2的失重量下降,因此可以根据以下比例式计算出试样中CaO的含量。
因此,有
以上计算表明试样中CaCO3的含量为95.5%,CaO的含量则为4.5%。
再如,我们可以使用热重法来计算复合材料中无机填料的含量。与常规经典的质量分析方法比较,用热重法研究高分子材料的组成的方法简便、快速、准确。通过一条TG曲线即可得到高分子材料的各种组成成分,而经典的质量分析法复杂且耗时。
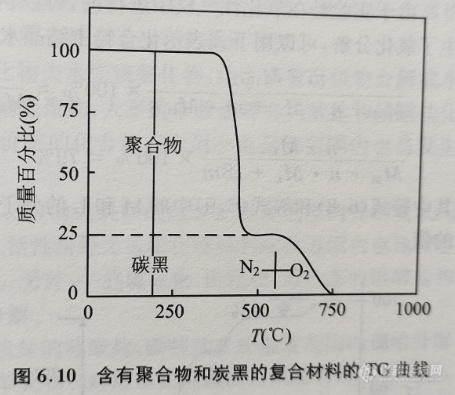
图6.10为一种含有聚合物和炭黑的塑料制品的TG曲线。在实验条件的选择上,通常先在惰性气氛环境中测定聚合物含量,然后再在氧化性的气氛环境中测定炭黑的含量。在这样的实验条件下, 聚合物和其他挥发组分在合适的温度下会发生挥发和分解, 稳定性比较高的无机物通常会在较高的温度下分解或者继续保持稳定。对于炭黑,在550℃以上时,如果有氧气分子存在,则会快速发生氧化而形成一氧化碳或者二氧化碳。这样可以通过在不同温度范围下由于聚合物分解和炭黑氧化引起的失重量的变化来分别确定相应组分的含量。对于一些结构复杂的聚合物(如结构中含有杂环或者芳香环),在惰性气氛下随着温度的升高,会在300℃以上逐渐形成比较稳定的碳化物。而在这种情况下,如果在550℃以上切换成氧化性气氛,则会使试样中由聚合物发生热裂解形成的炭和炭黑同时发生氧化分解。对于这种类型的样品体系而言,则需要分别进行惰性气氛和氧化性气氛下的热重实验。在氧化性气氛下,聚合物在较低的温度下裂解形成的炭会在比较低的温度下氧化分解,而炭黑则会在较高的温度下发生氧化分解。
另外,使用热重法可以与其他常用的表征手段如红外光谱法、质谱法、气相色谱-质谱联用法相结合来确定化合物的结构式。例如,对于一个含有结晶水的未知化合物,通过在其他分析手段确定其结构式和分子量后,可以使用热重法来确定其结晶水的个数。图6.11为一种药物巴洛沙星(分子式:C20H24FN3O4·nH2O,分子量为425)的TG曲线。由图可见,在加热过程中,在60~150℃会失去结晶水。图中的热重曲线显示,在该温度范围内失重量为8.6%,故可以根据以下关系式计算该药物的结晶水个数:
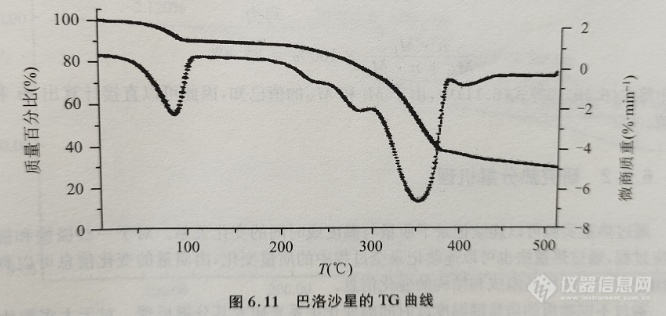
求解以上方式程式(6.7),可以得到n值为2.03,因此,可以确定该化合物中结晶水的个数为2。
另外,还可以用热重法来确定金属有机化合物的配体的个数和结晶水的含量。假设有一种配体个数(假设为n)和结晶水个数(假设为 m)未知的配位化合物(用M·Ln·mH2O表示),现通过热重实验来确定其配体个数n和结晶水个数m。实验条件为空气气氛,加热速率为10℃·min-1,实验温度为25~800℃。实验所得的热重曲线如图6.12所示。由图可见,试样在100~180℃内出现一个失重过程,失重量为11%,在290~600℃内出现3个连续的失重过程,失重量为79%。
由于实验是在氧化性气氛中进行的,可以认为配合物中的绝大多数的有机配体已经发生了氧化分解,可以用下式表示化合物中结晶水和配体的含量:
其中等式(6.8)和等式(6.9)中的M和L的分子量已知,可以通过联立以上二式确定m和n的值。
在以上实例中,我们还可以直接通过配体的含量来确定配体的个数,通过配体的个数确定结晶水的含量,具体方法如下:
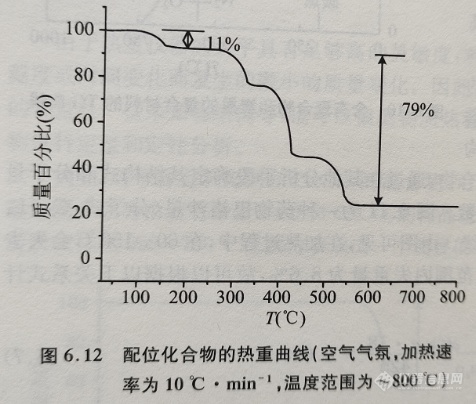
图6.12中,试样在290~500℃内出现了79%的失重,假设试样中不含结晶水,则配体的含量应该为
因此,配体含量的表达式可以改写为
其中等式(6.10)和等式(6.11)中,由于ML和MM的值已知,因此可以直接计算出m和n的数值。
6.3.2 研究热分解机理
通过热重实验可以连续记录下质量与温度或时间的变化关系。对于一些极快和极慢的反应过程,通过热重法也可以连续记录全过程中的质量变化,由质量的变化信息可以判断各个阶段所对应的样品组成和结构的变化信息。
通过不同物质的质量随温度或时间的变化关系来研究其分解机理。对于大多数物质而言,当质量发生变化时,其组成中的一些溶剂分子会发生气化。随着温度的升高,其结构中的一些不稳定部分也会发生气化以气体形式逸出,直至最终完全分解或分解成最稳定的结构形式。通过热重仪可以实时记录下这些气化过程所伴随的质量变化,我们也可以通过得到的热重曲线了解物质的热分解过程,进一步讨论其热分解机理。
一般来说,物质在不同温度范围内的质量变化主要对应于以下几个过程:
(1)25(室温)~120℃:物质在合成或保存过程中吸附的水分,有机溶剂等小分子的气体过程;
(2)80~300℃:对应于物质本身含有的结晶水、羟基化合物的脱水、一些分子量较大的有机物的不稳定基团的分解,以及一些较高沸点的有机物的气化等过程。此外,一些高价(二价以上)的无机碳酸氢盐、碱式碳酸基的分解也通常发生在该温度范围。
(3)200~550℃:大多数无机盐、氢氧化物失水变成氧化物,绝大多数有机物分解成小分子,大多数聚合物分解成单体或其他短键的低聚物,大多数草酸盐等有机酸盐和硝酸盐化合物也在此温度范围内分解。此外,一些低价态的化合物或金属在此温度范围内也易发生氧化过程。
(4)500~900℃:大多数高价态(二价以上)的无机碳酸盐在此温度范围内分解变成无机氧化物,一些有机大分子化合物的炭化物、活性炭等无机碳化物材料在此范围内也比较容易在氧化性气氛中氧化分解为CO2或H2O。另外,一些硫化物、硒化物、低价态的碳酸盐和磺酸盐化合物也通常在此温度范围内发生分解。
(5)800~1500℃:大多数高价态的无机盐的硫酸盐、磷酸盐在此温度范围内开始分解成相应的氧化物和二氧化硫,大多数低价态氧化物和硅酸基在该温度范围也容易发生熔融,一些无机复合氧化物在此温度范围内通常会相互作用形成新的化合物。另外,一些高价态的化合物在此温度范围内会发生分解变成低价化合物,如Co的氧化物的变化。
需要特别指出的是,以上不同温度范围内可能发生的一些过程主要是针对大多数化合物而言,一些特殊的化合物的分解温度可能会低于或高于此温度范围,在分析相应的温度范围内的过程时应特别注意。
下面结合TG曲线来分析乙酰氨基苯酚新型偶氮染料的热分解过程。图6.13为邻苯基偶氮(C14 H13N3O2)化合物的热重曲线。
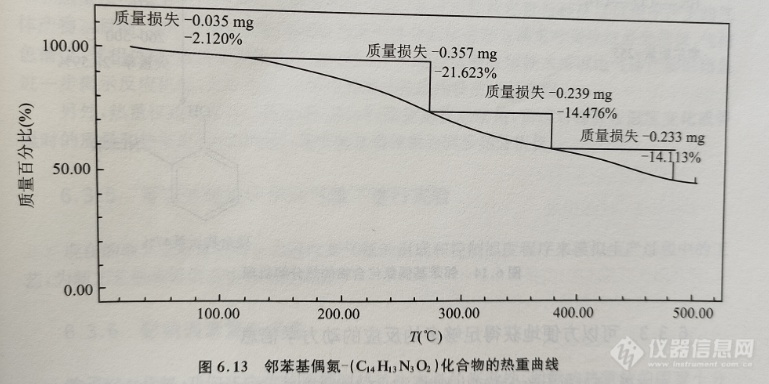
由图可见:
(1)化合物在室温25~100℃有一个较弱的失重台阶,该过程对应于样品中溶剂的气化过程,其失重量为2.1%;
(2)化合物在100~260℃有一个较为明显的失重台阶,其失重量为21.6%;
(3)化合物在260~380℃的失重台阶的失重量为14.5%;
(4)化合物在380~500℃的失重台阶的失重量为14.1%;
(5)当温度为500℃时,剩余的质量为47.7%。
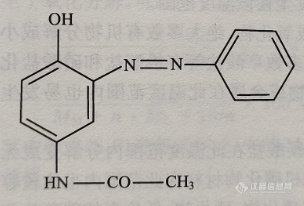
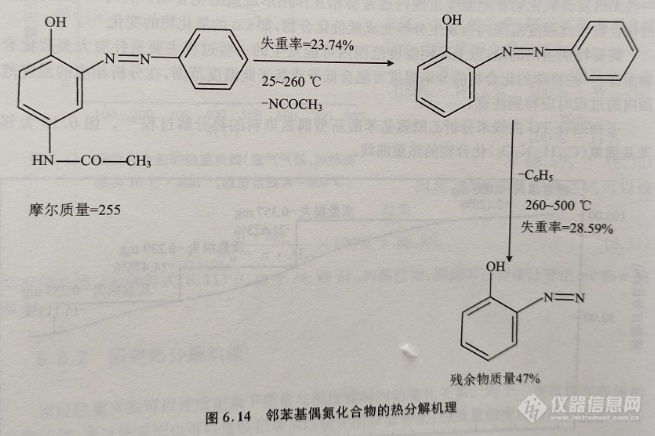
邻苯基偶氮(C14H13N3O2)化合物的结构式如左图所示。结合图6.13中的不同分解阶段可以推测,该化合物的结构在温度变化过程中发生了如图6.14所示的结构变化过程。
图6.14中的机理图表明,在该化合物发生分解时首先失去一分子的分子乙酰氨胺基片断,该过程对应于260℃以下的失重量,为23.7%,与理论值一致;随着温度的进一步升高,在260~500℃连续发生两步失重过程,该过程对应于分子中的苯环的脱去过程,失重量为28.6%,与理论值也一致;当温度为500℃时,最终产物为邻偶氮苯酚,其在结构中所占的重量百分比为47%,与TG曲线中残余物质量(47.7%)一致。
6.3.3 可以方便地获得足够多的反应的动力学信息
一般来说,通过热力学分析可以判断一个反应能否发生,而对于一个反应在进行时的速率、反应物减少和生成物增加、催化剂等对反应速率的影响以及寿命预测等问题,则需要用动力学方法进行研究。由于反应本身的复杂性,到目前为止,许多动力学理论不如热力学完善。由于热重实验的主要研究对象是固体或液体试样的质量随温度或时间的变化过程,在温度或时间发生变化的过程中,大多数反应由于有新物质生成(包括气体逸出)而导致这些反应是非均相反应,而这些现象加大了动力学分析的难度。另外,对于非等温实验,温度的变化又使非均相反应的动力学分析变得更加困难。
在本书第4章中,介绍了等温和非等温动力学相关的内容,因此与此相关的理论和背景知识在本部分不再做重复介绍。
对热重实验得到的曲线进行动力学分析是当前热分析动力学中的主要内容。概括来说主要有以下几个优点:
(1)实验需要的样品量较少。一般每次实验只需要几毫克或十几毫克的试样,对于一些不同温度下的等温实验和不同加热速率下的热重实验而言,每次实验所用的试样状态(包括粒径、形状等)和试样量应尽可能一致,以免由于试样本身的差异引起曲线的变形,从而影响动力学分析结果。
(2)可以得到某一反应从开始至结束的整个过程的动力学参数。
(3)耗时较短,操作方便。一般一组实验(按4~5条曲线计算)需要十几个小时,且重复性和规律性一般较好。
但是,热重法研究动力学过程也有它本身的一些不足,如影响热重实验的因素很多,使用不同的实验条件得到的动力学参数往往有很大的差别。此外在进行动力学分析时,采用不同的动力学模型也会得到不同的分析结果。除了可以通过热重曲线得到不同温度或时间下的反应速率外,还可以由TG曲线通过多种动力学模型来得到反应的动力学参数(活化能、指前因子、机理函数等)。
6.3.4可以方便地与其他分析技术联用
热重仪可以方便地与其他气体分析仪联用,实时定性和定量分析反应过程中产生的气体产物。目前,常用的可以与热重法联用的气体分析仪主要有傅里叶变换红外光谱仪、气相色谱仪、气相色谱-质谱联用仪和质谱仪等。通过这种联用技术可以由气体产物的信息进一步揭示反应机理,在本书第10章中将对这些联用技术进行介绍。
另外,热重仪还可以与差热分析、差示扫描量热技术联用,实现对物质在温度变化或等温时的质量和热效应的同时测量,通常称这类仪器为同步热分析仪。
6.3.5可以方便地在不同气氛下进行实验
现在的商品化热重仪可以通过改变气氛的组成和控制温度程序来模拟生产过程中的工艺,为新工艺研究提供直接的实验证据。
6.3.6 影响因素复杂多变
除了以上优势, 我们还应清楚地看到热重法本身的复杂性, 即影响热重法的因素十分多,主要包括仪器因素、实验条件因素、人为因素等,在分析热重实验数据时一定要清楚这些因素对数据的影响程度。
6.3.7 应用领域广泛
基于以上所列出的主要特点,热重法当前已在大多数的材料科学相关领域获得了广泛的应用。热重法是所有热分析技术中应用最多、最广泛的一种技术。
热重法经过将近一百年的发展,目前已经广泛应用于物理、化学、材料、生物、医学、食品、矿物、冶金、化工等材料相关的科学领域。
6.4 热重仪
6.4.1 工作原理
顾名思义,热重分析仪(通常简称为热重仪或TG仪)是在程序控制温度和一定气氛下,测量试样的质量随温度或时间连续变化关系的仪器, 它把加热炉与天平结合起来进行质量与温度测量。测试时,将装有试样的坩埚置于与热重仪的质量测量装置相连的试样支持器中,在预先设定的程序控制温度和一定气氛下对试样进行测试,通过质量测量系统实时测定试样的质量随温度或时间的变化情况。
热重仪常用的质量测量方式主要有变位法和零位法两种,变位法是根据天平梁倾斜度与质量变化成比例的关系,用差动变压器等检知倾斜度,并自动记录所得到的质量随温度或时间的变化,从而得到TG曲线。零位法是采用差动变压器法、光学法测定天平梁的倾斜度,通过调整安装在天平系统和磁场中线圈的电流,使线圈转动恢复天平梁的倾斜。由于线圈转动所施加的力与质量变化成比例,该力与线圈中的电流成比例,所以通过测量并记录电流的变化,即可得到质量随温度或时间变化的曲线。
6.4.2 仪器组成及结构
6.4.2.1 仪器组成
热重仪主要由仪器主机(主要包括程序温度控制系统、炉体、支持器组件、气氛控制系统、样品温度测量系统、质量测量系统等部分)、仪器辅助设备(主要包括自动进样器、压力控制装置、光照、冷却装置等)、仪器控制和数据采集及处理各部分组成。
6.4.2.2 仪器结构
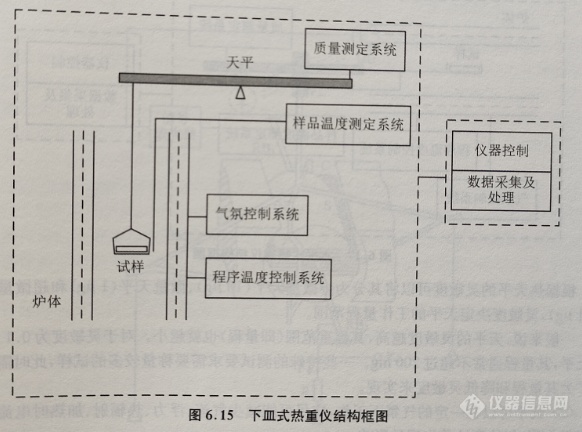
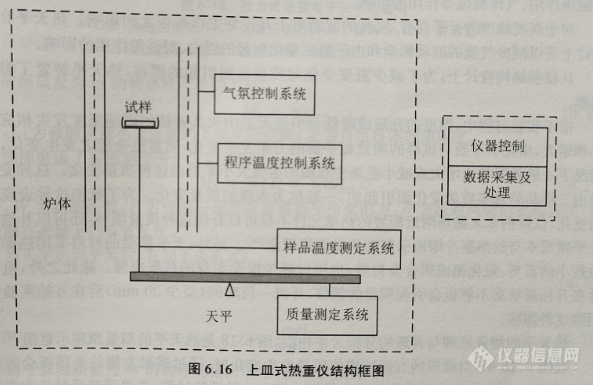
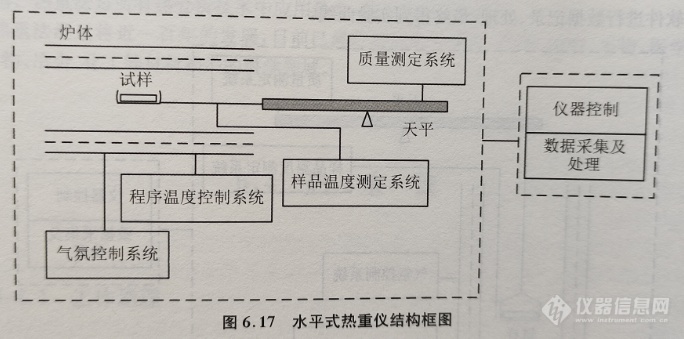
按试样与天平刀线之间的相对位置划分,常用的热重仪有下皿式、上皿式和水平式三种,这三种结构类型的仪器的结构框图如图6.15~6.17所示。
由图6.15~图6.17可见,质量检测单元的天平与常规的分析天平不同。这种天平的横梁的一端或两端置于气氛控制的加热炉中, 通常称为热天平(thermobalance), 热天平可以记录试样的质量随温度或时间的连续变化过程。温度的变化可通过程序控制温度的加热炉实现,试样周围的温度变化通常用热电偶实时测量,以减少试样与加热炉的温度的差异。热天平和热电偶测量到的质量信号经过变换、放大、模数变换后实时采集下来,由仪器附带的专业软件进行数据记录、处理,最终得到实验曲线。
6.4.2.3 热天平系统
热天平系统是热重仪的核心部分, 该系统可以实时记录试样的质量随温度和时间的连续变化关系,热天平与普通的分析天平的主要差别在于以下几点:
(1)天平的灵敏度足够高,一般热天平的灵敏度在0.1~1.0μg。
根据热天平的灵敏度可以将其分为半微量天平(10μg),微量天平(1μg)和超微量天平(0.1μg),灵敏度决定天平的工作量程范围。
一般来说,天平的灵敏度越高,其称重范围(即量程)也就越小,对于灵敏度为0.1μg的热天平,其量程通常不超过200mg。一些特殊的测试要求需要称量较多的试样,此时需要通过扩大其量程和降低灵敏度来实现。
(2)天平可以在一定的气氛下工作,应尽可能减少气流、浮力、热辐射、加热时电流产生的磁场作用、气体腐蚀等作用的影响。
对于高灵敏度的天平而言,气流的波动对于其正常工作有很大的影响,热天平在结构设计上可以减少气流的波动影响和由于温度变化引起的浮力、对流等作用的影响。
从仪器结构设计上,为了减少温度变化对质量检测引起的漂移,热天平装置了温度补偿器。
由于实验过程中,温度的升高或降低会引起天平中永久磁体的磁场温度发生相应的减小和增大,由此会导致与试样的质量相平衡的力矩发生变化,质量也会随之发生变化,这种情况下一般需要相应增大或减小磁场中线圈的电流大小来抵消这种质量变化。这种变化不是由于样品的真实质量变化而引起的,一般称为表现的质量变化。为了抵消这种表现的质量变化,仪器的永久磁场附近配置的热敏元件不仅可以补偿这种质量漂移,还可以补偿由于天平横梁本身的热胀冷缩而引起的质量漂移现象。另外,天平横梁的材料采用热膨胀系数较小的石英、氧化铝或铝合金材料,也可以减少横梁本身的热胀冷缩。除此之外,电子器件在开拓后状态不够也会引起质量的漂移,开机一段时间(至少30min)后在开始实验可以消除这种漂移。
热天平的测量原理与普通的分析天平相似,图6.18是热天平的测量原理示意图。
在图6.18中,当横梁的右侧试样的质量发生变化时,通过横梁左侧的光挡板会发生偏移,光挡板一侧的光电位移检测器可以灵敏地记录这种漂移过程,并将漂移量转换为电压号(直流电压或电流),这种电压号正比于质量信号,可以通过质量校准转换为试样的质量。
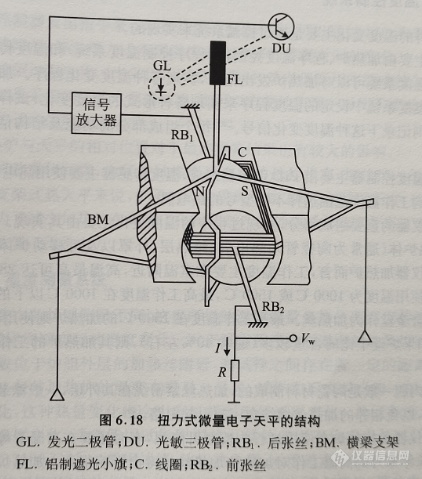
实验时,当加一质量为m的物怀在秤盘左边时,天平横梁支架连同扁形张丝、线圈和铝制遮光小旗一起逆时针转动。此时光敏三极管所受到光源的照射强度大,内阻减小;放大器就有输出电压,其输出电流流进后张丝到线圈,再流出前张丝经电阻到地,线圈中的电流在永久磁场下将受力而产生一个顺时针的力矩,来克服质量为m的物体所产生的力矩,而达到平衡。
被测质量为m的物体所产生的力矩:
式中,L1为被测质量与支点间的下垂平行距离;g为自由落体的加速度
线圈电流I在磁场中所产生的力矩为
式中,W为线圈数,F为线圈一根导线在磁场中所受的力,B为线圈所处的磁通密度,L2为线圈在磁场下的有效长度。
当天平达到平衡时,有如下关系式;
因此
对于被测质量为m的物体的输出电压,有以下关系式:
其中
6.4.2.4 温度控制系统
热重实验时的温度变化主要是通过控温系统来实现的。
控温系统主要由加热炉、程序温度控制器(程序控制温度系统)和温度传感器几部分组成。程序控制温度系统可以对加热炉发出指令,实现各种温度变化程序。加热炉的功能是按照程序控制温度系统中设定的温度程序来实现各种形式的温度变化, 试样周围的温度传感器(热电偶)则记录下这种温度变化信号。每个组成部分的功能及结构信息参见本书第5章。
程序控制温度控制器主要由PID调节器组成,温度传感器主要使用热电偶来实现,热重仪需根据仪器的工作温度范围选择不同型号的热电偶。
加热炉是仪器的重要组成部分,实现过程中的温度变化主要由其实现。加热炉主要由加热元件、耐热炉体(通常为陶瓷管)、热电偶、绝热层、外罩以及可移动炉体的机械部分组成。对于热重仪器加热炉而言,工作温度主要在室温附近,高温最高可达2800℃。大多数热重仪的最高使用温度为1000℃或1500℃,最高工作温度在1000℃以下的加热炉可以使用康铜或镍铬合金丝作为加热丝。最高工作温度在1500℃的加热炉则使用铂或铂-铑合金丝作为炉丝,如果炉丝中铑的含量较多(通常40%左右),则其加热炉的工作温度最高可达1750℃。
加热炉的内胆一般是陶瓷材料制成的,加热丝紧密绕在其外层,一般涂装一层陶瓷浆料来固定加热丝,以免相邻的加热丝缠结在一起引起短路。
由于热重仪器的加热炉在使用过程中反复升降温,有时还要在高温下等温工作相当长的时间,这种长年累月的高温工作对加热炉加热丝的寿命影响很大。加热炉的寿命是必须要面对的具体问题。一般的加热炉可以使用5~8年,具体的寿命与加工工艺和仪器的使用频率有关。对于1500℃高温炉来说,当加热温度超过1200℃时,尽量不要采用较慢的加热速率和较长的等温时间,这种超高温的实验对加热炉的使用寿命影响很大。
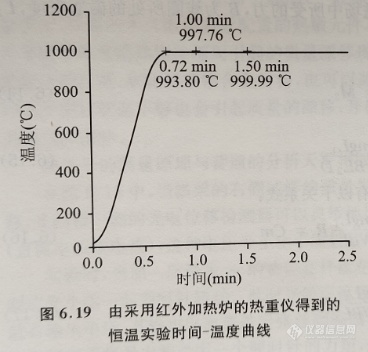
此外,加热炉的体积对控温有较大的影响。一般来说,较小体积的加热炉升/降温速率快, 但控温效果差, 恒温实验时温度的波动较大。而体积较大的加热炉加热恒温时温度起伏小,但加热速率较慢。对于非室温温度下的恒温实验来说,除了要求恒温阶段温度的波动小之外, 为了防止试样在加热阶段发生反应,还要求从实验开始的温度到指定温度的时间越短越好,即加热速率尽可能快。这对于传统的加热方式来说,是一个很难得到完美解决的难题。红外线加热炉可以使这个问题得到较好的解决,这种加热炉高温一般可以达到1200℃,瞬间加热速率超过2000℃,线性可控加热速率为500℃·min-1。通过红外加热可以在一两分钟之内达到指定的温度,适用于恒温实验和超快加热速率下的热分解实验研究。图6.19为利用红外加热炉进行恒温实验时的时间-温度曲线。由图可见,在当加热速率高于500℃·min-1时,加热炉仍然不存在热惯性现象,可以实现很好的恒温效果。
炉温程序控制器发出指令来控制加热炉的温度变化,可以通过PID参数的调节使炉子按照设定的加热降温、等温等方式实现温度变化速率和等温时间的变化。一般通过一对或两对热电偶来控制炉温变化。当采用一对热电偶时,热电偶既用来驱动控制系统又用来记录温度变化。如果采用两对热电偶来控温,则可以方便地实现一对用于驱动控制系统,另外一对用于测量炉子的温度变化情况。
另外,加热炉与天平的相对位置对于最终实验结果也有较大的影响。
对于吊篮式热重仪而言,为了使试样保持自由的悬挂状态,加热炉一般位于天平的下方。对于有梁支架式热天平来说,炉子可以位于天平的上部,也可以下方,还可以位于天平的一侧。通常为了减少加热炉在高温工作时辐射产生的热量影响天平的工作状态,一般情况下应将炉子放置于天平上方。
6.4.2.5 温度测量系统
与控温系统中的炉温测量不同,这里所指的温度测量是指使用温度传感器(通常为热电偶)来测量试样周围实际的温度变化。对于可以程序控制温度的加热炉而言,由于加热炉的热电偶一般位于炉胆外层的加热丝附近,和试样之间存在着一定的距离,因此试样周围的温度变化一般与加热炉的温度有差异,另外,试样在反应时自身一般会有因吸热或放热的热量变化,这种热量变化也会引起试样周围的温度变化。为了如实地反映试样在实验过程中的温度变化,通常使用试样周围热电偶的温度变化来表示试样的温度变化。当工作温度低于1100℃时,一般用镍铬-镍铝热电偶;对于最高工作温度为1500~1600℃的热重仪,通常使用铂-铂铑热电偶。当温度超出此温度时,通常用钨-铼热电偶来测量温度变化。
由于测量实验温度的热电偶与试样距离很近或直接接触,在选用热电偶时应考虑以下几个主要原则:
(1)热电偶所用的材料必须是惰性的,不能与试样或试样的分解产物发生任何反应,以防污染热电偶、降低其测温精度。
(2)热电偶的热电势与温度的关系在工作的温度范围内应保持线性关系。
如果热电偶与样品的相对位置发生变化,将会给温度的测量结果带来较大的影响。一般来说,热电偶与样品的相对位置应保持恒定;实验中如果热电偶的位置发生了变化,应对仪器及时进行温度校正。
需要特别指出的是,由于热电偶在高温下工作时间过长,并且经常与等温的分解产物接触,其状态会发生变化,需要定期对热电偶进行温度校准,以保证其温度测量的准确性。
热重仪器的温度校准方法将在接下来的内容中进行介绍,在此不做赘述。
6.4.2.6 气氛控制系统
热重实验时,试样周围的气氛对于热重曲线有着非常大的影响,在分析实验结果和制订实验方案时必须充分考虑实验气氛的影响。由于本书将在热重实验影响因素部分详细阐述气氛对实验曲线的影响,因此在本节中只讨论热重仪的气氛控制系统的作用。
除了早期的商品化热重仪没有气氛控制器外,现在几乎所有的热重仪器都配有气氛控制系统。进行热重实验时,气氛主要有以下作用:
(1)气氛可以将试样发生质量变化时的气体产物及时带离反应体系,有利于反应的进一步进行;对于一些有毒或腐蚀性的气体产物,气氛可以及时将这些产物带离仪器的检测系统,有利于保护仪器样品的支架和天平系统。
(2)对于一些易发生氧化的试样,使用惰性的气氛可以对试样起到保护的作用。
(3)可以通过实验气氛的变化来研究试样的一些反应特性,如可以通过改变气氛的组成来研究物质的氧化、还原、加成等反应过程中的质量的变化,有利于实现更加真实的反应过程。
(4)对于与热重仪联用的一些分析技术,如有气体逸出,气氛可以及时将分解产物带到气体分析仪中,以实现实时分析反应时生成的气体产物。
(5)可以通过改变气氛的压力实现一些特殊实验条件下的热重实验,这些特殊条件主要包括真空和高压等类型的实验。气氛的流量一般由流量控制器来控制,流量计主要有转子流量计、质量流量计(数字流量计)等类型,其中数字流量计可以记录实验过程中流量的实时变化,并可以通过软件保存下来这些变化过程。无论是数字流量计还是转子流量计,均要定期使用皂膜流量计进行校准,以免炉子出口由于分解产物的冷凝造成堵塞而引起流量下降。在使用一些危险性的气体(如H2、CH4、CO等)做实验气氛时,必须仔细检查气路和仪器的密封性,以免由于气路泄漏而引起爆炸或中毒事故的发生。
气氛在不同结构的热重仪内部的流动方式不同,共同之处在于气氛在仪器内部流动的方向一般是先经过气氛控制器、天平室,然后到加热炉,最后将气态分解产物经炉子出口带离炉体。现在的商品化仪器一般可以实现同时使两路以上的气体进入加热炉。大多数仪器的天平室还设计了独立的保护气路系统,以有效避免分解产物进入天平室而引起污染。当使用两种组分以上的混合物气体作为气氛时,应在仪器外部或前端先将气体经稳压后充分混合。然后,保持流量稳定地输出,经截止阀输入到测量室。一般不应简单地将两种不同流速的气体通过各自独立气体路在加热炉内进行混合,这样混合的效果通常比较差,也无法有效保证实验结果的重复性。当使用一些危险气体时,局部浓度过高容易引起爆炸事故。通常的做法是直接使用已经充分混合物的气体的标准气体钢瓶作为气源,
热重仪在真空条件下的实验主要通过将加热炉口与时机械泵或扩散泵相连接来实现。一般来说,单独使用机械泵可以获得较低的真空,而如果将机械泵与扩散泵配合使用到可以实现高真空。为了防止在抽真空的过程中粉末状试样发生飞溅现象,一般在机械泵、扩散泵和测量室(即原样品室)之间(通常在炉子出口附近)配置一个直径较大的管道,这两个管道上分别安装蝶阀和真空微调阀,在抽真空时,使支管道与机械泵相通。由于抽气速率较低,可以有效地避免试样发生飞溅。当达到机械泵极限值时再打开主管道使真空继续下降,从而可以实现在真空条件下的热重实验。
6.4.2.7 仪器控制和数据采集及处理
在实验过程中,待测物理量的原始信号首先经过传感器或相应的电路单元转换为电压模拟信号,然后再通过模数转换器将这些模拟信号(通常为电信号)转换成数字信号。
较早的商品化仪器的模/数转换是通过安装在计算机上的数据采集卡或专用的数据采集装置来实现的,现在通用的商品化热重仪大多采用RS232通信口、USB接口或网线接口来实现与仪器的通信。具体方式是首先将热重仪工作时的温度、质量、流速等实时信息通过单片机(即微处理机)与计算机相应的接口(如RS232串口、USB接口、网线接口等)进行通信,把数据传送到计算机存储系统。同时,也可以将试样信息、实验程序等信息由计算机的控制软件发送至仪器的程序温度控制系统、气氛控制系统等单元。可以用仪器的分析软件实时显示实验时的数据,并可在实验结束后对数据进行分析、计算和导出等操作。
实验时数据的采集频率通常是每一秒钟采集1个数据点。对于一些反应速率较快的反应来说,应该提高采点频率,一些仪器的软件中最高可以设置为一秒钟采集200个数据点。对于一些反应速率较慢的反应而言,其采点间隔可以适当加大。一般来说,采点间隔越大,得到的实验曲线越平滑。但过大的实验间隔有时会遗漏一些实验的中间过程,造成实验曲线变形。而较高的采点频率通常会导致实验曲线的噪声比较大,会给分析某些特征变化值一些困难。
6.4.3 热重仪的校准
由于热重仪测量的是试样的质量与温度或时间的变化关系,在仪器的使用过程中应定期使用相应的校准方法或规范对仪器的质量和温度进行校准或标定。另外,对于一些对实验气氛要求比较高的实验来说,还需要对仪器的气氛的流速进行校准。
6.4.3.1 热重仪的质量校准
与常规的分析天平的质量校准不同,由于热天平具有较高的灵敏度(灵敏度在微克量仪),因此在校准时使用的微克级别的砝码无法方便地获得。实际上,由于热重实验用的试样量一般在几毫克至几十毫克不等,大多数热天平的质量校准通常使用10mg或100mg的标准的砝码来标定天平的称量质量。通常的做法是:将一只已知质量的标准砝码放在天平的样品盘上,确定天平显示的质量与标准值是否一致。如有差异,通过仪器附带的软件或在仪器的显示面板上修改相关的设置、使显示的质量的数值与标准值一致。
对于一台灵敏度较高的热天平而言,在较长的时间内的质量漂移程度也是评价仪器性能好坏的一个重要的指标。在正式实验开始之前,必须对这种表观质量变化进行校正,通常的做法是:
(1)将不加试样的空的坩埚放置在相应的支架上,设定温度程序和气氛流速等条件,运行实验。由该实验得到的热重曲线为空白基线。需要注意,空白实验的温度程序、气氛流速、坩埚类型等条件应与正常实验一致。理论上,如果在正常实验时以上的操作条件发生了变化,应该再进行相应的空白实验操作。
(2)根据仪器的校准程序,在分析软件中打开空白曲线(正常实验模式下,由空白坩埚得出的实验曲线),标出不同温度下的质量变化,按照软件设置将此空白曲线调入至仪器的校准方法文件中,在之后的实验中将对这些质量漂移自动进行校准。对于一些质量变化较小的过程,有时还要对质量进行二次校准。即在完成以上质量校准操作后,在正常的实验模式下,在正式实验开始前,先用空白坩埚获得一条空白实验曲线,之后用相同的条件向空白坩埚中加入试样后开始实验获得试样的热重曲线,最后在分析软件中用试样的曲线与空白曲线相减,得到的曲线即为二次校正后的热重曲线。一般来说,通过这种校正方法所得到的热重曲线的质量漂移现象会减弱很多,但这种方法比较繁琐。另外,当仪器的状态发生了变化时,若再扣除空白曲线则容易引起热重曲线的变形。
有时还会采用已知分解过程的高纯化合物的质量变化来标定天平称量的准确度。
6.4.3.2 热重仪的温度校准
对于下皿式热重仪,热重仪的测湿热电偶不与试样直接接触,与试样有一定的距离。当炉体的温度发生变化时,不可避免地会在试样周围产生温度滞后。当在实验过程中试样发生了较大的放热或吸热效应时, 试样和热电偶之间的温度差将会变得十分明显。通常情况下,将热电偶放置在装有试样的支持器的下方1~2mm处。如果将热电偶放置在装有试样的支持器的上方,则在加热过程中产生的气体产物可能会污染热电偶。
通常采用以下几种方法对热重仪进行温度校正:
1.居里点法
在基于磁性标准物质的校准方法中,通常使用具有确定的居里温度(Curie temperature)值Te的纯金属或合金作为标准物质。该方法最初被用于由美国珀金埃尔默(Perkin-Elmer)公司开发的小型加热炉温度的校准中,由于加热炉中均匀加热区的尺寸有限,因此十分有必要对其进行精确的校准。尽管在早期的研究中使用的磁性材料是由Perkin-Elmer公司提供的,然而,经过几十年时间的发展,目前该方法已广泛用于热重仪的温度校准和数据处理中。该校准过程其实就是磁性温度的测量,其中磁效应的外推终止点即为Tc的数值。图6.20为使用几种磁性标准物质进行校准得到的TG曲线,由此可见,TG曲线和DTG曲线都可以使用该方法进行温度校准。通过这种方法可以方便地在单次实验中测量多个磁性样品的转变过程。
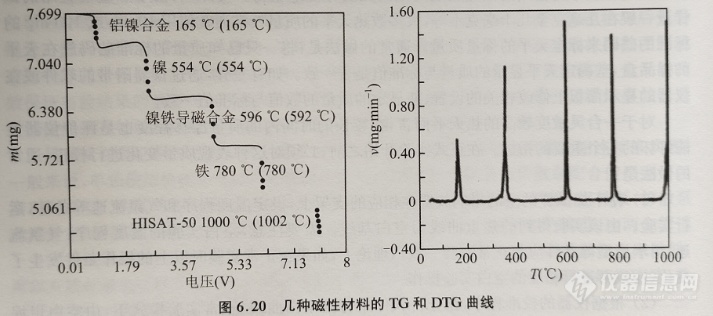
在磁场的作用下,当将铁磁性材料加热到某一温度时,其导磁性能很快完全消失,通常称此处所对应的温度为铁磁性材料的居里温度。居里点温度只与材料的组分有关,当材料的组分保持不变时,居里温度也不会发生改变。
校正时,将铁磁性材料放在天平的试样坩埚内,并在炉体外侧的试样位置处放置一块永久磁铁。由于磁场的作用,此铁磁性材料产生一个向下的力,位于试样上方的天平发生增重。当炉子升温到该铁磁性材料的居里温度时,铁磁性材料快速失去永久磁铁对它的向下拉力,表现为失重过程。实验结束后,在分析软件中根据曲线的拐点来确定居里温度(见图6.21)。
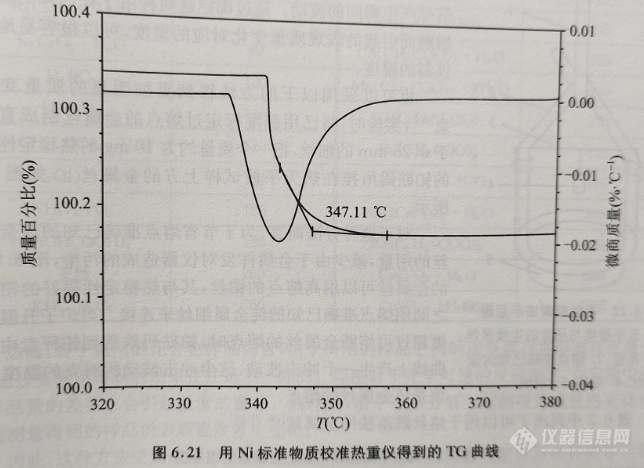
当使用已知居里温度的铁磁性材料所得到的测试结果与标准值不一致时,应在仪器的控制软件或者控制面板中进行校正。
在校正热重仪的温度时,应注意:
(1)应选择居里温度接近试样测试温度的材料;
(2)升温速率应与测试条件保持一致,一般为10~40℃·min-1;
(3)实验时的试样量应适中,不宜太小,否则曲线不明显;
(4)温度读数为TG曲线的台阶的最大斜率与台阶结束后基线外延线的交点所对应的温度(见图20)。
表6.1中列出了可用于热重仪的温度校准的磁性材料。
表6.1 可用于热重仪的温度校准的磁性材料
磁性材料名称 | 转变温度(℃) | 磁性材料名称 | 转变温度(℃) |
蒙乃尔合金 | 65 | 深拉镍铬合金 | 438 |
阿卢梅尔镍铝锰电阻合金 | 163 | 磁渗透合金 | 596 |
镍 | 354 | 铁 | 780 |
穆镍铁坡莫合金 | 393 | 海沙特50 | 1000 |
2.吊丝熔断法
吊丝熔断法通过将熔点准确已知的纯金属细丝固定悬挂在样品支撑系统附近非常接近样品的位置上,当温度升高至纯金属细丝的熔点时,金属丝发生熔化并从其支撑件滴落。对于这种方法而言,样品具体放置的位置很重要,滴落时的质量可能会减小并造成突然的质量损失。金属丝也可能会滴落在样品盘上,导致检测到的质量信号产生瞬间的波动。通过确定这两种由于在已知的温度下熔融而引起的表观质量变化对应的温度,可以很容易地校准仪器的温度。
也可以采用以下的方法得到更加明显的质量变化信息:实验时,将已用温度标定过熔点的金属丝制成直径小于0.25 mm 的细丝,把一个质量约为10 mg 的热稳定性很高的铂砝码吊挂在热天平放试样上方的金属丝上,如图6.22所示。
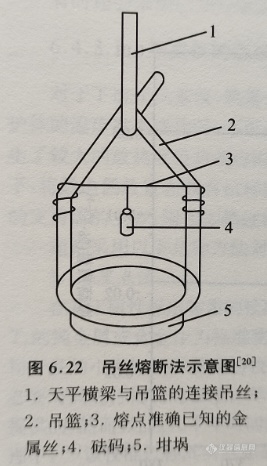
对于这种方法而言,为了节省熔点准确已知的纯金属细丝的用量,减少由于金属挥发对仪器造成的污染,图6.22中的金属丝可以用高熔点的铂丝,其与热稳定性很好的铂砝码之间用熔点准确已知的纯金属细丝来连接。当炉子升温到温度超过可熔断金属丝的熔点时,铂砝码跌落到铂秤盘内,TG曲线上产生一个冲击波动,这个冲击波动所对立的温度就该是该金属丝的熔点。
表6.2中列出了可以用于熔丝跌落法的金属丝。
表6.2 可用于熔丝跌落法的金属丝的温度值
材料 | 观测温度(℃) | 校正温度(℃) | 文献值θ(℃) | 与文献值的偏差θ(℃) | 材料 | 观测温度(℃) | 校正温度(℃) | 文献值θ(℃) | 与文献值的偏差θ(℃) | |
铟 | 159.90±0.97 | 154.2 | 156.63 | -2.43 | 铝 | 652.23±1.32 | 659.09 | 660.37 | -1.28 | |
铅 | 333.02±0.91 | 331.05 | 327.50 | 3.55 | 银 | 945.90±0.52 | 960.25 | 961.93 | -1.68 | |
锌 | 418.78±1.08 | 419.68 | 419.58 | 0.10 | 金 | 1048±0.87 | 1065.67 | 1064.43 | 1.24 | |
在用熔断铁落法校正热天平温度时,也应注意以下两点:
(1)标定金属丝的熔点选择接近试样温度的材料;
(2)升温速率一般选10~40℃·min-1。最好是被测试样的升温速率与校正时所用的升温速率相同。
3.特征分解温度法
在早期的校准工作中,相当多的研究者曾尝试使用具有明显的特征分解温度的材料对热重仪进行温度校准。通过结构已知的物质的初始分解温度来对热重仪进行温度校正。此处所指的初始分解温度为质量变化速率达到某一预先规定值之前某一时刻试样的温度,因此,所选用的标准物质应满足以下条件;
(1)在分解温度前的温度区域里应有足够的稳定性;
(2)初始分解温度应具有较好的重现性;
(3)由不同来源得到的同种标准物质,其初始分解温度应具有较小的差异。
表6.3中列出了可用于热重仪温度校正的物质。
表6.3 用于热重仪温度校正的标准物质的特征分解温度
标准物质 | 特征分解温度t(℃) | 标准物质 | 特征分解温度t(℃) |
K2C2O4·2H2O | 80 | KHC6H4(COO)2 | 245 |
K2C2O4·H2O | 90 | Cd(CH3COO)2·H2O | 350 |
H3BO3 | 100 | Mg (CH3COO)2·4H2O | 320 |
H2C2O4 | 118 | KHC6H4(COO)2 | 370 |
Cu(CH3COO)2·H2O | 120 | Ba(CH3COO)2 | 445 |
Ca(C2O4) ·H2O | 154 | Ca(C2O4) ·H2O | 476 |
NH4H2PO4 | 185 | NaHC4H4O4·H2O | 545 |
(CHOHCOOH)2 | 180 | KHC6H4(COO)2 | 565 |
蔗糖 | 205 | CaC2O4 ·H2O | 688 |
KHC4H4O6 | 260 | CuSO4·5H2O | 1055 |
然而,对于相同的化合物样品而言,由于所用的样品之间的成分或存在形态存在微小差异,通过实验所得到的结果往往是不一样的。即使对于完全可逆的反应而言,在实验中采用的样品量的差异也会引起温度的漂移。同样的,由于样品分解引起的吸热或放热变化也会引起测量得到的样品的表观温度发生变化。
因此,这种方法受到试样用量、升温速率、填装情况以及炉内气氛性质和种类等因素的影响,得到的结果经常出现重复性较差的现象,不同的仪器和不同实验室得到的结果的差异较大。现在经常用这种方法来验证经校正后的仪器的工作状态。
4.特征转变温度法
对于与差热分析或差示扫描量热法联用的热重仪而言,通常通过一些具有可逆的固↔固转变或固↔液转变的物质来进行温度校正。表6.4中列出了常用的标准物质,这种方法的特点是同一试样在炉内可以升温一降温一升温反复测定。
此外,对于水平式和上皿式结构的热重仪而言,其大多是将热重法与差热分析或差示扫描量热法联用。这类结构形式的仪器可以用已知熔融温度的标准物质通过初始熔融温度来标定仪器的温度,常用的标准物质列于表6.4中。
表6.4 可用于温度校准的标准物质的熔融温度
标准物质 | 熔融温度(℃) | 标准物质 | 熔融温度(℃) |
Hg | -36.9 | AI | 660.4 |
H2O | 0.0 | Ag | 961.9 |
C12H10O(二苯醚) | 26.9 | Au | 1064.4 |
C7H6O2(苯甲酸) | 122.4 | Cu | 1084.5 |
In | 156.6 | Ni | 1456 |
Bi | 271.4 | Co | 1494 |
Pb | 327.5 | Pd | 1554 |
Zn | 419.6 | Pt | 1772 |
Sb | 630.7 | Rh | 1963 |
Ir | 2447 |
由于高温下热辐射的影响,不同温度下测得的温度与实际的温度并非线性关系。对于温度范围较宽的实验,一般要选用几个标准物质来校准。如对于相变实验温度范围在25~1500℃的实验,一般要选用两种或两种以上的物质来校正不同的温度范围的特征温度。
曲线的峰面积通常随着温度的升高而降低。因此, 应选择熔点与所研究的反应温度范围相近的物质进行温度校正。例如,如果物质的分解温度在150℃附近发生,则应选择金属铟进行温度校正。另外,表6.4中所列的熔融温度的数值随样品的来源不同而略有差异。
6.5 热重实验过程
在经过温度、质量等一系列的校正,并达到要求之后,热重仪可以开始正式实验。一般来说,热重实验包括样品的准备、实验条件的选择、测量、数据处理等过程。在下面的内容中,将逐一介绍在这些过程中需要注意的问题。
6.5.1 样品的准备
理论上,一切非气态的试样都可以直接通过热重实验测量其质量在一定气氛和程序控制温度下随温度或时间的连续变化过程。但我们也应清醒地认识到,由不同状态的试样所得到的热重曲线的差别也很大。因此,选择合适的试样状态对得到合理的实验结果显得十分关键。
一般来说,对于不同状态的试样而言,需做一些相应的处理才可以应用于热重实验。
6.5.1.1 固体试样
对于不同状态的固体试样应采用不同的制样方式:
(1)对于粉末状的试样而言, 如果颗粒比较均匀可以直接进行实验。如果试样之间的粒径差别较大,最好经过研磨或筛分处理。另外,如果试样易吸湿或含有较多的水分或溶剂,则在实验前应进行干燥处理。
(2)对于薄膜样品而言,在实验时可以将其切割成比坩埚内径略小的圆片,将其均匀平铺到坩埚底部,以使重心在坩埚中间。不要在坩埚内任意堆积试样,这样会导致试样在分解过程中由于重心发生变化而带来表观的质量变化。
(3)对于大块的样品而言,实验时可根据需要决定块状样的粉碎程度。由于试样的粒径对其分解过程也有影响,因此,如果需要考查块状样品的热稳定性,则应将样品加工成较薄的碎片后将其铺在坩埚底部即可开始实验。如果要了解试样在粉末状态下的分解行为,则可以使用相应的粉碎技术将试样进行粉碎处理。粉碎后应进行筛分处理,使用尺寸相近的试样进行实验,这样得到的实验数据的重现性较好。
(4)对于纤维状的样品而言,应使用相应的切割工具将纤维分成小于坩埚内径的小段,实验时将小段试样平铺在坩埚底部即可。切勿将纤维试样揉成团直接加入到坩埚中,这样得到的实验曲线极易出现由于在加热过程中重心变化而带来的表观质量变化,影响实验数据的分析。
对于固态试样而言,如果试样本身是物理混合的混合物,在实验时应考虑取样的位置差异。由于在一次实验中热重实验需要的试样量很少,一般在几毫克到十几毫克之间,因此每次实验取样不一定有代表性。为了使实验数据具有较好的重复性和代表性,在取样前应将试样进行混匀,必要时还应进行平行实验,平行实验的次数一般为3~5次。
6.5.1.2 液体试样和黏稠试样
液体试样一般包括液态物质和溶液两种状态的试样。
由于液体状态的物质大部分具有较强的挥发性,因此在将试样加人到坩埚后应尽快开始实验。对于单一组分的化合物而言,试样的挥发对TG曲线的总体形状影响不大。对于多组分的化合物而言,较长时间的挥发会影响试样的组成。
浓度较低的溶液试样不宜直接进行热重实验,尤其是浓度在3%以下的溶液。由于溶剂的挥发是一个十分缓慢的过程,并且这个过程会影响溶质的热分解过程,因此,对于较低浓度的溶液而言,应在实验开始前对溶液进行浓缩或干燥处理。
黏稠状试样或凝胶试样可以直接进行实验,试样中如含有较多的溶剂,则应尽可能地把溶剂去除。这类试样在取样时应先混匀,从中间部位选取试样进行分析。另外,对于含有悬浮物的液体,在取样前应摇匀。
6.5.2 实验条件的选择
如前所述,影响热重实验条件的因素很多,除了试样状态,仪器本身因素外,实验时选用的实验条件如实验气氛、温度程序、实验容器和实验气氛等都会影响最终的实验结果。
6.5.2.1 实验气氛气体的选择
在选择热重实验的实验条件时,应根据实验目的和试样本身的性质来灵活选择。一般来说,当物质发生质量变化时,主要有汽化(挥发)、升华、分解、氧化还原/加成等反应。在以上的过程中:
①当试样发生挥发和升华时,其不会与气氛发生反应,气氛的作用是及时将汽化产物带离试样周围,以利于反应的进一步进行。
对于试样的分解过程而言,如果其在分解的过程中仅是自身的结构发生分解而未与气氛中的气体进行反应,则一般称这种分解过程为热裂解。热裂解是物体本身在温度变化时发生分解的真实体现。如果仅仅通过热重实验来考察试样在不同温度下的热分解过程或热稳定性,则一般会选用不与试样发生反应的气氛(即惰性气氛)作为实验气氛。对于大多数分解反应而言,常用的惰性气氛主要有氮气(He)、氩气或氮气。此处所指的惰性气氛是相对的,例如氮气气氛对于大多数有机物的分解是具有惰性的,而对于一些金属样品而言,其在高温下则会与氮气发生反应形成相应的氮化物,此时的氮气气氛变成了反应性的实验气氛。
从另一个角度来说,如果我们要考察试样在不同的温度下与环境中的气氛气体如氧化性气体(氧气等)、还原性气体(氢气、甲烷、一氧化碳等)或反应性气体(CO2、NO2等)发生反应的过程,试样会与气氛中的反应性气体进行反应。与自身的热裂解过程相比,氧化过程进行的速度要快得多。例如,对于结构复杂的有机物而言,在氮气气氛下,分解产物会逐步分解成性质相对稳定的炭化物。而同样的化合物在氧化性气氛的作用下,裂解形成的碳化物会继续与氧气发生氧化反应,最终氧化成结构最稳定的小分子化合物,如二氧化碳、水等物质。一般来说,对于无机/有机(或高分子)混合物、复合材料而言,可以通过有机组分在加热过程中氧化分解时的质量变化信息来判断样品中的无机化合物与有机化合物或高分子化合物的比例。
在图6.23中给出了同一化合物在氧气和空气气氛下的热重曲线,由图可以看出这两个过程有着十分显著的区别。
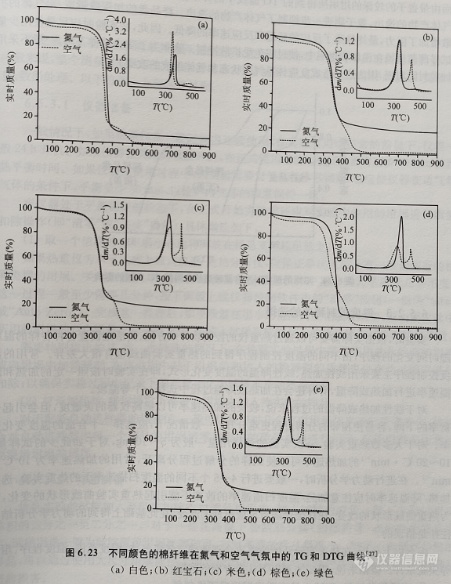
因此,在实验前一定要根据具体的实验目的来合理选择实验气氛。
无论是静态还是动态,如果气氛与试样或产物发生反应,将促进反应的进行,使反应提前。
热重实验时的气氛通常分为以下几类;
(1)惰性气氛,如He、N2、Ar;
(2)氧化性气氛,常用的是空气、强氧化气氛,如O2;
(3)还原性气氛,如H2、CO;
(4)腐蚀性气氛,如Cl2、F2等;
(5)在没有以上气氛流通时,试样在发生汽化或分解时产生的气体在试样周围形成的静态气氛;
(6)真空或控制压力。
需要指出,以上所指的氧化性、还原性以及腐蚀性气氛都是相对的。
通过比较不同气氛下的TG曲线,有助于理解试样发生的反应。例如,在空气气氛下,只含C、H、N的有机物比在氮气气氛下分解速度快,且最终残重将为零,而在氮气中C以碳的形式留下来无法分解。如果试样在氮气气氛中最终分解产物中含有金属单质,则在空气中将形成氧化物。
6.5.2.2 实验容器的选择
热重实验中用来放置试样的容器一般为坩埚。由于试样在实验过程中一般会随着温度升高而发生熔融、汽化、分解等强烈反应,这些过程的产物会与仪器的支架或吊篮发生反应而损坏仪器。为了使仪器尽可能地少受这些干扰,一般每次实验前都要将试样放置在坩埚中。坩埚的形状多种多样,用来制作坩埚的材料也多种多样,常用坩埚材料主要有铝、氧化铝、石英、不锈钢、铜、镍、铂、金等,坩埚的形状和结构也对热重实验曲线有较大的影响。
由于在实验过程中的坩埚只是起到实验容器作用,因此,坩埚在实验过程中不能与试样或分解产物发生任何作用,应根据试样和分解产物的信息来灵活选择合适的坩埚材料,同时还应注意所用坩埚的最高使用温度。
合理选择实验坩埚对能否得到真实的分解过程曲线十分关键。对于无论是试样受热分解出气体的还是试样与周围气体相互作用的反应而言,反应时相关的气体都要通过试样表面逸出或渗入,都要通过试样颗粒之间进行扩散。
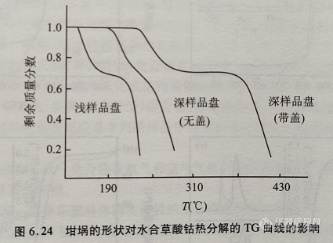
在试样量、试样颗粒度、填装松密度等实验条件都相同的情况下,样品盘的形状不同对TG曲线也有影响。图6.24中给出了不同的样品形状对于同一种水合草酸钴化合物的TG曲线的影响。由图可见,在实验时采用较浅的坩埚有利于气体产物的逸出,分解温度较低。而由带盖子的较深的坩埚所得到的TG曲线中的分解温度最高,这表明较深的坩埚不利于气体产物的逸出,盖子则进一步抑制了气体产物的逸出。样品盘的加深或带盖,给气体的扩散增加了阻力,最终导致了反应的延迟和反应速率的降低。因此,在实验时应尽量使用少量试样薄薄地摊在浅皿状坩埚中,使过程免受扩散控制。除非为了防止试样飞溅,一般不采用加盖封闭坩埚,因为这会造成反应体系气流状态和气体组成的改变。
6.5.2.3 温度控制程序的选择
实验时,根据实际需要可以通过热重仪的控制软件来方便、灵活地设置各种各样的温度随时间变化的程序,由不同的温度控制程序得到的热重实验曲线也有很大差异。常用的温度控制程序主要采用线性加热、线性降温的温度变化形式,即在实验时按照一定的加热和降温速率进行加热或降温,有时还会在加热或降温过程中选择一个等温段。
对于线性加热或降温的过程来说,较快的加热速率可以提高仪器的灵敏度,但会引起分辨率的下降,容易使相邻的分解过程更难分开。一般情况下,应选择一个合适的温度变化速率。对于大多数热重实验,一次实验的试样用量一般为5~10mg,对于如此少的试样量,10~20℃•min-1的加热速率可以使试样的分解过程分离开,常用的加热速率为10℃•min-1。在进行动力学分析时,一般要进行4~5个不同的温度扫描速率下的热重实验,选择加热/降温速率时应注意加热/温度扫描速率的改变不能引起热重实验曲线形状的变化,因为热重曲线形状的改变,往往会伴随着反应机理的改变,在此基础上得到的动力学分析结果往往是错误的。
综合以上分析,在热重实验开始前需要合理地确定气氛气体、温度范围、温度程序、坩埚等实验条件。概括来说,需要注意以下几个方面的问题:
1 选择何种气氛,测试中是否要根据情况更换气氛。
②选择合适的温度程序。含有多个结晶水则采用较慢升温速率以提高分辨率;测定物质中含有的各种形式的溶剂时也需要采用尽量慢的升温速率。
③选择合适材质和形状的坩埚。
6.5.3 测量
在完成样品准备和实验条件选择工作之后,接下来就可以开始使用热重仪进行测量了。一般来说,整个测量过程大致包括:仪器准备、样品制备、设定实验条件和样品信息、实验测量、数据处理。以下将逐一介绍这些过程。
6.5.3.1 仪器准备
一般情况下,如果热重仪在一段时间内连续使用,在实验室用电正常的前提下,仪器一般24h开机。如果仪器在关闭后重新开机,在正式使用之前应保证仪器有至少30 min的预热平衡时间。如果仪器在使用过程中,因实验需要对气氛气体做调制,也应使仪器在通气氛气体的条件下,平衡至少30min,以使炉内气体的浓度保持一致。
在仪器处于平衡稳定的状态下,在正式开始实验前还应对实验中使用的坩埚进行质量扣除操作(即“清零”或“去皮”操作),具体做法如下:
(1)取一个洁净的空坩埚小心地将其放在样品支架或吊篮上。
如果热重仪为水平式或上皿式热重-差热分析仪,应保证参比支架上有一质量相近的相同类型的坩埚。关闭加热炉,使显示屏或仪器数据采集软件中显示的天平质量几乎不变。这一过程一般至少需要几分钟,按下面板上或仪器控制软件中的“清零”按钮(一般为“tare”或“Auto Zero”)。完成这一操作后,如果质量在很小的范围内变化或者不变,则表明实验中所用的坩埚的空白质量已经扣除完毕,在装人试样后软件显示的质量即为试样的绝对质量。
需要特别指出的是,在一些特殊的情况下,在热重实验过程中需要使用扎孔的盖的坩埚或向坩埚中加稀释剂, 在该过程中对于坩埚盖和加入的稀释剂的质量也应在此过程中进行扣除;以确保实验过程中记录下的质量变化为试样本身的质量变化。
(2)打开加热炉,将坩埚取下准备向坩埚中加入待实验的样品。
对于配置自动进样器的热重仪,一般可以集中对几个空白坩埚依次进行清零操作,软件会对自动进样器中每一个编号的坩埚清零过程中的质量差异进行记录,在使用时应注意不要混淆坩埚的顺序。
6.5.3.2 样品制备
将待实验的试样加入至经过扣除空白质量坩埚中,加入试样的质量一般不应超过坩埚体积的三分之一至二分之一。对于一些在高温下会剧烈分解(如炸药等)或熔融的样品而言,试样用量一般为能够覆盖坩埚底部即可,有时需要的样品量更少。对于一些剧烈分解的样品,可以通过使用大尺寸坩埚或加入稀释剂的方法来减少试样的热分解过程对支架或吊篮的损害。
每次热重实验时所用的试样量应视具体试样而定。由于实验用试样的密度不尽相同,完全根据试样的质量来确定一次实验所需的试样质量是不合适的。对于一些密度很小的碳材料试样而言,将坩埚装满后,试样的质量不超过1mg,此时若仍要求每次实验时试样的质量为5~10mg显然是不合理的。对于不同组成结构相近的一系列试样而言,为了消除实验时的试样量对实验曲线的影响,每次实验用的试样量应接近。
另外,对于一些性质已知的试样而言,在研究其在不同温度下的微小的质量变化时,通常通过加大试样量来提高实验的灵敏度。例如,对于一些复合氧化物而言,由于其结构中存在缺陷会产生一些氧空位。在有氧条件下,加热时会产生一个微小的增重过程。这一过程中的质量变化通常小于0.5%,用较少的试样量很难检测到这一过程。再如,在研究试样的升华过程时,通常使用不加盖坩埚和加扎孔盖坩埚条件下得到的热重实验曲线进行对比。
制样时,将适量的试样加入至坩埚中。用镊子夹住坩埚在桌面上振动几下,使试样均匀地分布在试样底部。
对于一些较易挥发和不稳定的液体黏稠试样或易吸潮的粉末试样而言,摇匀试样的操作要快,以免试样在空气中停留太久而发生变化。
打开加热炉,用镊子小心地将试样加入到热重仪的吊篮或支架上。及时关闭加热炉,在仪器控制软件中设定试样信息和操作条件,待软件显示的质量读数不发生变化时,即可开始实验。
对于一些较易挥发的液体试样而言,由于试样的质量一直在发生变化,此时应在天平清零操作后提前在控制软件中设定好相应的信息然后将试样放入支架或吊篮中并关闭加热炉,尽快开始实验。
6.5.3.3 设定实验条件和样品信息
目前的商品化热重仪都配有可以控制仪器的控制软件和数据分析软件,不同厂家的仪器的软件界面各不相同,但在软件中需要输入的试样信息和实验条件信息大多十分相似。在软件中输入的与实验相关的信息,可以在后期的数据分析过程中被方便地查看和显示。
一般来说,在正式实验开始前,需要向控制软件中输入的信息主要有:
1. 样品信息
样品信息主要包括样品名称、编号、送样人、实验人、批次、文件名等。目前大多数仪器的软件不支持中文输入,在有些软件中可以输入试样的中文名称,建议用英文字母和数字表示以上信息,其中最好不要出现“%”“?”“\”以及汉字等不能识别的符号。
对于配有自动进样装置的仪器而言,除了以上信息外,还应输入装有样品的坩埚所对应的自动进样器的位置序号。
2. 实验条件信息
与实验条件相关的信息主要有:
(1)试样质量
一般不需要手动输入试样的质量,可以通过软件读取天平的示数来实现,由于试样加入坩埚之前,空白坩埚的质量已经进行了扣除,软件显示的质量即为试样的质量。目前普遍采用实验开始时采集到的每一个质量信号作为试样的初始质量,在大多数软件中还有一个备注选项,可以在其中输入一些需要特别注明的实验信息,如试样来源、取样、处理方法等。
(2)温度程序信息
温度程序信息主要包括实验时的升温/降温速率、不同温度下的等温时间以及实验开始温度、最高温度等。对于温度调制热重实验,还应输入温度调制的振幅和调制周期。对于速率控解析热重实验,除输入实验温度范围和线性温度变化速率外,还应输入有质量变化时的最小速率以便仪器在此速率以上自动调整加热/降温速率。
(3)试样信息
试样信息主要包括实验时使用的坩埚类型(开口还是加盖)、坩埚材料、坩埚体积等。
由于坩埚对实验数据也会产生影响,因此,在实验时一定要及时在软件中输入坩埚体积等信息。不应出现在实验时实际使用的坩埚与软件中记录的坩埚的信息不一致的现象。
(4)气氛种类及流速
在控制软件中应及时记录下实验时使用的气氛的种类和流速。对于一些配有数字控制的质量流量计的仪器而言,输入的流量即为实验时气氛的流速。对于其他流量计,需先调节流量计的示数,再将流量输入到软件中。无论使用以上何种流量计,都应使用皂膜流量计测量气氛在加热炉出口的流速,将其数字作为实验时所用气氛的最终流速。
(5)其他信息
除了以上试样信息和温度程序信息外,还要在控制软件中设置数据点采集频率,常用的采点频率为1秒/点。对于实验周期很长的实验可以用较小的采点频率为10秒/点,相反地,对于一些较快的反应,则需要较高的采点频率记录下实验过程中的每一个细节变化。一般来说,采点频率越高,得到的实验曲线的信噪比较差。
6.5.3.4 实验测量
在输入以上信息后,待试样的质量信号稳定后(易挥发试样除外),可以按下控制软件中的“开始”按钮开始实验,加热炉按照已经设定温度控制信息对试样进行加热、降温、等温等操作,仪器的测量装置实时记录下这些过程中的质量变化信息并保存。在实验结束后,实验过程中试样信息、实验程序、实验数据等信息将单独生成一个文件,这个文件可以使用仪器附带的分析软件打开并进行相关的数据处理。
由于热重仪天平的灵敏度非常高,在实验过程中实验室内仪器工作台旁尤其不可以出现较大的振动,炉子出口附近也不能有较大的气流波动。例如,由于实验室内空调口和电风扇易引起气流波动,因此其应与炉子出口保持足够大的距离。
6.5.4 数据处理
在获得热重实验数据之后,用仪器附带的分析软件打开实验时生成的原始文件。由于数据采集软件是以时间为单位进行计时的,对于恒定加热/降温速率的实验而言,可以通过下式将时间换算成温度:
式中,T0为实验开始温度,t为实验时间,β为加热速率。
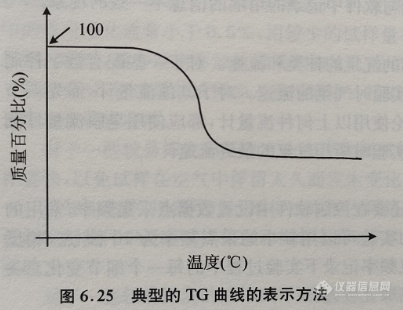
对于TG曲线,在数据采集软件中的每一时刻t都记录下了相对应的温度和质量变化。在作图时,可以直接用温度轴作为横轴,也可以根据等式(6.18)将时间直接转换为温度。通常用纵轴表示质量。为了便于比较,一般通过软件将试样的绝对质量(单位一般为毫克)转换为相对质量(用百分数表示)。实验开始时的质量为100%,实验中每一时刻(即温度)的质量百分数为以百分比表示的试样质量,如图6.25所示。
由图6.25可见,试样质量变化的实际过程通常为一个渐变的过程,并不是在某温度瞬间完成的,因此热重曲线的形状不呈直角台阶状,而是有过渡和倾斜区段。
在热重曲线中,纵坐标表示质量(一般用百分比表示)从上向下表示减少,横坐标表示温度或时间从左向右表示增加。
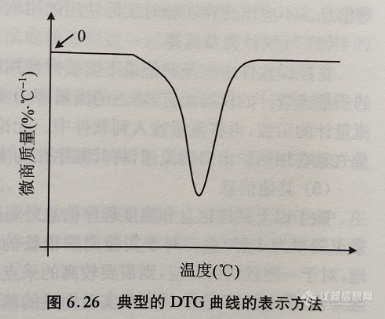
热重曲线通常用来表示质量变化速率与随温度或时间的变化关系,由质量曲线对温度或时间求导得到,如图6.26所示。
由实验直接得到的DTG的单位一般是mg•s-1,可以用以下关系式分别将DTG的单位转化为%·s-1、%·min-1或%·℃-1:
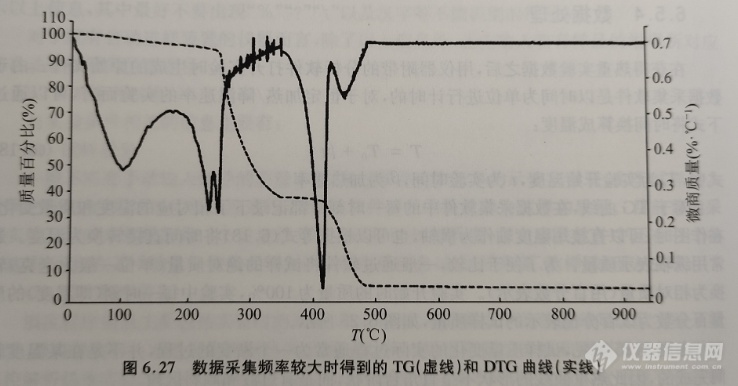
为了便于比较,DTG的单位应该换算为%·s-(时间较短时)、%·min-1(时间较长时)、%·℃-1 (线性加热时)的形式。早期的热分析仪的微分单元可以直接记录DTG曲线,现在的商品化仪器主要通过分析软件的微分功能直接将热重曲线进行微分得到DTG曲线,实验时的数据采集频率对DTG曲线的形状影响较大。微分时的取点间隔越小所得到的DTG曲线越符合实际,但得到的各点的数据点之间的波动大,即曲线上毛刺较多,如图6.27所示。由图可见,由于数据采集频率较大,通过得到的DTG曲线的基线的毛刺较为明显。
一般情况下,采用相同的数据采集频率得到的不同加热速率下的热重曲线经微分后,加热速率下的DTG曲线则较平滑。这是因为对于较快的加热速率而言,完成相同的温度范围的温度扫描所需要的时间较短,采集到的数据点也比较少,因此曲线较为平滑。可以通过调整数据采集频率的方法来改善这种现象,即较小的加热速率由于时间较长,可以加大采集点间距,而较大的加热速率由于实验较短,则应适当加大数据采集频率。
从数学上也可以按照牛顿二项式定理由TG曲线来得到各点的DTG曲线,即
式中,h为质量变化时的等时间间隔,即采集时间间距,mn-2, mn-1,mn+1,mn+2是前后相邻的四个点n-2、n-1、n+1、n+2的质量。由等式(6.20)可见,h值越小则得到的dmn/dt值越大,即基线的波动越明显。
使用分析软件可以方便地实现上述热重曲线作用,并对图中每一个质量变化台阶的质量百分比和相应特征温度进行计算,并将处理结果转化成相应的图片文件和可以在其他常用绘图和数据分析软件(如Excel、Origin等)运行的ASCII码文件。
有时也用试样质量损失百分比作为纵坐标来表示热重曲线,如图6.28所示。
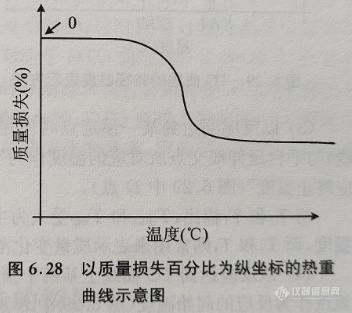
与图6.25不同,这种作图方式的纵坐标表示的是质量变化,开始为零。这种方式一般不常用。
6.6 TG曲线的特征物理量的确定方法
6.6.1 常用的特征温度表示方法
对于得到的热重曲线而言,所使用的仪器的灵敏度对曲线的形状的影响很明显。而对于同一台仪器,由于实验条件的不同也会对曲线形状的变化产生较为显著的影响。为了便于比较和研究,人们规定了TG曲线的一些特征温度。
热重曲线中质量变化反映了试样的性质在温度变化过程中发生的变化,对于一个变化过程,一般用温度和质量来同时进行描述。常用的物质温度主要有初始温度(initial temperature,一般用Ti表示)、外推起始温度(extra plot onset temperature,用Tonset表示)、终止温度(final temperature,用Tf表示)、外推终止分解温度(end temperature,用Te或Tend表示)、n%分解温度(n% temperature,用Tn%表示)和最快质量变化温度(DTG峰值温度,peak temperature,用Tp表示),这些特征温度可以方便地使用分析软件在图上标注出来。
目前主要有以下几种确定TG曲线的特征温度“起始温度”的方法(见图6.29):
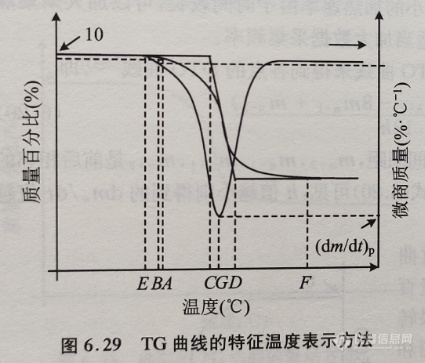
(1)以失重数值达到最终失重量的某一百分数时的温度值作为反应起始温度(图6.29中A点)。
n%反应温度为质量减少n%时的温度,可以直接由热重曲线标出(Tn%),常用的n%分解温度主要有0%、1%、5%、10%、15%、20%、25%、50%时的 Tn%,0%分解温度是指试样保持质量不变的最高温度。
这种温度比较容易确定,可以用来简单比较相同条件下得到的热重曲线之间的反应温度的差异。
(2)以质量变化速率达到某一规定数值时的温度作为反应起始温度(图6.29中B点)。
(3)以反应到达到某一预定点时质量变化曲线的切线(如TG曲线斜率最大点处的切线)与平台延伸线交点所对应的温度作为“外推反应起始温度”(图6.29中C点)和“外推反应终止温度”(图6.29中D点)。
与Ti和Tf相比,Tonset和Tend受人为主观判断的影响较小,常用来表示试样的特征分解温度,而Ti和Tf则常用来表示质量变化范围的起征温度。
(4)以反应达到TG曲线上某两个预定点的连线(切割线)与平台延伸线交点所对应的温度作为反应的起始温度(图6.29中E点)和反应终止温度(图6.29中F点)。
但是无论采用何种方法确定初始温度,都具有相应的特殊性和局限性,至今尚未得到一种公认的普遍适用的方法。
最快质量变化温度也称最大速率温度或DTG峰值温度(Tp),是指质量变化速率最大的温度(图6.29中G点),可以直接由DTG的曲线的峰值获得,Tp对应的质量变化速率即为反应的最大质量变化速率,常用(dm /dt)p表示(见图6.29)。
常用图6.29中C点外推起始温度或A点预定质量变化百分比(通常为5%)温度来表征物质的热稳定性。
除了以上特征温度外还经常用10%正切温度(TTN)、加和温度(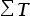 )和积分程序分解温度(Integral Procedural Decomposition Temperature, IPDT)来表示一个过程的特征温度。其中:
)和积分程序分解温度(Integral Procedural Decomposition Temperature, IPDT)来表示一个过程的特征温度。其中:
(1) 10%正切温度(TIN)是通过正切温度(TN)与失重量为10%时的面积比的乘积得到的, 而正切温度则通过TG曲线上最大失重速率点的切线与温度轴的交点(温度)来确定。正切温度与起始分解温度有关,而面积比涉及起始分解程度。试样越稳定,这两个数值就越大。
(2)在分解完成后达到恒重时的残余质量C值加1再除以2,以此商值为余重C时所对应的温度,即为加和温度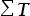 。
。
(3)积分程序分解温度法根据失重曲线下面的面积来分析高聚物的热稳定性,提供了对不同材料进行比较的共同基础。
6.6.2 由TG曲线确定质量变化信息
第一步,按照下式计算质量变化百分比Δm;
式中,m0为样品起始的质量,m1为质量变化结束后的质量百分比。
对于含有两个质量变化步骤的TG曲线而言,第二步的质量变化百分比为
 式中,m1为第二步质量变化开始时(即第一步质量变化结束时)的质量,m2则为第二步质量变化结束时的质量。
式中,m1为第二步质量变化开始时(即第一步质量变化结束时)的质量,m2则为第二步质量变化结束时的质量。
某些物质在一定温度范围还可能会发生多个反应,而且很有可能多个反应同时发生或相互有重叠、覆盖,表现在TG曲线上就是台阶之间不明显,这时候通过微分曲线往往可以获得更多有价值的信息。TG曲线上的一个台阶,对应于DTG曲线为一个峰(图6.27和图6.29),通过这个峰可以更加容易地确定质量变化的开始温度Ti、结束温度Tf、分解最快的温度(峰温)Tmax,从而区分从TG曲线上难以辨别的台阶;DTG曲线下的峰面积与质量变化成正比;DTG曲线的任一点都代表在该温度时质量变化的速率,因此可应用于反应动力学的研究。
6.7 TG曲线的解析
如前所述,热重曲线是实验过程的最终体现,不同的试样和实验条件下所得到的曲线各不相同。由于试样、实验条件、仪器本身等因素对实验曲线均会产生不同的程度的影响,因此,合理、全面地分析热重实验曲线显得十分重要。在分析曲线时要充分结合试样本身的组成、结构和性质以及实验条件等因素进行综合分析。
在对TG曲线进行分析时,除了需要确定以上的特征温度外,还需对热重实验曲线中每一个质量变化过程作更为详细和具体的解释和说明,但有时仅通过热重曲线得到的信息难给出全面、合理的解释,此时需要与由其他的表征手段得到的实验数据结合起来进行综合分析,在之后的相关章节中将对这些内容加以阐述。
由实验直接记录得到的是以直流电动势形式反映试样温度的和反映试样质量变化的数据,由此绘制的图形称为原始热重记录曲线,对原始曲线作适当处理后就能得到基本的热重数据:试样在一定范围内的质量变化量和变化过程的起始温度与终止温度, 以及符合规定表达方式的热重曲线。
由于相当多的原始的热重曲线并不符合有关热重出线的表达要求和规范, 因此通常不能将其直接作为最终形式的实验数据直接列入正式报告,通常需要将原始的热重曲线转换成规范的热重曲线。
对于热重曲线,有时还需对每步变化过程的本质进行更为详细具体的解释和说明,但是很多情况下仅由TG曲线提供的信息显然是难以做到的,还需要结合其他分析方法的结果来进行综合分析。
下面首先以CuSO4·5H2O脱去结晶水的过程(见图6.30)为例,说明由曲线可以得到的信息。
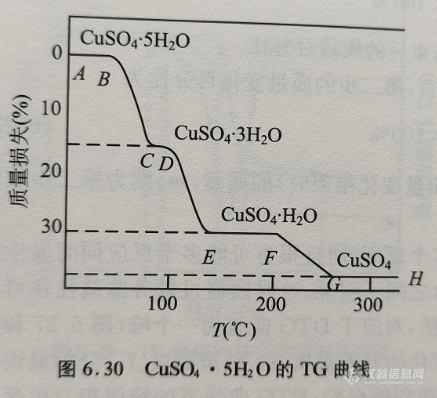
图6.30中的TG曲线在A点和B点之间没有发生质量变化,即试样是稳定的,在B点开始脱水,曲线上呈现出失重,失重的终点为C点。这一步的脱水过程为
CuSO4·5H2O→CuSO4·3H2O+2H2O
在该阶段,CuSO4·5H2O失去两个水分子。在C'点和D点之间试样再一次处于稳定状态,然后在D点进一步脱水,在D点和E点之间脱掉两个水分子。在E点和F点之间生成了较为稳定的化合物,从F点到G点开始脱掉最后一个水分子。由G点到H点的平台表示形成了更加稳定的无水化合物。
CuSO4·3H2O→CuSO4·H2O+2H2O
CuSO4·H2O→CuSO4+H2O
根据热重曲线上各平台之间的质量变化,可计算出在各个步骤中样品的失重量。图6.30中的纵坐标通常表示为质量的标度和总的失重量。
利用热重法测定试样时,往往开始有一个很小的质量变化,这是由试样中所存在的吸附水或溶剂引起的。当温度升至T1时,才产生第一步失重。第一步失重量为W0-W1,其失重量ΔW为
式中,W0为试样的质量,W1为第一次失重后试样的质量。
在热重曲线中,水平部分表示质量是恒定的,曲线斜率发生变化的部分表示质量的变化。根据热重曲线上的各阶段的失重量可以很简便地计算出各步的失重量,从而判断试样的热分解机理和各步的分解产物。从热重曲线可看出热稳定性温度区、反应区、反应所产生的中间体和最终产物。
另外,通过热重曲线可以确定化合物的分解机理。
下面以CaC2O4·H2O为例,来说明由TG曲线确定热分解机理的过程。
含有一个结晶水的草酸钙的热重曲线和热重曲线,如图6.31所示。
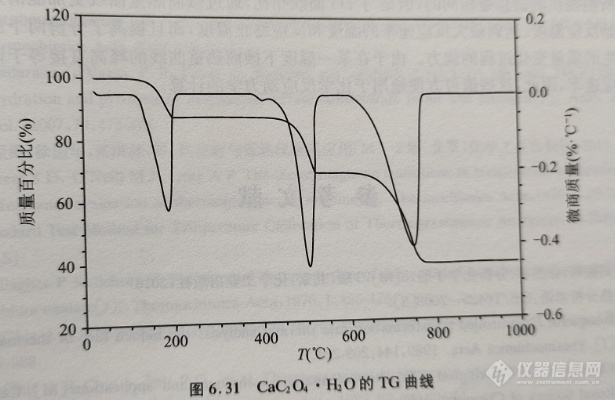
一般地,CaC2O4·H2O的热分解过程分下列几步进行:
CaC2O4·H2O→CaC2O4+H2O
CaC2O4→CaCO3+CO
CaCO3→CaO+CO2
在100℃以前,CaC2O4·H2O没有失重现象,其热重曲线呈水平状,为TG曲线中的第一个平台。在100~200℃之间失重并开始出现第二个平台。这一步的失重量占试样总质量的12.5%,相当于每摩尔CaC2O4·H2O失去1 mol H2O。在400~500℃之间失重并开始呈现第三个平台,其失重量占试样总质量的18.5%,相当于每摩尔CaC2O4分解出1molCO。最后,在600~800℃之间失重并出现第四个平台,为CaCO3分解成CaO和CO2的过程。
图6.31中的DTG曲线所记录的三个峰是与CaC2O4·H2O三步失重过程相对应的。根据这三个DTG的峰面积,同样可算出CaC2O4·H2O各个热分解过程的失重量。
在热重法中,DTG曲线比TG曲线更为有用,因为它与DTA曲线相类似,可在相同的温度范围进行对比和分析而获得有价值的资料。
6.8 TG 曲线的描述
对TG曲线的描述十分重要,应结合实验条件、样品的组成和结构、前处理、制备方法等相关信息对TG曲线进行合理、准确、全面的描述。
由热重实验得到的是在程序控制温度下物质质量与温度关系的曲线,即热重曲线(TG曲线),横坐标为温度或时间,纵坐标为质量。必要时,后者也可用失重量等其他形式表示。由于试样质量变化的实际过程不是在某一温度下同时发生并瞬间完成的, 因此热重曲线的形状不呈直角台阶状,而是形成带有过渡和倾斜区段的曲线。
从上述应用实例可以看出:当原始试样及其可能生成的中间体在加热过程中因物理或化学变化而有挥发性产物释出时,从热重曲线可以得到它们的组成、热稳定性、热分解及生成的产物等与质量相关联的重要信息。另外,由热重曲线还可以得到其他许多有用的信息。例如,从TG曲线可以方便地得到分解温度和热稳定的温度范围。
为了获得可靠的曲线并能对曲线作出正确解释,首先应确定合理的实验条件,并尽可能用其他方法,例如X射线分析、逸出气分析以及差热分析等作进一步的补充。这是因为热重法易受许多因素的影响,由热重曲线确定的反应温度只是在一定的仪器、实验条件与试样参数条件下的值,只有经验意义。热重法的另一个局限性是其仅能反映物质在受热条件下的质量变化,因此得到的信息也是有限的。
通过对热重曲线进行一次微分所得到的热重曲线可以实时地反映试样质量的变化和温度(或时间)的关系,DTG曲线的形状与DTA曲线的相似。虽然热重曲线与TG曲线所能提供的信息是相同的,但是与TG曲线相比,通过热重曲线更加能清楚地反映出起始反应温度、达到最大反应速率的温度和反应终止温度,而且提高了分辨两个或多个相继发生的质量变化过程的能力。由于在某一温度下热重曲线的峰高直接等于该温度下的反应速率,因此,这些值可方便地用于化学反应动力学的计算。
产品货期: 2天
整机质保期: 3年
培训服务: 安装调试现场免费培训
安装调试时间: 到货后2天内
电话支持响应时间: 2小时内
是否提供维保合同: 是
维修响应时间: 1天内
节假日是否提供上门服务: 是
核心零部件货期: 2天
核心零部支持时间: 20年
是否支持上门巡检: 是
是否提供预防性维护计划: 是
是否提供期间核查方案: 是
是否提供免费应用支持: 是
是否提供付费应用支持: 是
是否提供线上售后平台: 是
维修付款方式: 先维修后付款
基本维修资料公开: 技术参数
无理由退换货: 不支持
其他: 用心服务,尽最大努力做到客户的满意。
中航时代热重分析仪TGA热重分析仪(微机差热天平-TGA微机热天平-微机差热仪)的工作原理介绍
热重分析仪TGA热重分析仪(微机差热天平-TGA微机热天平-微机差热仪)的使用方法?
中航时代TGA热重分析仪(微机差热天平-TGA微机热天平-微机差热仪)多少钱一台?
热重分析仪TGA热重分析仪(微机差热天平-TGA微机热天平-微机差热仪)可以检测什么?
热重分析仪TGA热重分析仪(微机差热天平-TGA微机热天平-微机差热仪)使用的注意事项?
中航时代TGA热重分析仪(微机差热天平-TGA微机热天平-微机差热仪)的说明书有吗?
中航时代热重分析仪TGA热重分析仪(微机差热天平-TGA微机热天平-微机差热仪)的操作规程有吗?
中航时代热重分析仪TGA热重分析仪(微机差热天平-TGA微机热天平-微机差热仪)报价含票含运吗?
中航时代TGA热重分析仪(微机差热天平-TGA微机热天平-微机差热仪)有现货吗?
最多添加5台
