找不到产品?留下需求帮您找
一键询价-

赛多利斯 Microsart ATMP DNA提取试剂盒
一周
面议
-

赛多利斯 Microsart AMP DNA提取试剂盒
一周
面议
-

赛多利斯 Microsart Research 细菌检测试剂盒
一周
面议
-

赛多利斯 Microsart ATMP 细菌检测试剂盒
一周
面议
-

赛多利斯 Microsart Research 支原体检测试剂盒
一周
面议
-

赛多利斯 Microsart® ATMP 支原体检测试剂盒
一周
面议
-

赛多利斯 Microsart 支原体验证标准品(菌株标准品)
一周
面议
-

赛多利斯 Microsart 支原体校准试剂(DNA标准品)
一周
面议
-

赛多利斯 Microsart® 细菌验证标准品(菌株标准品)
一周
面议
-

赛多利斯 Microsart 细菌校准试剂(DNA标准品)
赛多利斯 | 一周
面议



五种致泻性大肠埃希氏菌鉴定试剂盒(PCR法)
致泻大肠埃希氏菌鉴定剂盒(PCR 法)
u 产品说明
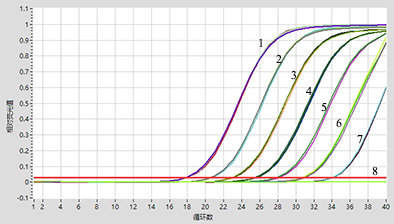
病菌检测系列可针对食品、饲料等样品中的致病微生物的特异核酸片段进行扩增,仪器实时监测扩增
过程中的荧光信号变化,自动判读结果。本产品用于致泻大肠埃希氏菌的检测。检出限为 10
3 CFU/ml。
◆ 产品组成(96 测试)
试剂 含量 作用
孔 1 反应液-uidA
23μl/孔
12 孔/排
8 排
(本产品使用 12 联
PCR 管分装,每排含
12 种反应液各 23ul)
内参
孔 2 反应液-ipaH 鉴定 EIEC
孔 3 反应液-pic 鉴定 EAEC
孔 4 反应液-aggR 鉴定 EAEC
孔 5 反应液-astA 鉴定 EAEC
孔 6 反应液-stx1 鉴定 EPEC 与 EHEC
孔 7 反应液-stx2 鉴定 EPEC 与 EHEC
孔 8 反应液-bfpB 鉴定 EPEC 与 EHEC
孔 9 反应液-escVa 鉴定 EPEC 与 EHEC
孔 10 反应液-lt 鉴定 ETEC
孔 11 反应液-stp 鉴定 ETEC
孔 12 反应液-sth 鉴定 ETEC
NG-Ecoli 100μL × 1 支 阴性对照
NG-DW 100μL × 1 支 空白对照
PG-Ecoli 100μL × 1 支 阳性对照
Loading Buffer 600μL×1 支 电泳上样缓冲液
◆ 所需仪器
ABI ,BioRad,TaKaRa 等 PCR 扩增仪,电泳仪,凝胶成像仪等电泳配套设备。(使用荧光定量 PCR 仪进行定
性判读时则无需电泳设备)
◆ 自备耗材和仪器
①灭菌 1.5mL 或 2.0mL 离心管;②冰盒;③移液器(0.5-10μL,10-100μL,100-1000μL)及配套灭菌吸头;④
离心机;⑤涡旋混匀器;⑥金属浴。
◆ 样品处理
参照《GB4789.6—2016 食品安全国家标准 食品微生物学检验 致泻大肠埃希氏菌检验》中的操作步骤进行前
增菌。建议使用试剂配套细菌基因组 DNA 提取系列产品。
◆ 实验操作
1.添加模板(样本制备区,放置于冰盒中进行)
取所待检样品数+3 的 12 联反应管,将试剂完全解冻,分离心 30s。离心后揭开封口膜,使用穿刺加样法穿过
固封层向每管反应液中分别加入 2μL 模板(或直接使用无菌吸头挑取少许待检菌落至反应管中)。
加样示例:(有 2 个待测样品)
取 5 排 12 联反应管,按顺序一排全部加 NG-DW,第二排全部加 NG-Ecoli,第三排全部加样品 1,第四排全
请于-20℃条件下保存,有效期 12 个月
SM-011203M-A02
2
部加样品 2,第五排全部加 PG-Ecoli。
盖好配套的 PCR 管盖后,涡旋混匀 30s,离心 1min,立即进行 PCR 扩增反应。
2. 扩增反应(扩增及产物分析区)
按下列条件设置扩增反应:(如需使用荧光法进行检测请选择 FAM 通道)
PCR 循环 荧光收集位点
95℃ 10 分钟 1 个循环 —
95℃ 30 秒
30 个循环
—
63℃ 30 秒 —
72℃ 90 秒 ※
72℃ 5 分钟 1 个循环 —
3. 产物电泳(扩增及产物分析区)
称量 4. 0g 琼脂糖粉,加入至 200 mL 的 1×TAE 电泳缓冲液中,充分混匀。使用微波炉反复加热至沸腾,直到
琼脂糖粉完全融化形成清亮透明的溶液。待琼脂糖溶液冷却至 60℃左右时,加入溴化乙锭( EB )至终浓度为 0.5μg/mL,
充分混匀后,轻轻倒入已放置好梳子的模具中,凝胶长度要大于 10cm,厚度宜为 3mm~5mm。检查梳齿下或梳齿
间有无气泡,用一次性吸头小心排掉琼脂糖凝胶中的气泡。当琼脂糖凝胶完全凝结硬化后,轻轻拔出梳子,小心将胶
块和胶床放入电泳槽中,样品孔放置在阴极端。向电泳槽中加入 1×TAE 电泳缓冲液,液面高于胶面 1mm~2mm。将
5μL PCR 产物与 1μL 6×上样缓冲液混匀后,用微量移液器吸取混合液垂直伸入液面下胶孔,小心上样于孔中;阳性
对照的 PCR 反应产物加入到后一个泳道;一个泳道中加入 2 μ L 分子量 Marker 。接通电泳仪电源,根据公式:
电压=电泳槽正负极间的距离(cm)×5V/cm 计算并设定电泳仪电压数值;启动电压开关,电泳开始以正负极铂金丝
出现气泡为准。电泳 30min~45min 后,切断电源。取出凝胶放入凝胶成像仪中观察结果,拍照并记录数据。
u 可使用 Gold view、Gal-Rad 等等效的核酸荧光染料替代 EB。
u 推荐使用 DNA Marker:DL2000 或 100bp ladder,等可指示 100bp~1500bp 条带的 Marker。 ◆ 结果分析
1. 阴阳性判读:
进行电泳检测时,需对比 Marker 进行判断,当目的靶标对应位置出现单一显著条带时可判断该靶标为阳性;
否则为该靶标检测为阴性。(使用荧光定量 PCR 仪检测时,检测孔 Ct≤30 时判断该孔为阳性;当检测孔 Ct>30 时,
该检测孔为阴性)
SM-011203M-A02
3
示例电泳图
2. 有效性判读:
需同时满足:1.空白对照中所有泳道均为阴性;2.阴性对照中 uidA 泳道阳性,其余泳道阴性;2.阳性对照中所
有泳道阳性,此时可判断实验有效。如无法满足上述条件,则实验无效,需重复实验;如重复后结果仍为无效,请
于本公司技术支持联系。
3. 结果判读:
在实验有效的情况下,可根据下表进行判读:
致泻大肠埃希氏菌类别 目标条带的种类组合
EIEC ipaH(+)
uidA
(+/-)
EAEC aggR,astA,pic 中一条或一条以上阳性
EPEC bfpB(+/-),eae(+),stx1(-)stx2,(-)
STEC/EHEC stx1,stx2 中一条或一条以上阳性,eae(+/-),bfpB(-)
ETEC lt,stp,sth 中一条或以上阳性
u 97%以上大肠埃希氏菌为 uidA 阳性,可参考阴性对照中该基因检测结果判断扩增效果;
u 当结果判定为 EPEC 阳性时,若 bfpB 靶标为阳性则说明样品含有典型 EPEC;若 bfpB 靶标为阴性则说
明样品为非典型 EPEC;
u 当结果判定为 STEC/EHEC 阳性时,若 eae 靶标为阳性则说明样品含有典型 EHEC;若 eae 靶标为阴性
则说明样品为非典型 EHEC。
◆ 注意事项
1.本试剂检测灵敏度高。为了防止污染,实验要分区操作。
1)一区:样本制备区。
2)第二区:扩增及产物分析区。
★ 分区之间好进行物理性隔离,避免人为因素造成的污染。
2. 实验过程中穿戴工作服和乳胶手套,使用移液器,试验产生的所有废弃物及时处理。
3.严格按照操作步骤操作,试剂配制和加样等步骤请严格按照说明书要求在冰盒上操作。
4.反应液中的成分对光敏感,应避光保存。试剂使用前要完全解冻,但应避免反复冻融,推荐使用前离心 30
秒。
5.不同批号试剂请勿混合使用,在有效期内使用。