经皮给药制剂研究前沿:一文了解微透析(微灌注)活体取样技术

微透析(微灌注)作为近年来新兴的一种活体取样技术,克服了传统取样存在的样本量较多、前处理过程复杂、不能准确反映成分在机体内实时变化、不能准确测定游离药物浓度等缺点,具有活体、实时、靶向、连续取样等特点,能更真实地反映药物在机体吸收、分布、代谢、排泄的过程,在药动学及药动学药效学(PK-PD)结合模型的研究中被广泛应用[1-2]。美国FDA近年已经通过微透析(微灌注)技术开展了一些临床试验,结果表明该技术有潜力成为经皮给药制剂药品研究新方法,解决了我国经皮给药系统(TDDS)局部药物浓度评价困难的问题。为此,本文通过梳理微透析(微灌注)技术的原理及特性,总结其在经皮给药制剂研究中的应用现状,分析了存在的问题和挑战。
1微透析技术原理概述
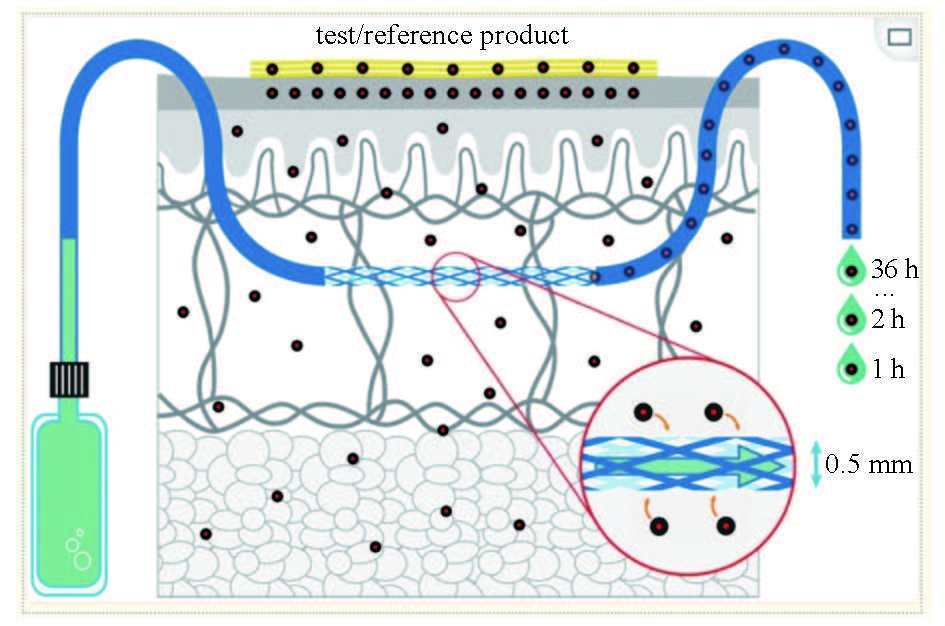
皮肤微透析 (dermal microdialysis,DM) 技术使用平行埋植于真皮层或皮下组织层的线性探针(linear probe) 以及探针中灌流的生理溶液,将皮下内源或外源性物质以一定比例浓度梯度透过探针的半透膜进入透析液中(图1)。皮肤微透析是一种独特的技术,用于在作用部位对局部和/或全身给药的药物进行体内取样,例如对真皮和皮下组织中未结合的含药组织液进行取样。其作为一种研究方法在过去十年中经历了快速发展、改进和验证,并已被证明是药代动力学和药效学研究的多功能、安全和有价值的工具[1]。
用于微透析实验的探针在形状和材料上可能有很大的差别,这取决于它们在实验中的使用部位。Delgado等人(1972年)开发了早期版本的微透析探针[2],该探针被称为透析电极管,用于清醒猴子的长时间脑内灌注实验。第一个应用到体内的线性探针,是由Ungerstedt 和 Pycock (1974)首次介绍的,采用了中空纤维设计(图2)。由于线性是单向流动且直径小,因此很少造成组织液干扰,其缺点是需要进出两次穿透组织。还有一种兼具强度和灵活性的长线性探针,用于在软外周组织中取样(图3)。另外,还有最常见的刚性探针用于脑部微透析研究(图4),该研究使用了植入导管和柔性针式探针,以减少运动中被误穿刺的风险。每种类型探针都有不同截留分子量规格,截留分子量由探针膜孔径大小决定,分子量范围通常为6~100 kDa,蛋白质类大分子一般不能适用。用于微透析探针的材料有聚碳酸酯、聚醚砜或铜甲烷。近几年,出现一种微灌注(dermal Open flow microperfusion,dOFM)的新技术,探针外观类似于线性微透析探针(图5),材料不同于微透析的半透膜,而且灌流液的灌注方式也不太一样,由于该技术采用无过滤膜设计,可以有效兼容亲脂性药物和蛋白质类大分子[3]。
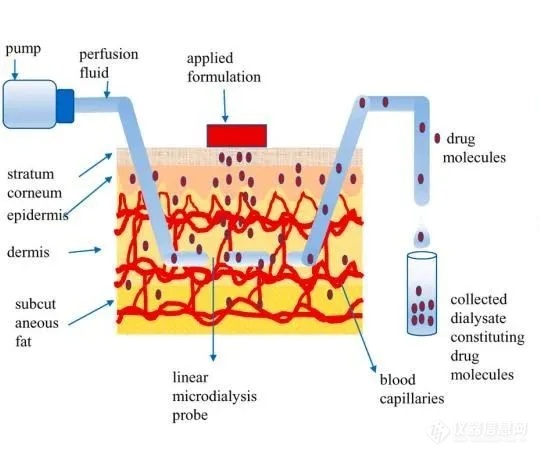

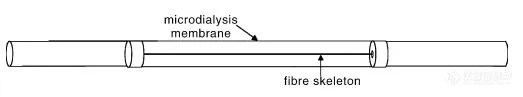
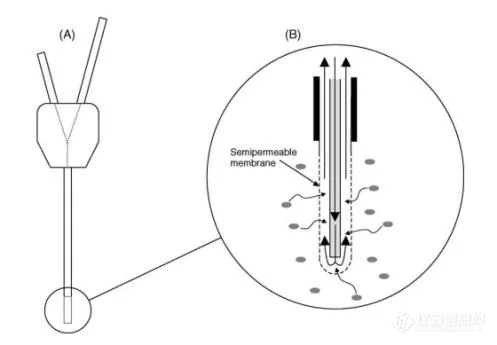
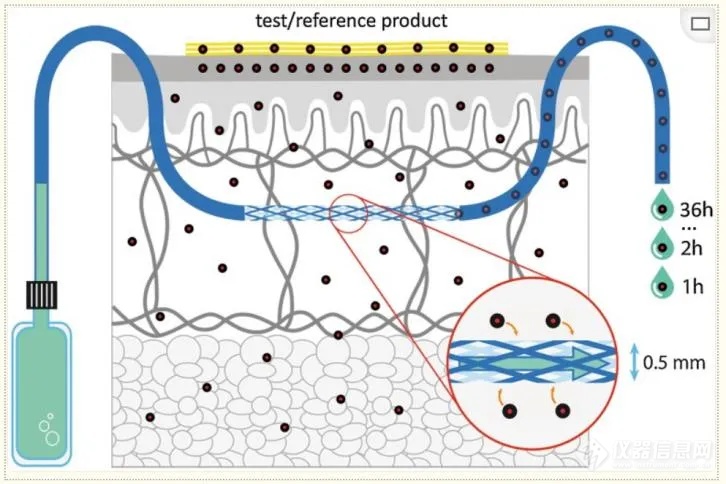
图5.真皮开流微灌注(dOFM)示意图[5]
2 皮肤微透析技术应用现状
经皮给药微透析方法可用于检测皮肤/真皮细胞外液在不同物理或化学损伤后或生理条件下的生化变化。在各种类型的皮肤病、炎症、疼痛、烧灼损伤程度和分布的研究中,经皮给药和皮肤微透析技术在临床前和临床人体试验中都有广泛的应用。该技术也适用于不同给药途径(包括全身性和局部性)或各种配方工艺制剂的生物利用度的比对。在临床和临床前通过主动(如离子导入)或被动(各种赋形剂和药物释放系统)促渗剂技术来提高化合物的皮肤通透性[6]。以下就皮肤微透析的方法开发关键问题,包括检测方法、促渗研究、纳米药物、经皮给药制剂临床研究以及皮肤病研究方面进行综述和讨论。
2.1微透析方法开发的关键问题
2.1.1相对回收率 张英丰等[7]系统地进行了相对回收率的考察,包括微透析探针半透膜的孔径超声脱气时间及灌流液改性剂对回收率的影响,流速、浓度对微透析相对回收率和绝对回收率的影响,相对回收率与相对损失率的关系及探针差异性比较,探针相对回收率稳定性考察(分为体外相对回收率的稳定性研究/体外相对损失率稳定性研究/体内相对损失率RL的稳定性研究),体内外回收率的关系,温度/灌流液改性剂对体外回收率的影响;通过体外模拟实验证实微透析探针的采样性能存在差异,体外回收率与体内回收率亦存在差异,结果表明探针的回收率稳定性和控制好流速是影响微透析回收率的主要因素。王景雁等[8]研究了反渗析法测定模型药物的探针在体回收率,结果显示药物浓度对不同药物探针回收率没有显著影响,灌注速率与探针回收率均呈指数关系,浓差法显示两种模型药物的探针回收率与传递率相等,药物与渗析膜无吸附作用。李怀国等[9]用CMA30微透析探针(瑞典CMA公司)研究了玉龙散中乌头碱在大鼠皮肤局部的经皮给药吸收过程,结果显示随着流速的增加,体内相对损失率逐渐减少,回收率增加;同时考察了乌头碱的浓度对探针回收率无明显影响。
2.1.2 探针植入深度 目前为止还没有探针植入深度的金标准检测方法。相关研究比较了显微镜HE组织切片法、US法和CT法,皮肤表层的探针深度波动范围300~500 μm,在皮肤深层的深度波动范围900~1300 μm,结果显示出深度差异高达23%[10]。
此外,微透析探针深度与局部渗透药物量之间存在相关性有许多争论。在人体腹部皮肤的真皮实验中使用线性 MD 探针,对皮肤的浅表(<1 mm)、中间(1~2 mm)和深部 (>2 mm)进行定位,探针上方的皮肤腔中局部施用 4 mg·mL-1 苯甲酸 (BA);每小时取样透析液,实验12小时,通过高效液相色谱法分析BA含量。通过 20 MHz 超声扫描测量探针的深度。时间-浓度曲线下面积(AUC)描述了实验期间组织中的药物暴露,结果显示,真皮层中探针深度与局部渗透药物量存在反比关系。该结果与体内情况相关,可以预测,探针不同深度的采样差异,将在实验开始时或短期实验研究中产生更显着的影响。基于这项研究,建议皮肤微透析技术需要测量探针深度,并且应努力将探针深度变异性降至最低[11]。
2.2微透析技术的应用
通过皮肤微透析技术可以研究经皮给药制剂药物在皮肤表面的渗透、扩散和吸收等过程,探讨药物的皮肤吸收机制,为新药研发和临床疗效评估提供依据;还可以研究经皮给药制剂药物对皮肤的刺激、过敏和毒性等作用,为药物的安全性评价和临床应用提供依据;此外,皮肤微透析技术可以监测皮肤疾病治疗过程中的药物浓度变化,了解药物在皮肤表面的代谢和排泄情况,为皮肤疾病的治疗效果评估提供依据。
2.2.1经皮给药促渗研究 微透析技术与数学建模相结合,为经皮给药系统的进一步研究提供了很好的平台。Meng Yang等[12]制备雷公藤内酯纳米乳凝胶作为新的递送系统,并描述了其离体特性,基于体内微透析测量技术的药物浓度,可以更准确地测量药物在皮肤中的扩散系数,并验证数值结果。
促渗剂是指能提高或加速药物渗透穿过皮肤的物质。理想的渗透促进剂应对皮肤无损伤或刺激,无药理活性,无过敏性,理化性质稳定,与药物及其辅料有良好的相容性,起效快,作用时间长等等。因此,选择合适的促渗剂成为透皮吸收制剂开发的重要环节。
王鹏等[13]考察了桉油作为经皮促渗剂的皮肤刺激性与在体经皮促渗活性,结果显示桉油对亲脂性药物和亲水性药物具有良好的在体经皮促渗效果,且与化学促渗剂相比,具有相对温和的皮肤刺激性,这为其在外用制剂中的应用提供了数据支持。
Markus Lubda等[10]也进行了相关研究:薄荷油作为促渗剂,以川芎嗪(logP=2.34)和葛根素(logP=-0.35)作为亲脂性和亲水性模型药物为例,当薄荷油的浓度达到一定浓度时,薄荷油才对亲脂性药物(川芎嗪)表现出较好的促渗效果;而对亲水性药物(葛根素),由于薄荷油的溶解度特征,既没有能改变皮肤角质层的屏障作用,也没有改变亲水性药物的热力学活性,因此没有表现出较好的经皮促渗活性。
樟脑作为促渗剂,在不同亲脂性药物经皮给药递送中也有潜在应用。例如通过体内皮肤微透析,研究樟脑对亲脂性和亲水性模型药物(即利多卡因和替加氟)的增强作用,体内皮肤微透析表明,樟脑对模型药物的经皮给药吸收具有相似的渗透行为,与常用和标准的渗透增强剂月桂卡普兰相比,樟脑产生的皮肤刺激性相对较低。体外皮肤渗透研究表明,樟脑能显著促进不同亲脂性模型药物的经皮给药吸收,且渗透增强活性随药物logP值呈抛物线曲线下降,对弱亲脂性或亲水性药物的渗透增强效率最佳(估计logP值为0)[14]。
甘油也是一个良好的促渗剂,对大鼠皮内微透析环孢菌素经皮给药吸收研究表明,添加浓度为6%、10%和20%(v/v)的甘油使环孢菌素的表观吸收率分别提高3.0、6.4和6.9倍[15]。
此外,中药配方也有类似经皮给药促渗作用。杨华生等[16]采用微透析技术研究制川乌对白芍中芍药苷经皮转运的影响,从经皮转运角度研究制川乌-白芍配伍协同增效作用机制,扫描电镜观察结果表明制川乌作用于皮肤后,角质层细胞间隙明显增加,且与氮酮对皮肤的作用类似。研究表明制川乌-白芍配伍能显著提高芍药苷的经皮给药吸收,达到配伍“增效”的目的。
2.2.2皮肤微透析药代动力学分析方法研究 皮肤微透析药代动力学分析方法研究包括微透析+LCMSMS技术,药物皮肤微透析+血液微透析+LCMSMS技术,灌流液添加白蛋白提高定量回收率等技术。黎晓丽等[17]运用微透析技术研究了制川乌-白芍配伍对6种酯性生物碱局部药动学的影响,结果发现微透析采样联合LCMSMS分析技术可以用于乌头碱经皮给药吸收过程的研究。李怀国等[18]初步明确了玉龙散中乌头碱在皮肤局部的经皮给药吸收过程,为制剂工艺优化、质量标准提高以及新药药效学评价提供了实验参考依据。贺怡等[19]利用内标微透析采样技术,同步研究尼古丁经皮给药贴剂的血液和皮肤局部药动学特征,获得其较全面的体内药动学规律,结果显示尼古丁在血液与皮肤的药动学参数相比,AUC0-∞、Cmax、Tmax在皮肤中较大,MRT0-∞在血液中较大,尼古丁经皮给药贴剂经皮给药后,药动学参数证明尼古丁通过经皮给药渗透在皮肤中以相对较高的浓度蓄积,能达到快速有效的吸收,进入血液后血药浓度相对较低且维持稳定,发挥显著长效作用。王丹等[20]自行研制的双位点微透析-HPLC联用技术平台,设备简便实用,可为药动学与代谢研究提供新的取样分析检测方法。Abhay Joshi等[21]通过环丙沙星研究微透析连续采样+间歇取样,与单独连续采样对比,两种取样方式的皮肤药代动力学参数在统计学上没有差异。
2.2.3新型药物-纳米制剂研究 纳米技术的应用使得经皮给药药物递送系统的药物选择范围进一步扩大,并提高了药物的治疗效果,形成了一种极具价值、令人期待的新型给药方式。目前,常用于经皮给药药物递送系统的纳米制剂包括纳米乳、脂质纳米囊泡、脂质纳米粒、聚合物纳米粒、纳米晶体、溶致液晶纳米粒等[22]。杨硕等[23]综述了脂质体、传递体、醇质体、非离子表面活性剂囊泡4种囊泡载体的组成、特征及其制剂在经皮给药系统中治疗几种皮肤病的应用,为今后的研究提供思路。Ying Hao等[24]设计了一种近红外光响应型5-氟尿嘧啶(5-Fu)和吲哚菁绿(ICG)负载的单甲氧基-聚乙二醇-聚己内酯(MPEG-PCL)纳米颗粒(5-Fu-ICG-MPEG-PCL),然后将5-Fu-ICG-MPEG-PCL与透明质酸可溶性微针系统(HA MN)相结合,得到负载5-Fu-ICG-MPEG-PCL的HA MN,用于治疗皮肤癌,包括人表皮样癌和黑色素瘤。赖建辉等[25]应用经皮微透析技术研究双丹脂质体凝胶(SD-Lip Gels)和双丹凝胶(SD-Gels)的皮肤药动学过程,考察其在体经皮渗透性能,结果显示双丹脂质体凝胶(SD-Lip Gels)可延长药物在皮下组织中的滞留时间及有效浓度,具有更优的缓释作用,可望成为双丹方经皮给药的新剂型。杨盟等[26]采用皮肤、血液双位点同步微透析技术研究雷公藤甲素普通凝胶、纳米乳、纳米乳凝胶在大鼠皮肤和血液中的药动学过程,结果显示雷公藤甲素纳米乳和纳米乳凝胶皮肤和血液的AUC0-t明显高于雷公藤甲素普通凝胶,且雷公藤甲素纳米乳凝胶缓释效果更加明显,显著提高了雷公藤甲素的生物利用度。李静雅等[27]使用微透析采样技术联合LC-MS/MS同时测定马钱子碱和士的宁的分析方法,并研究大鼠经皮给予马钱子囊泡凝胶后的经皮给药吸收,结果显示该方法操作简便、灵敏度高、专属性强。另有文献[28]报道以脱氧胆酸钠为边缘活化剂制备盐酸青藤碱(SH)转移体(SHTs),以SH脂质体(SHLs)为对照制剂,通过Franz扩散池的体外皮肤渗透实验和双位微透析取样技术的体内皮肤/血液药代动力学实验,探讨了经皮给药渗透特性差异,建立了IVIVC,结果显示基于离体皮肤渗透特性预测SHLs和SHTs的体内皮肤/血液药代动力学特性是可行的。微透析用于囊泡药物与清漆相结合,可以量化局部应用物质的经滤泡渗透,当毛囊关闭时,咖啡因的渗透显著降低。在毛囊开放的区域,使用后的前十分钟内已经检测到咖啡因[29]。
2.2.4 临床应用 美国食品药品管理局(FDA)认为,局部作用药物的生物等效性是该类仿制药品种研发面临的一个长期挑战,这对仿制药影响很大,并且开启了最具挑战性的科学话题。在两种外用药物生物等效性的证明方法中,皮肤胶带剥除法被FDA曾经认为是最合适的方法,并命名为皮肤药代动力学法(DPK)。描述DPK方法的FDA指南草案于1998年发布,但是随后于2002年被FDA撤回,结果是目前局部作用药物的仿制需要通过比较临床试验终点来确定生物等效性[30]。在另外一项对比实验中,通过角质层胶带剥离和微透析在12名健康志愿者中评估商业外用制剂盐酸土霉素的生物等效性,经过微透析进行药代动力学评估后,在90%置信区间CI下,测试结果不能体现出生物等效性[31]。
2.2.5 微灌注-dOFM 皮肤开流微灌注dOFM是近几年兴起的临床科研PK新方法,适用于外用药物产品的 BE评估(图6)[32]。为了促进局部皮肤病仿制药的研发,FDA也开展了相关研究计划,开发一种局部作用透皮药物的药代动力学研究新方法。到目前为止,dOFM已被评估为可能成为一种PK新方法用于BE评估,并且已经有了多项临床科研BE研究,例如阿昔洛韦乳膏[33]和中度亲脂性外用药物利多卡因/丙胺卡因凝胶/乳膏[34]等。
dOFM有可能减少或避免局部应用药物产品或任何在真皮中局部起作用的口服药物产品的临床终点研究。基于临床PK的dOFM研究为临床终点研究提供了一种经济的替代方案,从而有助于开发负担得起的局部应用仿制药产品。由于所有dOFM装置都是与各自的监管机构密切合作开发的,因此,dOFM有望成为皮肤仿制药产品测试国际指南的一个组成部分[33]。
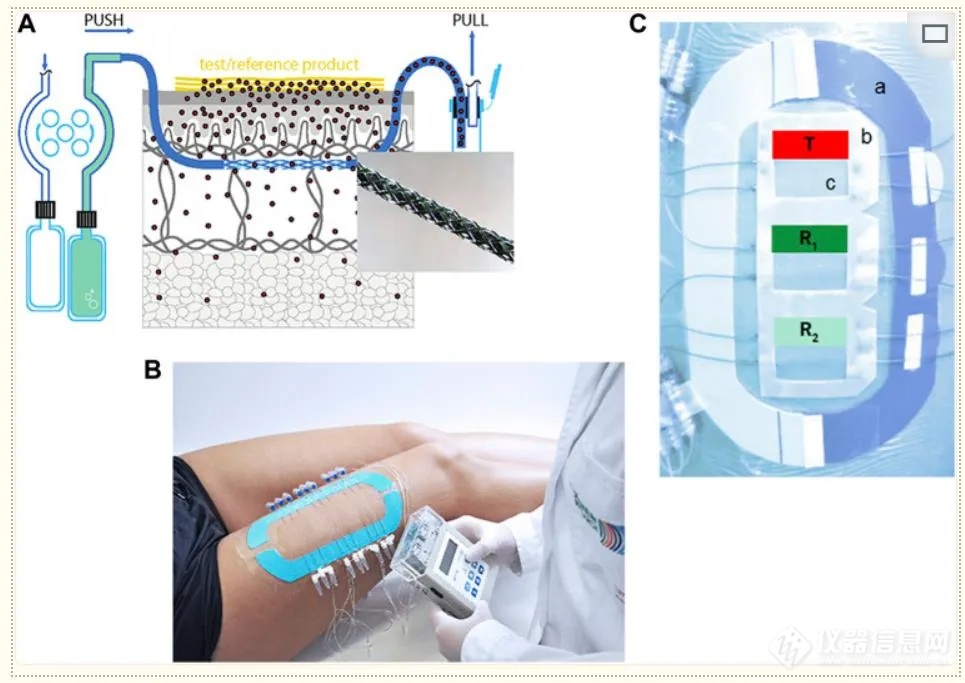
对于透皮制剂仿制药而言,透皮制剂的生物利用度可以通过基于PK的BE研究来确定[39]。但是,对于不被吸收到血液中的外用仿制药产品,血液体内药代动力学的研究并不合适,因为血液样本中活性药物成分(API)的水平通常太低而无法检测到,并且血液中的API浓度不一定能反映局部皮肤作用部位的API浓度。皮肤体内药代动力学研究提供了一种替代方法,用于评估仿制药产品相对于其参考产品的BE。皮肤PK具有很大的节约成本潜力,通过替换昂贵、耗时的临床终点研究,为外用仿制药提供了一个有前途的选择。因此,基于皮肤PK的方法,例如皮肤开流微灌注(dOFM),是解决任何皮肤外用药物产品(甚至包括Q2/Q3与原研参比不一致的产品以及无法应用于其他方法的复杂药物产品和递送系统)BE创新且有前途的替代方案[34]。
2.2.6 皮肤微透析在皮肤病中的应用 皮肤微透析(SMD)是一种多功能采样技术,可用于从人体皮肤的细胞外区室中回收可溶性内源性和外源性分子,帮助人们了解皮肤炎症和皮肤炎症性疾病,包括皮肤1型超敏反应、特应性皮炎、银屑病、牛皮癣、慢性荨麻疹、药物超敏反应和紫外线B (UVB)诱导的皮肤反应研究中的应用[35]。
3 微透析和微灌注技术面临的问题和挑战
3.1问题和挑战
尽管微透析技术在经皮给药制剂药物研究中已取得一定成果,但由于其自身特点,仍存在一些问题和挑战[2]。总体来说,微透析和微灌注是目前行业公认唯一的活体局部实时采样技术,具有多项优点,实时活体采样,动物和人体均适用(动物采样还可进行清醒模式),采样准确无损失,而且还可以多位点同时采集;不过微透析和微灌注的采样针非常细容易堵塞损坏,采样流速比较慢,影响了采样频率和采样量,而且实验操作比较复杂,对人员和设施条件要求比较高,采样探针为半透膜结构,回收率和平行性一直是个问题。微灌注能很好的解决吸附回收率问题,平行性好,装置小巧,适合临床前和临床使用,同时微灌注还兼容大分子,克服了微灌注只能采集小分子的问题。
3.1.1 采样污染 关于采样过程中样品的损失和污染问题,微透析技术需要将采样针插入待测生物体内,但由于生物体的复杂性和不稳定性,采样针可能会受到堵塞、损坏或污染,导致样品损失和误差增大[36]。
3.1.2 采样频率和样品量的限制 微透析技术需要连续采样,但采样频率和样品量都会受到限制,如果采样量过大会对生物体造成不必要的伤害或干扰,同时也会增加采样成本。
3.1.3 待测物质在体内分布的不均匀性 生物体内的物质分布往往是不均匀的,有些部位浓度较高,有些部位浓度较低,这会导致微透析技术采样到的样品浓度与实际生物体内浓度存在误差。
3.1.4 操作复杂,实验要求较高 微透析技术需要进行精细的操作,如果实验操作不当可能会导致误差或样品污染,从而影响实验结果的可信度。
3.1.5 技术的影响 经皮给药制剂药物通常具有特殊的物理化学性质,例如高分子量、低溶解度、化学稳定性差等,这些性质可能会导致微透析技术采样到的样品浓度与实际生物体内浓度存在误差[37]。
3.1.6 给药药物水平测定 微透析用于局部和全身给药后皮肤中的药物水平测定结果表明该方法不适用于所有药物或化合物的研究,实验表明如果不进一步开发该方法,通过微透析对高度蛋白结合的药物或亲脂性很强的药物进行采样是不可行的[38]。研究[39]表明,微灌注应该更适合高亲脂性和大分子药物。
3.1.7 回收率的设定 Anselm Jorda等[40]在实验方法设定-定量回收率,在使用生理盐水PA的反向透析中,双氯芬酸的平均相对损失为(99.2±0.5)%(组织探针)和(95.8±1.7)%(静脉探针);使用人血白蛋白HSA,平均相对损失分别为(﹣4.4±7.2)%和(0.2±7.5)%;结果显示PS和HSA不适用于定量双氯芬酸绝对浓度的灌注溶液。尽管方法学上存在挑战,但HSA仍可用于比较实验或生物等效性研究。而微灌注(OFM)基本没有这方面问题,回收率基本大于90%。
4 微透析(微灌注)技术的展望及建议
4.1 技术进一步拓展
微透析(微灌注)技术的未来发展将会与新技术相结合,例如纳米技术、生物工程技术等,这些新技术的应用将有助于提高微透析技术的效率和精度。此外,随着人工智能和机器学习等技术的发展,这些技术也将被应用于微透析技术中,实现自动化和智能化监测。
4.2 探针需进一步改进
目前微透析(微灌注)技术的探针还存在一些问题,例如易被堵塞、使用寿命短等。未来可以对探针进行改进,例如采用更细的探针材料、优化探针结构设计等,以提高探针的稳定性和使用寿命。
4.3 采样速度有待提高
目前微透析(微灌注)技术的采样速度相对较慢,未来可以通过采用更高效的采样技术,例如多通道采样技术、连续采样技术等,以提高采样速度。
4.4 分析方法需进一步优化
微透析(微灌注)技术的分析方法也可以得到进一步的优化,例如采用更精准的质谱分析、色谱分析等技术,以提高分析的准确性和可靠性。
4.5 拓展临床应用
微透析(微灌注)技术在临床上的应用将会更加广泛,例如在药物代谢、神经生物学、心血管等领域的应用。同时,随着技术的不断发展,微透析技术的应用范围也将不断拓展。
4.6 降低成本和提高可及性
微透析(微灌注)技术的成本相对较高,需要大量的设备和人力资源支持。未来可以通过技术改进、规模化生产等方式,降低微透析技术的成本,提高其可及性。
5 结论
经皮给药系统(TDDS)已成为一种潜在的、被广泛接受的和流行的新型药物递送系统的方法。其易于给药、易于操作、全身暴露小、不适感小、广泛的灵活性和可调性,控释、延长治疗效果以及更多优点,使其成为有效给药的有前途的方法[41]。目前,国内经皮给药制剂的研发多以仿制药和改良型新药为主,尤其是局部起效的外用制剂偏多,但是由于人体局部药物的浓度无法像临床BE一样通过血药浓度方便评价,这就面临着大量仿制药需要做大临床的现实局面。
虽然微透析(微灌注)技术在经皮给药制剂药物研究中具有广阔的应用前景,但仍需进一步解决现有问题和挑战,例如在实验设计和操作过程中应谨慎对待,同时还要不断探索新的技术和方法来提高实验的准确性和可靠性。微灌注(dOFM)技术是近年发展起来的一种类似于微透析的新技术,临床应用潜力巨大,未来应关注这类技术的持续优化和创新应用,提高其在经皮给药制剂药物研究中的准确性和可靠性,为新药研发、药物疗效、安全性评价和药品标准提供有力支持。
参考文献见原文,点击链接下载全文:
更多![]()
OFM开放式微灌注
厂商
2024.09.25
第九届中国药物制剂节圆满收官,透皮制剂研究蓄势待发
厂商
2024.09.14
皮肤屏障完整性评估:电阻抗测量与经皮水分测量的综合考量
厂商
2024.09.14
-20℃ or -80℃?储存条件对皮肤屏障渗透性和电阻抗特性的影响研究
厂商
2024.09.02