中国药科大学徐克明/钟文英团队《AFM》:火箭式微针助力深层药物递送
为解决上述问题,中国药科大学徐克明、钟文英团队创新性地提出了一种火箭式微针递药系统,能够通过自推进机制实现药物的深层递送,在黑色素瘤联合治疗中表现出良好效果。该研究以题为“A Multifunctional Rocket-Like Microneedle System with Thrusters for Self-Promoted Deep Drug Penetration and Combination Treatment in Melanoma”的论文发表在最新一期《Advanced Functional Materials》上。

该研究设计了一种名为 PcNP/TRA-HA-Tyr/CLG-MN 的双层“火箭式微针”。微针(microneedle,MN)的上层由具有光动力活性的介孔二氧化硅纳米粒子组成,其特征在于共价键合光敏剂,并在介孔中负载曲美替尼(trametinib,TRA),这是一种针对黑色素瘤细胞过度激活 MEK 通路的靶向小分子药物。微针的下层由酶交联透明质酸-酪胺(HA-Tyr)水凝胶和胶原酶(collagenase,CLG)组成,可以充当火箭助推器,通过重塑肿瘤组织的细胞外基质(extracellular matrix,ECM)促进纳米颗粒的深层穿透。在制备的三种MN中,PcNP/TRA-HA-Tyr(II)/CLG-MN在肿瘤组织的渗透最深,在体内的保留时间最长。在PcNP/TRA-HA-Tyr(II)/CLG-MN给药后进行光动力治疗能够显著抑制小鼠A375移植瘤的生长。总之,将介孔二氧化硅纳米颗粒、酶交联水凝胶和CLG介导的ECM重塑相结合的“一石三鸟”策略能够提高药物的深层穿透和联合疗法的抗肿瘤功效,在纳米医学领域展现出较好的应用潜力。
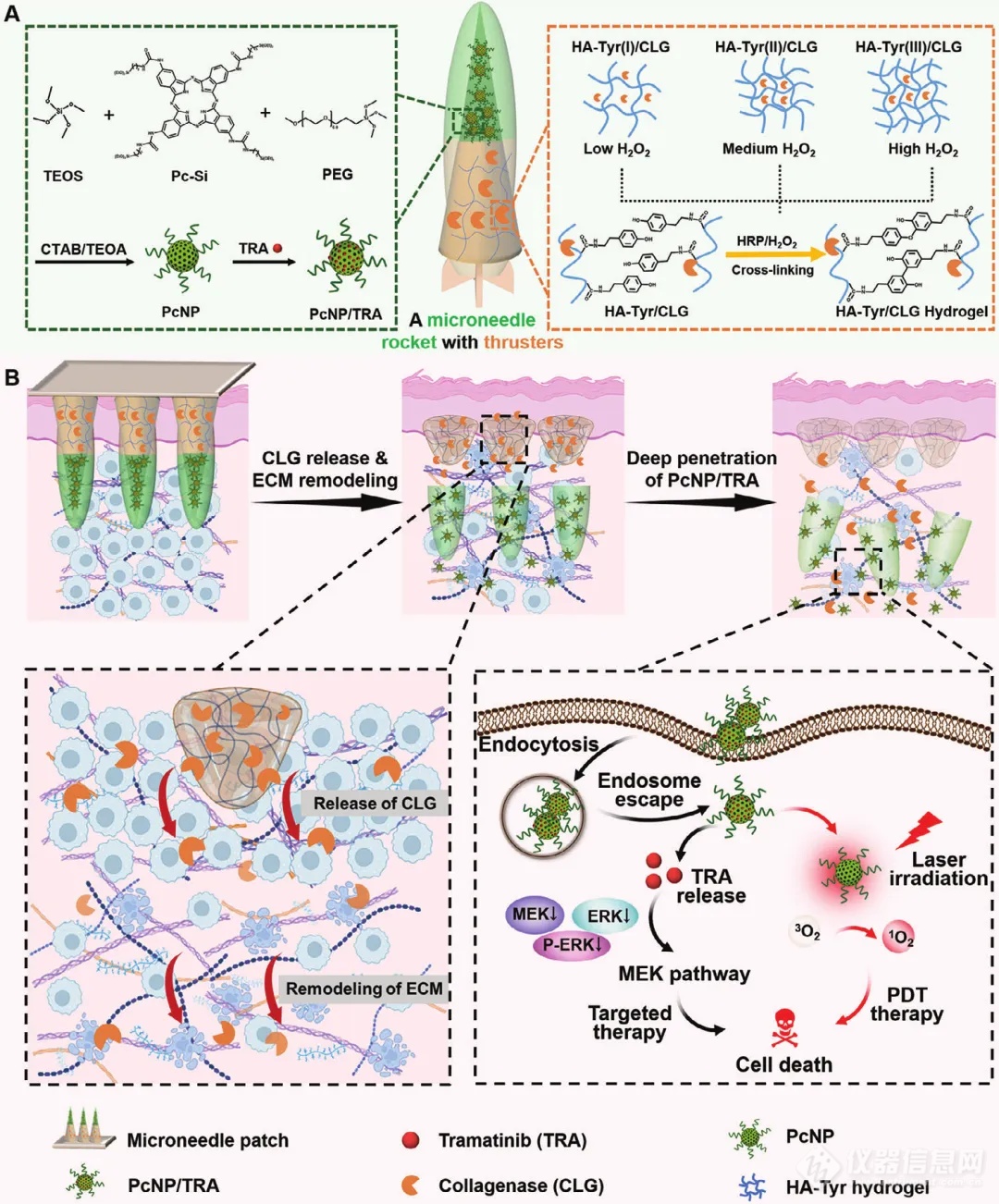

当“火箭式微针”穿透皮肤表皮时,MN的上层和下层发生分离。MN的下层在皮下膨胀形成水凝胶,调节CLG的释放,从而重塑致密的ECM,促进药物的扩散和分布。同时,MN上层的介孔二氧化硅纳米颗粒(PcNP/TRA)深入肿瘤内部并被黑色素瘤细胞内吞。一方面,TRA靶向黑色素瘤细胞过度激活的MEK通路,降低ERK激酶磷酸化水平。另一方面,Pc-Si响应外部红外光刺激,产生活性氧自由基,实现黑色素瘤的PDT治疗。最终,靶向疗法和PDT疗法共同发挥作用,高效杀伤肿瘤细胞,抑制黑色素瘤生长。
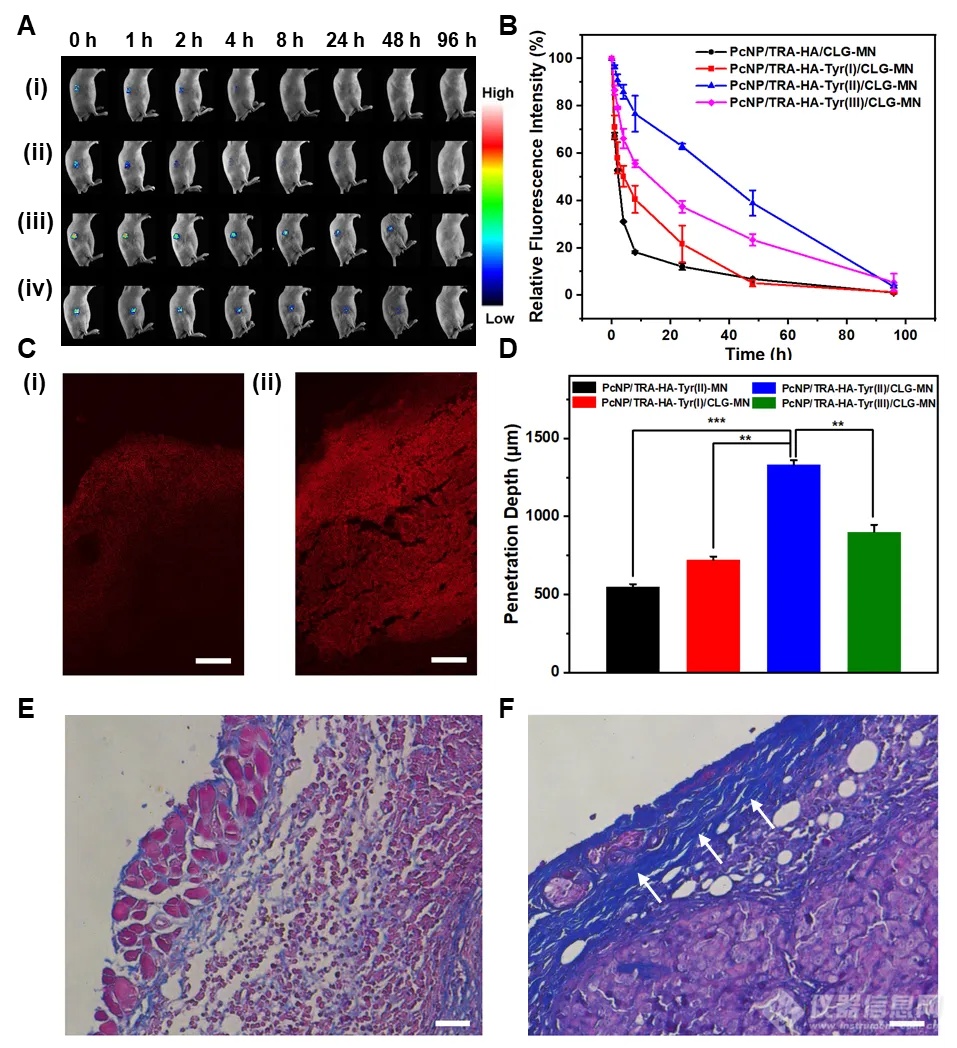
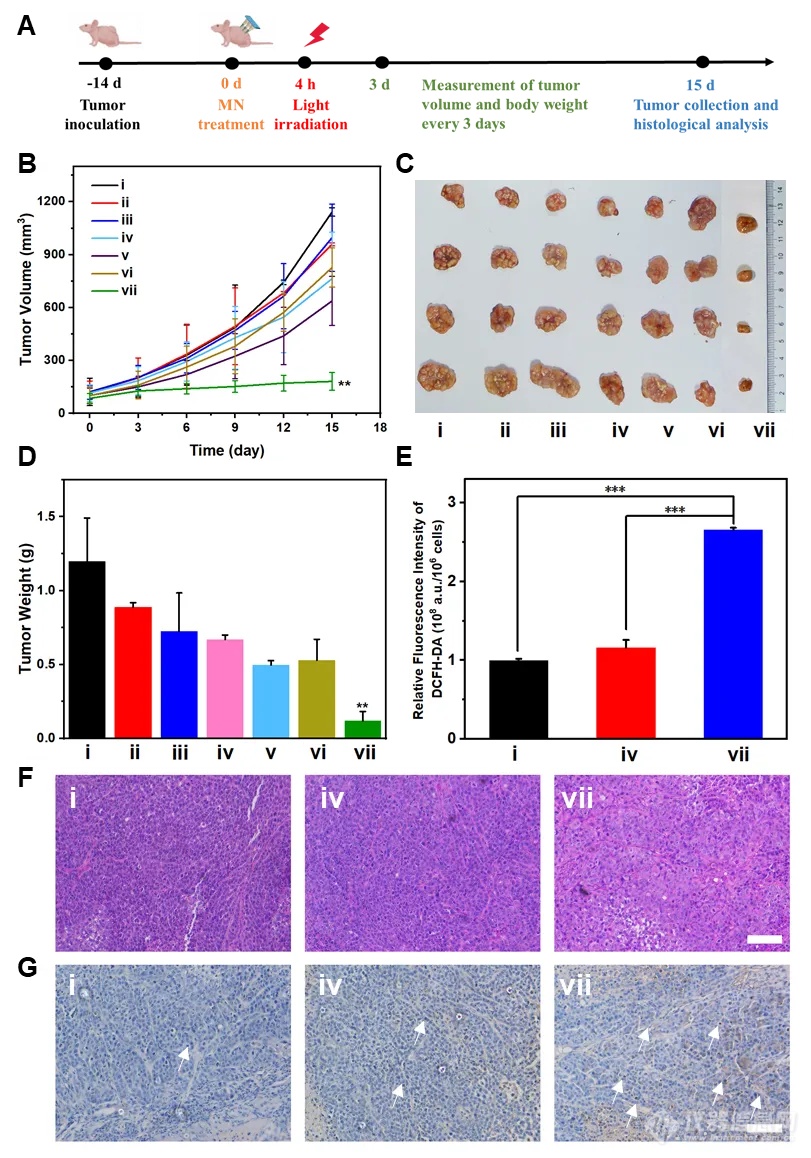
综上,作者采用“一石三鸟”策略设计了一种多功能“火箭式微针”递药系统,通过整合微针的穿透和CLG的助推器功能,促进药物在肿瘤组织的深度渗透。CLG助推器采用了一种类似火箭喷射的机制,能够在微针插入皮肤后自发启动,进一步推动纳米药物向深层组织渗透。这一设计不仅能提高药物的穿透深度,还能确保药物在肿瘤部位的有效浓度。该研究为药物深度穿透和黑色素瘤联合治疗提供了新途径,为微针技术在重要疾病治疗中的应用提供了新思路。
更多![]()
深圳大学苏磊课题组《Aggregate》:可穿戴微针贴片-用于抗利尿激素紊乱综合症智能早期预警
厂商
2024.10.25
产学研共谋医工融合,精密生物3D打印与前沿应用研讨会在长沙圆满落幕!
厂商
2024.10.24
微纳3D打印生态系统新升级!摩方推出ArchPost C100紫外固化箱
新品
2024.10.18
【第二轮会议通知】精密生物3D打印与前沿应用研讨会即将召开
厂商
2024.10.17








