Ä文献|探究血浆中纯化外泌体的最佳组合
细胞外囊泡 (Extracellular Vesicles, EVs) ,是由细胞释放的各种具有膜结构的囊泡结构的统称,这些囊泡的直径可以从30 nm到9 μm不等。细胞外囊泡主要可以分为3个亚群:
凋亡小体ApoBDs,囊泡尺寸较大(1~5 μm),结构组成多变;
微囊泡MVs,直径为150 nm~1 μm;
外泌体exosomes,直径范围为30到150 nm,也是目前研究火热的领域之一。
EVs广泛存在于人体的血液、乳汁、尿液以及唾液等多种体液中,其种类和数量与机体的生理状态息息相关。因此,EVs有望成为新型的疾病诊断标志物、纳米药物载体、治疗制剂和药物作用靶标,在疾病的诊断和治疗领域具有非常广阔的应用前景。
所有细胞都会将细胞外囊泡 (EV) 释放到血浆等生物液中。由于EVs的含量远低于血浆中的游离蛋白和脂蛋白,从丰度较高的游离蛋白和类似大小的脂蛋白中分离 EVs在技术上仍然具有挑战性。
近期,哈佛大学的一项研究使用了不同孔径的树脂的凝胶过滤层析法,分析比较了它们从血浆中分离得到EVs的得率,并评估去除游离蛋白和脂蛋白的效率,并开发了基于在同一层析柱中组合多种类型的层析填料的改进的EVs的分离方法。
评估不同琼脂糖含量分子筛的分离效果
首先,作者先评估了单步尺寸排阻层析 (Size Exclusion Chromatography, SEC) 填料Sepharose CL-2B、Sepharose CL-4B和Sepharose CL-6B的纯化效率对比,三种填料的琼脂糖交联度分别为2%、4%和6%,并使用Simoa测量每个收集组分中的CD9、CD63、CD81白蛋白和ApoB-100以评估纯化效率。
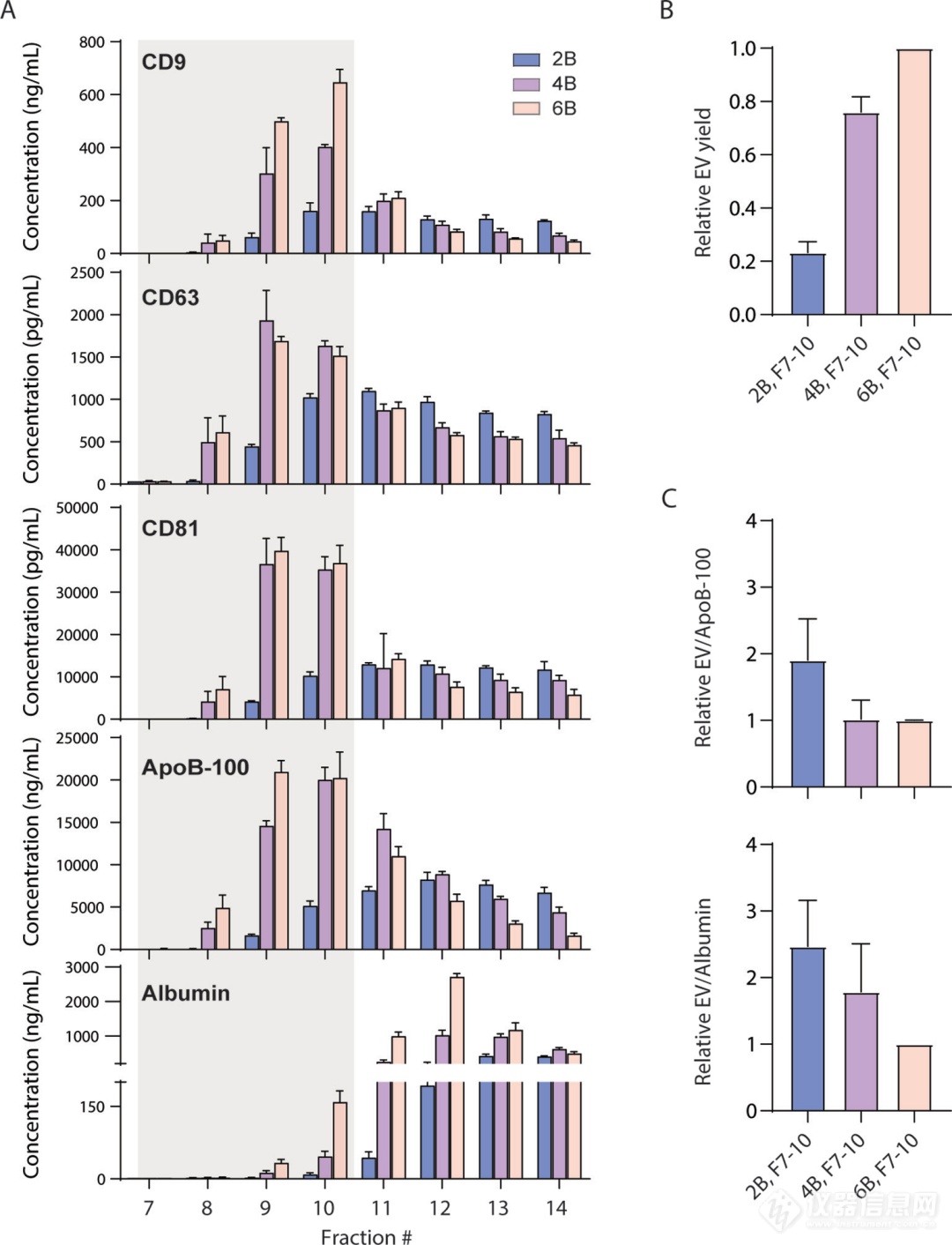
图1:使用不同树脂对血浆进行SEC凝胶过滤层析。
A
使用Sepharose CL-2B、Sepharose CL-4B或Sepharose CL-6B对1 mL血浆样品进行SEC后,收集的每个组分通过Simoa测量CD9、CD63、CD81、ApoB-100和白蛋白的水平。
B
统计Sepharose CL-2B、Sepharose CL-4B或Sepharose CL-6B分离后细胞外囊泡 (EVs) 产量,通过计算CD9、CD63和CD81比率的平均值,以组分7-10计算。
C
EVs相对于脂蛋白或游离蛋白的纯度通过相对EV产量(CD9、CD63和CD81比率的平均值)除以ApoB-10或白蛋的水平来计算。
结果发现,尽管在琼脂糖交联度最小的SEC填料Sepharose CL-2B中,EVs/ApoB-100的比率较高,纯度最好,但相对于其他两种SEC填料而言,这是以牺牲的EVs的产量收率为代价的,可以看到在三种SEC填料中Sepharose CL-2B收率最低。
测试纯化方案
作者接下来尝试了三种方案,单纯的SEC层析,与阳离子交换层析 (Cation exchange chromatography, CIEX) 叠加的双模式层析 (Dual-mode chromatography, DMC) ,以及SEC+CIEX+MMC(复合模式层析,Multimodal chromatography)的三模式层析方案 (Tri-Mode mixed-mode Chromatography, TMC) ,以0.5 mL的体积进行组分收集,检测组分中CD9、CD63、CD81白蛋白和ApoB-100的含量评估纯化效率。
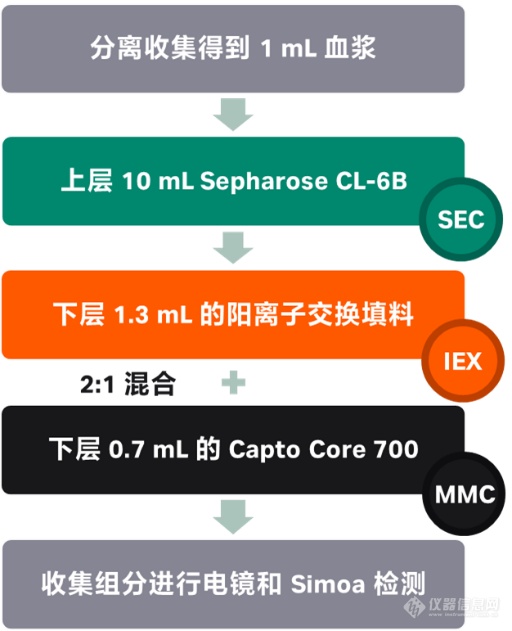
对于SEC层析方案,研究者选用10 mL柱体积的Sepharose CL-6B层析柱进行实验;
对于SEC+CIEX方案,由于EVs通常带负电荷,故选择阳离子交换填料用来分离EVs和脂蛋白,研究者装填了顶层10 ml Sepharose CL-6B,底层2 ml阳离子交换填料的双模式层析柱;
对于SEC+CIEX+MMC方案,研究者认为Capto Core 700这种多模式层析MMC填料在底层使用时,这种树脂会“捕获”在SEC过程中与EVs共同分离的游离蛋白质。研究者同样在顶层装填了10 ml Sepharose CL-6B填料,在底层以2:1的比例混合CIEX填料和MMC填料后进行装填。
装填好层析柱后,使用PBS清洗层析柱2次,每次加入5mL PBS洗液。随后取用1 mL血浆的血浆样品,在PBS洗液完全流出层析柱后进行上样。样品完全进入层析柱后,收集流出的0.5 mL的组分1。然后加入PBS,体积等于收集的一个组分体积 (0.5 mL) ,然后循环进行流出组分的收集,以及加入PBS的操作。对收集的组分记号留存备用。
对于EVs组分的评估实验,可在第6个组分(SEC方案)或第9个组分(DMC或TMC方案)收集结束后,一次加入四个组分体积的PBS (2 mL) ;然后在SEC层析方案取第7-10个组分,在DMC和TMC层析方案收集至9-12个组分。
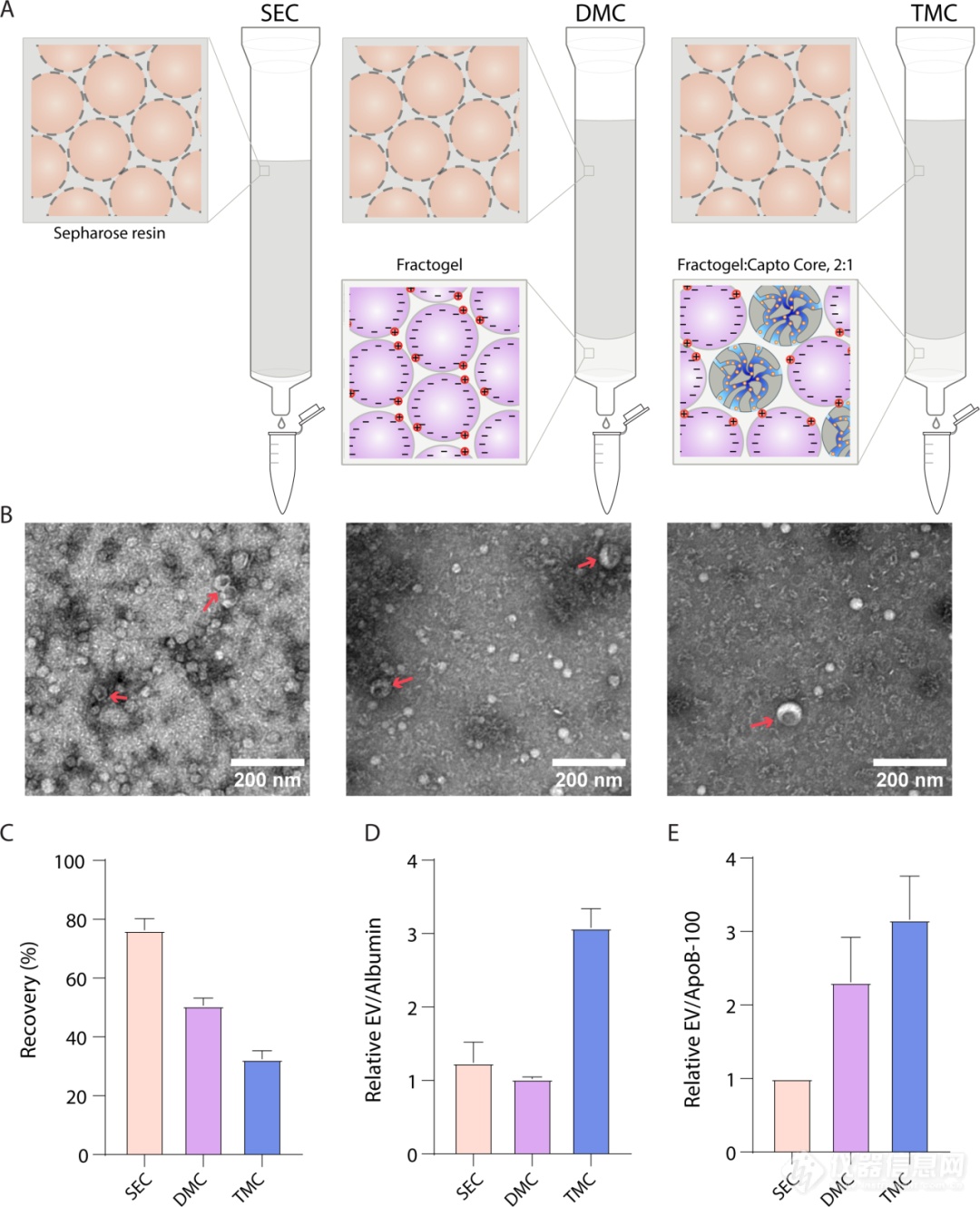
图2:运用电子显微镜和Simoa评估比较几种层析方案从血浆中纯化分离EVs的效果
A
三种层析柱装填示意图;
B
用SEC(左)、DMC(中)或TMC(右)柱从血浆中分离出的EVs的电镜图。红色箭头表示EVs;
C
计算从血浆中分离出SEC(组分7-10)、DMC(组分9-12)或TMC(组分9-12)的EVs回收率。指定组分中CD9、CD63和CD81蛋白的Simoa测量值与稀释血浆中这些蛋白的测量值的比值,然后取这三个比值的平均值来计算回收率;
D
EVs相对于游离白蛋白的纯度是通过在每种条件下相对EV产量(CD9、CD63和CD81比率的平均值)除以白蛋白的相对水平来确定的;
E
EVs相对于脂蛋白的纯度是通过在每种条件下相对EVs产量(CD9、CD63和CD81比率的平均值)除以ApoB-100的相对水平来确定的
研究者比较了使用SEC、DMC和TMC层析柱从血浆中纯化EVs的效果。研究者首先使用电子显微镜对每种层析柱的EVs进行成像,发现尽管脂蛋白仍然存在,但DMC和TMC的层析方式得到的EVs纯度高于脂蛋白(图2B)。
随后使用Simoa实验,将SEC、DMC和TMC柱对EVs、脂蛋白和游离蛋白的相对水平进行定量。标志物检测结果表明,与SEC层析柱相比,DMC和TMC层析柱明显地降低了ApoB-100和白蛋白的含量,但也导致了EVs产量的一些损失,特别是CD9。
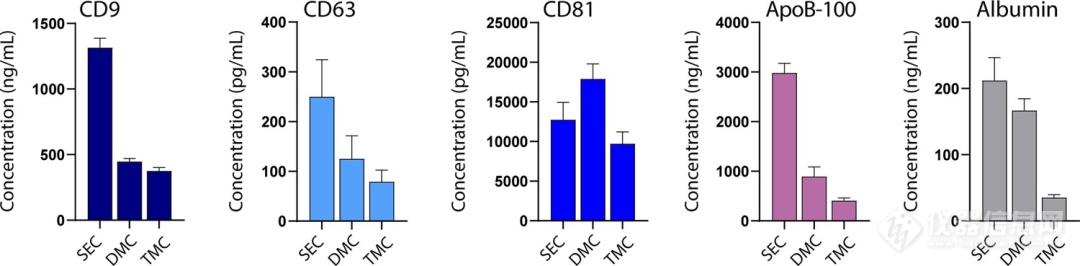
图3:凝胶过滤层析 (SEC) 、双模式层析 (DMC) 和三模式层析 (TMC) 中标记物水平的比较。
Simoa使用SEC(组分7-10)、DMC(组分9-12)或TMC(组分9-12)的样本测量从1 ml血浆分离的细胞外囊泡 (EVs) 样品中的CD9、CD63、CD81、ApoB-100和白蛋白水平。
结果也表明,DMC和TMC柱的EVs产量低于SEC,但TMC柱的EVs/白蛋白的比率以EVs/ApoB-100比率显着较高,DMC柱EVs/白蛋白的比率与SEC基本持平,EVs/ApoB-100比率显著较高(图2C-E)。
最后,为了评估用TMC分离的高纯度EVs的效用,作者进行了基于质谱的蛋白质组分析。对血浆中的EVs进行质谱分析通常是具有挑战性的,因为游离蛋白和脂蛋白的水平比EV蛋白的水平高几个数量级。使用TMC,能够从仅1 mL血浆中分离出的EVs中检测到780种蛋白质,丰度远高于常规的三步法(PEG沉淀+碘己醇梯度分离+SEC)。这些结果证明了使用TMC进行小样本量深度蛋白质组学分析的优势。
小 结
作者最后总结,无论是最大化EVs产量的单模式SEC,还是最大化EVs纯度的三模式TMC,层析方式都是从临床样本中分离EVs的有力平台,具有价格便宜,工艺更稳定且运行时间短等特点。传统的密度梯度离心法通量较低且耗时,因此不适合于临床样品的EVs分离。
分离EV的最佳方法并不存在,因为选择的分离方法必须与其后续的应用相匹配。该研究后续需要极高纯度EVs,因而开发了TMC层析柱。作者预计TMC层析柱对于利用蛋白质组学发现EVs生物标志物将发挥巨大作用,因为EVs被其中脂蛋白和游离蛋白污染会阻碍深度覆盖,而TMC层析方式显著的降低了这些杂蛋白的混入。未来可利用并行运行层析柱的自动化设备,实现基于层析柱的方法处理临床样品的途径,该设备未来的迭代将进一步提高样本吞吐量。本研究开发的方法将有助于实现分子诊断中的EVs纯化分析。
更多![]()
美谷分子微生物筛选系统 QPix亮相央视晚间新闻 ,助力创新中国
厂商
2024.07.11
推动生物合成学的创新解决方案
厂商
2024.07.11
如何科学延长超速离心机的使用寿命?
厂商
2024.07.08
高效自动化胶囊装填系统:专为临床试验量身定制的优化方案
厂商
2024.07.04








