从法规角度谈谈药物溶出度、溶出度仪
溶出度系指活性药物成分从片剂、胶囊剂或颗粒剂等制剂在规定条件下溶出的速率和程度,在缓释制剂、控释制剂、肠溶制剂及透皮贴剂等制剂中也称释放度。
2015《中国药典》从药品质量控制的角度对体外溶出度试验进行了规范。

药物的吸收取决于药物从制剂中的溶出或释放、药物在生理条件下的溶解作用以及在胃肠道的生物膜渗透性。由于药物的溶出和溶解具有重要影响,因此体外溶出试验有可能预测其体内行为。

建立普通口服固体制剂(如片剂和胶囊)体外溶出度试验方法,有下列作用:
评价药品批间质量的一致性
指导新制剂的研发
在药品发生某些变更后(如处方、生产工艺、生产场所变更和生产工艺放大),确认药品质量和疗效的一致性。

通过研究载体、辅料、剂型等对药物溶出度的影响,能科学地筛选出辅料的品种、最佳处方和最佳剂型。
随着溶出度试验的不断改进和完善,测定品种数目的不断增加,制药领域对溶出度设备的自动化、准确性、稳定性要求越来越高。
Raytor溶出仪符合USP、中国药典的要求,具备适应从手工操作到全自动化和高通量分析的实验系列工作流程的灵活性,软件具有权限管理、审计追踪等功能,提供3Q认证服务、完整溶出的实验解决方案。

自动取样
Raytor溶出仪配置八通道或十二通道高精度注射泵,能高效地在每个时间点提供准确而精密的自动取样。
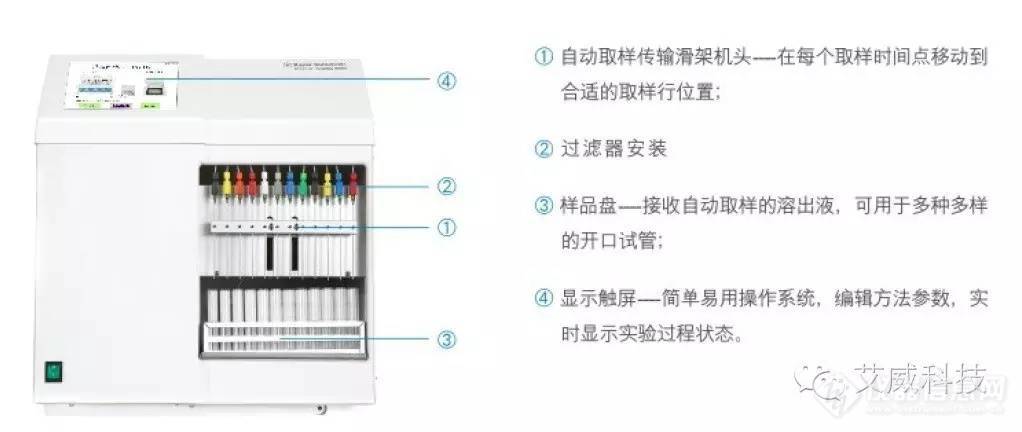
溶出度仪驱动头自动升降
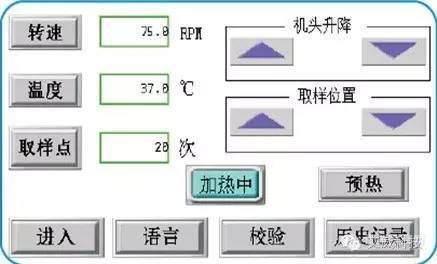
采用智能自动升降方式,确保搅拌轴的设置高度、中心位置等关键参数实验条件的重现性

按GMP法规的项目要求校准(一致性评价)
按法规要求,在设备导入、合适的时间间隔、设备搬迁、设备有较大改动时应实施校正。
机械校正
可调整测量溶出杯的水平度、中心度、搅拌桨的高度、回转轴的晃动度、转数等。

化学校正
使用USP标准药剂进行试验
? 崩解型制剂用 10 mg 强的松片
? 非崩解型制剂用 300 mg 水杨酸片
符合USP/FDA 等法规要求
使用非驻留式温度探头在预设时间点检测溶出介质温度。软件系统按权限分级管理,仪器内置热敏打印功能,输出实验过程关键状态数据,文档化,满足相关法规要求。

国家近期对制药领域的投入加大,药品一致性评价的要求将使溶出度仪的需求将有一个爆发式的增长。Raytor溶出度仪满足新药典、新GMP一致性评价所特有的要求,高效、稳定、准确。
更多![]()
我公司代表参加第四十届迪拜实验仪器设备展
厂商
2022.11.23
又一标准发布并实施!天隆参与!
厂商
2024.05.27
会议邀请 | 2024无机分析技术研讨会暨第十六届珀金埃尔默原子光谱用户会
厂商
2024.07.12
解决方案 | 更高效精准地检测高无机碳水中总有机碳
厂商
2024.07.17