搜全站
搜展位
赛默飞方案 | 仿制药一致性评价 PE/BE 解决方案
药品审评审批制度改革已经是上升到国家层面的重大决策部署,其中仿制药质量和疗效一致性评价 是其中事关民众健康、企业兴衰的重大举措。国务院办公厅 2016 年 8 号文《关于开展仿制药质量和疗 效一致性评价的意见》显示了政府改变现有仿制药评价、审批制度的强大决心,而国家食药监局(CFDA) 在 2016 年 106 号文中首次公示了第一批 2018 年底前须完成仿制药一致性评价的 289 个品种,涵盖了 国家医保药物名录中最常用的药物,预示着仿制药一致性评价的大幕正式拉开! 2018 对每一个仿制药 生产企业来说都至关重要!
紧迫性……
对于药企来说,顺利完成一个仿制药品的一致性评价周期大约需要 23 个月!而今天…… 赛默飞世尔科技以其强大的创新实力和完整而优质的产品线,为您提供自动化、数 据化(合规)和高效率的“仿制药一致性评价分析检测解决方案”,与您从以下四个方面一起从容 面对 PE/BE 各项流程!
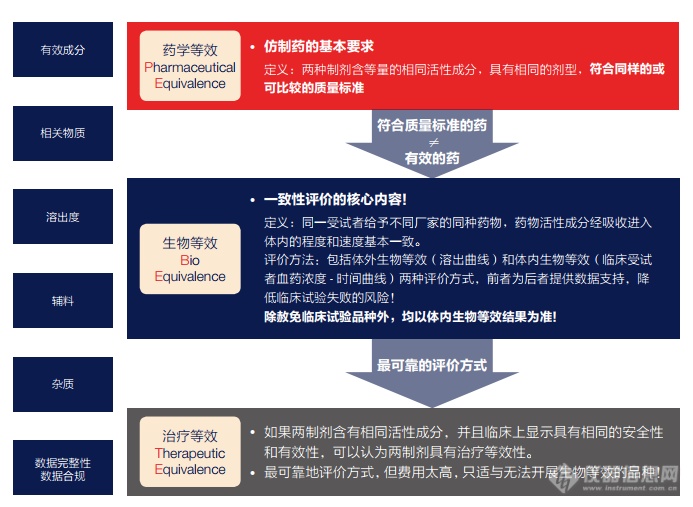
药物等效性评价
生物等效性评价
方法学验证、快速数据处理方案
数据合规性支持方案
点击 仿制药一致性评价 PE/BE 解决方案 查看详细解决方案!
扫描下方二维码即可获取赛默飞全行业解决方案,或关注“赛默飞色谱与质谱中国”公众号,了解更多资讯

最新动态
更多![]()
微塑料表征新方案| 利用单颗粒ICP-TOF-MS进行多元素指纹分析
厂商
2024.09.26
Stellar MS高通量PRM靶向定量,加速转化医学研究
厂商
2024.09.24
新国标应对—GB 5009.298-2023 食品中三氯蔗糖(蔗糖素)的测定
厂商
2024.09.24
赛默飞科技引领未来 —— 诚邀您出席第十四届环境毒理学与化学学会亚太国际会议
厂商
2024.09.20
推荐产品
供应产品