Є’µљ“їЉ“–¬µƒєЂЋЊ…ѕ∞а£ђ“тќ™√ї”–љ” №єэ÷ ЅњЈљ√жµƒ≈а—µЇЌє§„чЊ≠—й£ђЋщ“‘’вЄцќ ћвћб≥цњ…ƒ№”––©–¶ї∞µƒ≥…Ј÷£ђ „ѕ»‘Џ’вјпЋµ√ч“їѕ¬£ђѕ£ЌыіуЉ“≤ї“™љй“в°£
єЂЋЊ µ—й “ «‘Џ»•ƒкƒкµ„Ќ®єэЅЋCMAµƒ∆ј…у£ђµЂ «јѕµƒ“ї≤њЈ÷»ЋЉЄЇх»Ђ≤њ„яєвЅЋ£ђ µ—й “‘Џ’в“їƒкјп√ж“≤ЉЄЇх√ї”–єэ’э≥£µƒ‘Ћ„ч£ђѕ÷‘Џјѕ∞е’–±ш¬т¬н„Љ±Є“™ƒ√ѕ¬CNASµƒ»ѕ÷§£ђЄ–ЊхјІƒ—≤ї–°°£“тќ™CMAЈҐ≤ЉЅЋ„о–¬µƒ∆ј…у“™«у£®≤ї÷™µј’в√і±ніп’э≤ї’э»Ј£ђЌы÷Є≥ц£©£ђЋщ“‘ґ‘”Џ‘≠”–µƒћеѕµќ“√«ѕл÷Ў–¬Ќ∆Ј≠÷Ў–¬љ®ЅҐ£ђ÷ Ѕњ ÷≤бїї∞ж£ђѕ£Ќы‘Џґ‘’’CNASµƒ∆ј…у„Љ‘тљш––±а÷∆ћеѕµ£ђЌђ ±“≤“™Љ”»л–¬µƒ„ ÷ »ѕґ®∆ј…у„Љ‘тµƒƒЏ»Ё£ђµЂ «≤ї÷™µј»зЇќЉ”»л£ђітЋгѕ»љЂ∆ј…у„Љ‘тµƒґ‘’’±н„ц≥цјі£ђµЂ «≥цѕ÷ЅЋ“їЄцќ ћв£ђ–¬µƒ„ ÷ »ѕґ®∆ј…у„Љ‘тЇЌ“‘«∞Ќк»Ђ≤ї“ї—щЅЋ£ђ≤ї÷™µј»зЇќ»•”л‘≠јіµƒЄс љґ‘”¶∆рјі£ђЌыіу ¶√«ƒ№÷Єµг“їѕ¬°£
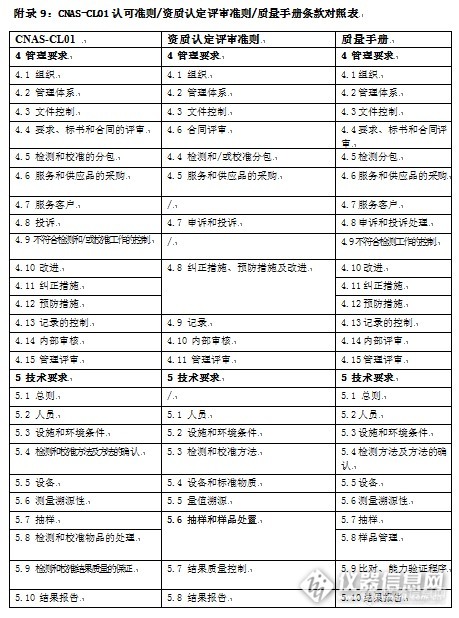
ѕ¬ЌЉ «‘≠”–µƒґ‘’’±н£Ї