 回复yulihuagong发表于:2014/10/21 10:22:19
回复yulihuagong发表于:2014/10/21 10:22:19悬赏金额:
10积分 状态:
已解决
请各位大侠帮忙,我需要检测的体系中有乙酸,还有硝酸,但是我想检测出硝酸的含量,那我是不是就只能检测硝酸根的含量了,请各位帮忙,如何检测?谢谢!
 hhx050 回复于:2014/10/27 14:35:18
hhx050 回复于:2014/10/27 14:35:18硝酸含量的测定使用酸碱滴定即可。先配置氢氧化钠的溶液,用标准的硫酸溶液滴定出其准确浓度,再用氢氧化钠溶液滴定出硝酸的浓度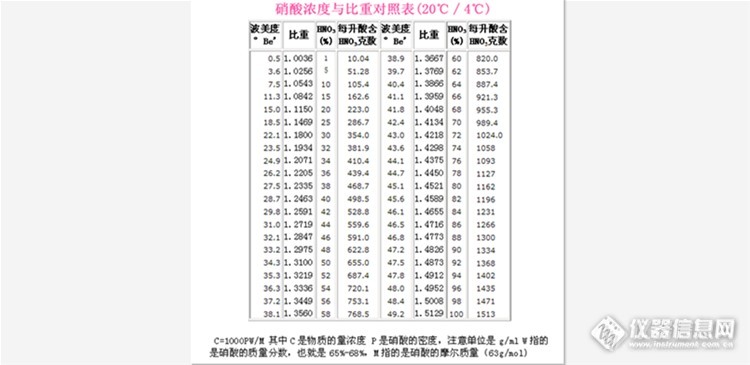 1、当量浓度=1000.d.质量百分浓度/E;
1、当量浓度=1000.d.质量百分浓度/E;
2
、质量百分浓度=
当量浓度E/1000.d
;3
、摩尔浓度=1000.d
质量百分浓度/M
;4
、质量百分浓度=
质量-
体积浓度(毫克/
升)/104.d
;5
、质量-
体积浓度(mg/L
)=104
质量百分浓度;ppm
是重量的百分率,ppm=mg/kg=mg/L
,即:1ppm=1ppm=1000ug/L
,1ppb=1ug/L=0.001mg
,式中:E
—溶质的克当量;d
—溶液的比重;M
—溶质的摩尔质量;硝酸根离子的检验方法用品:试管、试管架、试管夹、量筒;硝酸钾、硫酸亚铁、浓硫酸。原理:硝酸根离子有氧化性,在酸性溶液中能使亚铁离子氧化成铁离子,而自己则还原为一氧化氮。一氧化氮能跟许多金属盐结合生成不稳定的亚硝基化合物。它跟硫酸亚铁反应即生成深棕色的硫酸亚硝基铁:3Fe2++NO3-+4H+=3Fe3++2H2O+NO FeSO4+NO=Fe
(NO
)SO4
实验室里常利用这个反应检验硝酸根离子,称为棕色环试验。这种简单亚硝基化合物只存在于溶液内,加热时,一氧化氮即从溶液内完全逸出。亚硝酸根离子也能发生类似的反应。要区别这两种酸根离子可以用浓磷酸,亚硝酸根离子能显现深棕色而硝酸根离子却不能。准备和操作:往试管里注入3
毫升1
摩/
升的硝酸钾溶液和3
毫升1
摩/
升的硫酸亚铁溶液,振荡试管,混和均匀。斜持试管,沿试管壁慢慢注入浓硫酸3
毫升(图7-97
),使密度较大的浓硫酸沉入试管的底部,跟硝酸钾和硫酸亚铁的混和溶液分成两层。稍待片刻,把试管慢慢竖直,不久,两层液体间就有一个棕色的环生成。注意事项:硫酸亚铁必须是新制备的,硫酸必须是浓的。操作时不能把溶液冲浑。其它实验方法:适用于固态的硝酸盐或相当浓的硝酸盐溶液。把少量的硝酸盐晶体或浓溶液置于试管内,然后加入少量浓硫酸(1
∶1
)。再向试管内加入一小块铜片。给试管加热,有红棕色气体产生,则证明含有硝酸根离子。
